Chirurgická léčba hormonálně aktivních adenomů hypofýzy
Surgical treatment of hormonally active hypophysial adenomas
There had been treated 277 patients with pituitary adenoma in period from 1999 to 2003 at Department of Neurosurgery, Central Military Hospital, Prague. Altogether there had been treated 108 patients with hormone-secreting adenomas. Normalization or sufficient hormone level decrease was observed in 61 patients after the first surgery. Hormone level decrease was not sufficient in remaining cases. Second surgery was performed in 18 cases, medicamental treatment was indicated in 17 cases, radiosurgery was applied in 34 cases. There was no mortality after transsphenoidal surgery, morbidity was observed in 2 cases (visual impairment in 1 case, CSF leak in 1 case). Permanent adiuretine substitution is needed in 7 cases.
Key words:
pituitary adenoma – hormone-secreting – trassphenoidal surgery
Autoři:
V. Masopust 1; D. Netuka 1; V. Hána 2; J. Marek 2; V. Beneš 1
Působiště autorů:
Neurochirurgická klinika 1. LF UK, IPVZ a ÚVN Střešovice, Praha
1; 3. interní klinika 1. LF UK a VFN, Praha
2
Vyšlo v časopise:
Cesk Slov Neurol N 2007; 70/103(4): 402-406
Kategorie:
Krátké sdělení
Podpořeno grantem IGA MZ ČR NR 8052-3
Souhrn
Od roku 1999 do roku 2003 bylo na Neurochirurgické klinice 1. LF UK, IPVZ a ÚVN Praha operováno celkem 277 nemocných s adenomem hypofýzy. Z tohoto počtu bylo 108 pacientů s hormonálně aktivními adenomy hypofýzy. K normalizaci nebo k dostatečnému poklesu hormonální hladin došlo u 61 pacientů po první operaci. V 47 případech nebyl hormonální pokles po první operaci dostatečný. Celkem v 18 případech byla indikována sekundární operace, pooperační medikamentózní léčba byla indikována u 17 pacientů, na Leksellově gama noži bylo ozářeno 34 pacientů. Po transsfenoidální operaci byla mortalita nulová, morbidita byla zaznamenána u 2 pacientů (1× trvalé zhoršení zraku, 1× likvorea). Trvalá substituce adiuretinem je nutná u 7 pacientů.
Klíčová slova:
adenom hypofýzy – hormonálně aktivní – transsfenoidální operace
Úvod
H. Cushing provedl první transsfenoidální operace již v roce 1910, čímž položil základ pro budoucí chirurgickou léčbu adenomů hypofýzy [1,2]. Postup se však sám zavrhl ve prospěch transkraniálních operací. K renesanci transsfenoidálního přístupu poté došlo až v 60. letech minulého století, na popularizaci tohoto přístupu se výrazně podílel J. Hardy [3]. První transsfenoidální operaci v ÚVN provedl otorinolaryngolog E. Černý, poté se touto problematikou zabýval zejména I. Fusek, který tento přístup používal od roku 1971 [4-6].
Detailní rozbor komplikací transsfenoidálních operací publikovali Náhlovský et al. v roce 2004 [7].
Hormonálně aktivní adenomy hypofýzy jsou léčeny buď pro své expanzivní chování a s tím spojené klinické příznaky, častěji však pro zvýšené hormonální hladiny. Současný pohled spočívá v kombinaci 3 léčebných modalit: a. medikamentózní léčba, b. chirurgická léčba, c. ozáření reziduálního, či recidivujícího adenomu hypofýzy, obvykle na Leksellově gamma noži (LGN). Jednotlivé modality se vzájemně nevylučují, naopak jsou komplementární. Pouze komplexní léčbou lze dosáhnout dobrých výsledků klinických i endokrinologických při minimální morbiditě a prakticky nulové mortalitě. Specifikem našeho pracoviště je jednak nejvyšší počet operací adenomů hypofýzy v ČR a výborná spolupráce zejména se III. interní klinikou 1.LF UK a oddělením stereotaktické a radiační neurochirurgie, nemocnice Na Homolce. Proto předkládáme současné výsledky.
Materiál a metodika
Od roku 1999 do roku 2003 bylo na neurochirurgické klinice 1. LF UK, IPVZ a ÚVN Praha operováno celkem 277 nemocných s adenomem hypofýzy. Z celkového počtu bylo 108 pacientů s hormonálně aktivními adenomy hypofýzy, u kterých jsme provedli 124 operací. Záměrně nehodnotíme pacienty z roku 2004–2005, protože 1roční sledování považujeme za zcela minimální požadavek pro hodnocení výsledků, preferujeme dvouroční odstup od operace při hodnocení výsledků.
Nadprodukci somatotropního hormonu (STH) mělo celkem 57 pacientů, adrenokortikotropního hormonu (ACTH) 32 pacientů, folikulostimulačního hormonu (FSH) 1 pacient a tyreotropního hormonu (TSH) 1 pacient (tab. 1). V 17 případech jsme operovali pacienty s nadropudkcí prolaktinu (PRL), indikací k operační léčbě bylo zhoršení zraku i přes medikamentźní léčbu (14 případů), nebo nedostatečný efekt léčby D2 agonisty stran hladiny prolaktinu (3 případy). U všech 17 pacientů bylo předoperačně známo, že se jedná o prolaktinom, tj. ani v jednom případě nebyl pacient operován bez znalosti hormonální aktivity adenomu. Pokud nedochází ke ztrátě zraku u pacientů s prolaktinomy v řádu hodin, poté nejprve doporučujeme medikamentózní léčbu. Jakmile nedojde ke zlepšení zraku během medikamentózní léčby (standardně po 3 týdnech léčby), poté indikujeme operační léčbu.
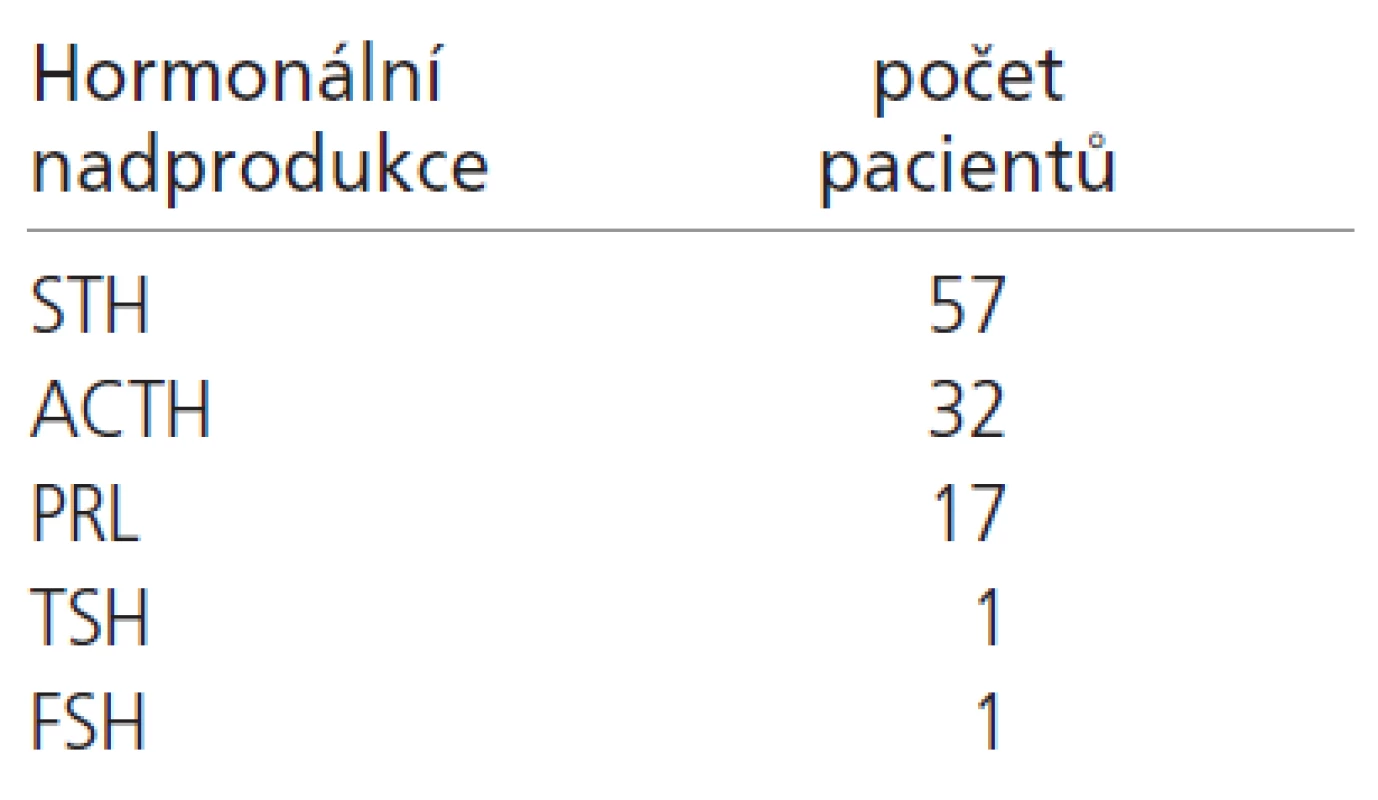
Průměrný věk nemocných byl 43,6 let (nejmladší 18 let, nejstarší 72 let). Soubor tvoří 61 žen a 47 mužů. Během 124 operací byly použity tyto přístupy: primární transsfenoidální resekce 104x, primární transkraniální resekce 2x, sekundární transsfenoidální operace 11x, sekundární transkraniální resekce 7x (tab. 2). Ve 35 případech se jednalo o mikroadenomy (8x STH produkující adenomy hypofýzy, 27x ACTH produkující adenomy hypofýzy), v 73 případech o makroadenomy.

Kritéria endokrinologické úspěšnosti operace:
- prolaktinom: normální hladina prolaktinu pro muže < 15 ug/l, pro ženy < 20 ug/l.
- akromegalie: GH-OGTT < 1ug/l, IGF-1 normální hladina závislá na věku a pohlaví
- Cushingova choroba: volný močový kortizol během 24 hodin < 210 nmol/den,
- dexametazonem supresibilní plazmatický kortizol (tj. když 1 mg dexamatazonový test < 80 nmol/l), restituce diurálního rytmu kortizolu.
Námi používaná chirurgická technika:
- přístup sublabiální není již tak častý, ale použitelný u všech pacientů. Sublabiální přístup přináší o několik milimetrů větší operační pole. Tento přístup indikujeme u pacientů s gigantickými adenomy, výběrově u pacientů s makroadenomy. V těchto případech, byť jen minimálně, větší operační pole umožní lepší peroperační orientaci a umožní použití většího množství nástrojů. Dále tento přístup používáme u pacientů s extrémně malými nosními dírkami.
- přímý endonazální přístup, kdy vstupujeme pod sliznici až při vchodu do sfenoidální dutiny. Používán jej nyní rutinně, avšak zvládnutí případné peroperační komplikace je obtížnější, zejména protože je tento přístup ještě menší než při předchozí přístup. Za užitečné považujeme použití bezrámového navigačního systému.
- postup endoskopický, který používáme od druhé poloviny roku 2004. Nevýhodou této metodiky je opět obtížné řešení případných peroperačních komplikací. Zároveň není příliš vhodný pro objemné adenomy. Rutinně používáme kontrolu polohy nástrojů pomocí bezrámového navigačního systému.
Do spodiny sedla vytváříme otvor vysoobrátkovou frézou. Za minimální považujeme otvor 8x6 mm, v případě potřeby jej rozšiřujeme. Řez tvrdou plenou má tvar písmene X. Odstraňujeme nádor od baze tak, aby nádorové hmoty postupně klesaly. Zpočátku tedy ze spodiny sedla a laterálních stěn. Pokud dojde k poklesu diafragmatu a operační pole je dostatečně přehledné, lze tento výkon považovat za radikální. Ovšem pokud k poklesu nedojde, je možné resekční dutinu vyplnit kontrastní látkou a provést skiaskopickou kontrolu rozsahu resekce adenomu. V současné době je však výhodnější prohlédnutí vzniklé dutiny za pomoci endoskopu s 45° optikou.
Výsledky
K normalizaci nebo k dostatečnému poklesu hormonálních hladin došlo po první operaci u 61 pacienta (56,5 %). Ve 47 případech (43,5 %) nedošlo k dostatečnému poklesu hladin hormonů po první operaci. Sekundární operace byla provedena v 18 případech (16,6 %). Medikamentózní léčba byla aplikována i po operaci u 17 pacientů (17,1 %). Následné ozáření na LGN podstoupilo 34 nemocných (31,4 %). Po transsfenoidální operaci byla nulová mortalita a 2% morbidita (1x permanentní zhoršení poruchy zraku, 1x likvorea).
Výsledky dle jednotlivých skupin :
PRL secernující adenomy: U 6 pacientů (35 %) došlo k dostatečnému hormonální poklesu po operaci, 11 pacientů (65 %) bylo léčeno D2 agonisty i po operaci. Celkem 8 pacientů (47 %) pacientů vyžadovalo hormonální substituci (tab. 3).

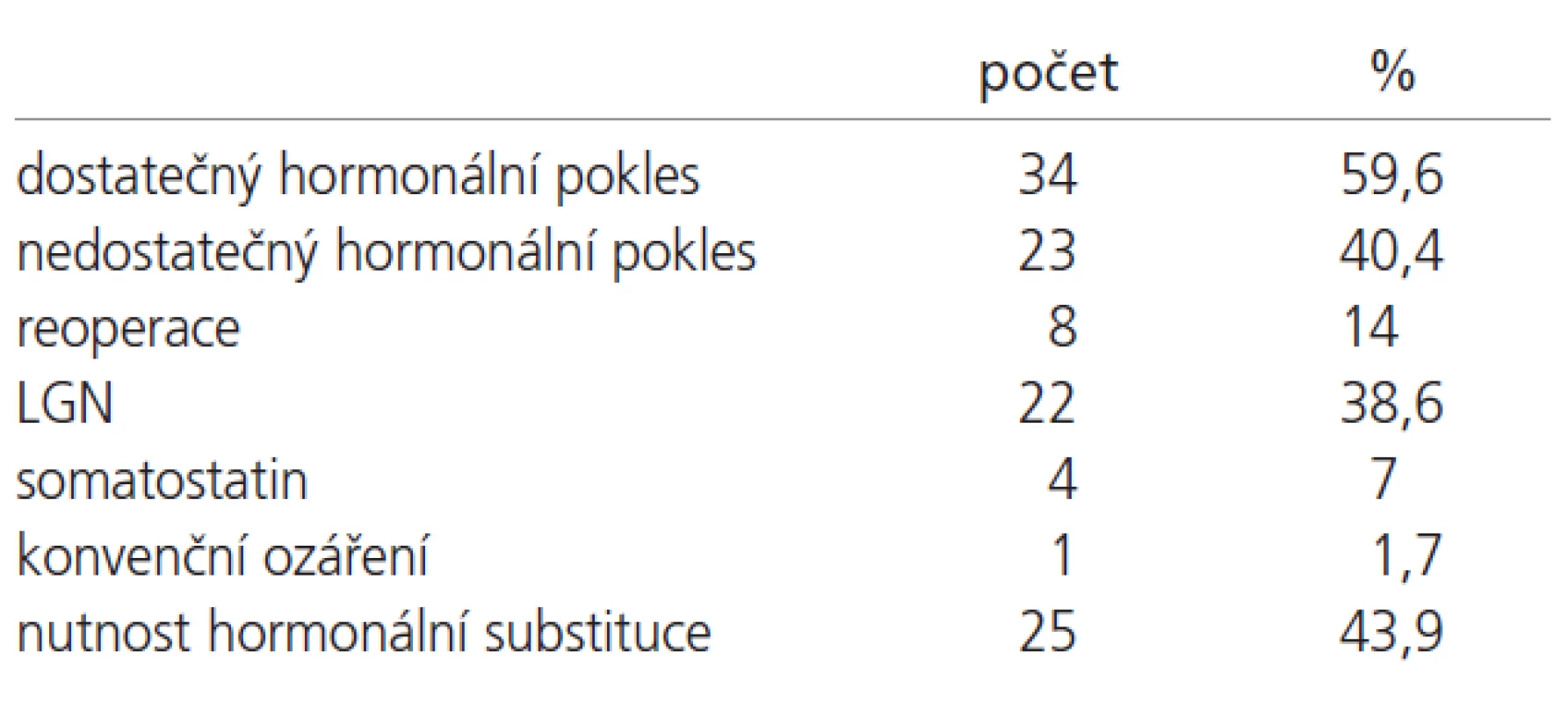
STH secernující adenomy: Dostatečný hormonální pokles u 34 pacientů (59,6 %). Celkem 23 (40,4 %) pacientů vyžadovalo další léčbu: reoperace 8x (14 %), ozáření na LGN 22x (38,6 %), následná léčba somatostatinem 4x (7 %), konvenční ozáření 1x (1,7 %). Po první operaci bylo 32 pacientů (56,1 %) bez nutnosti hormonální substituce (tab. 4).
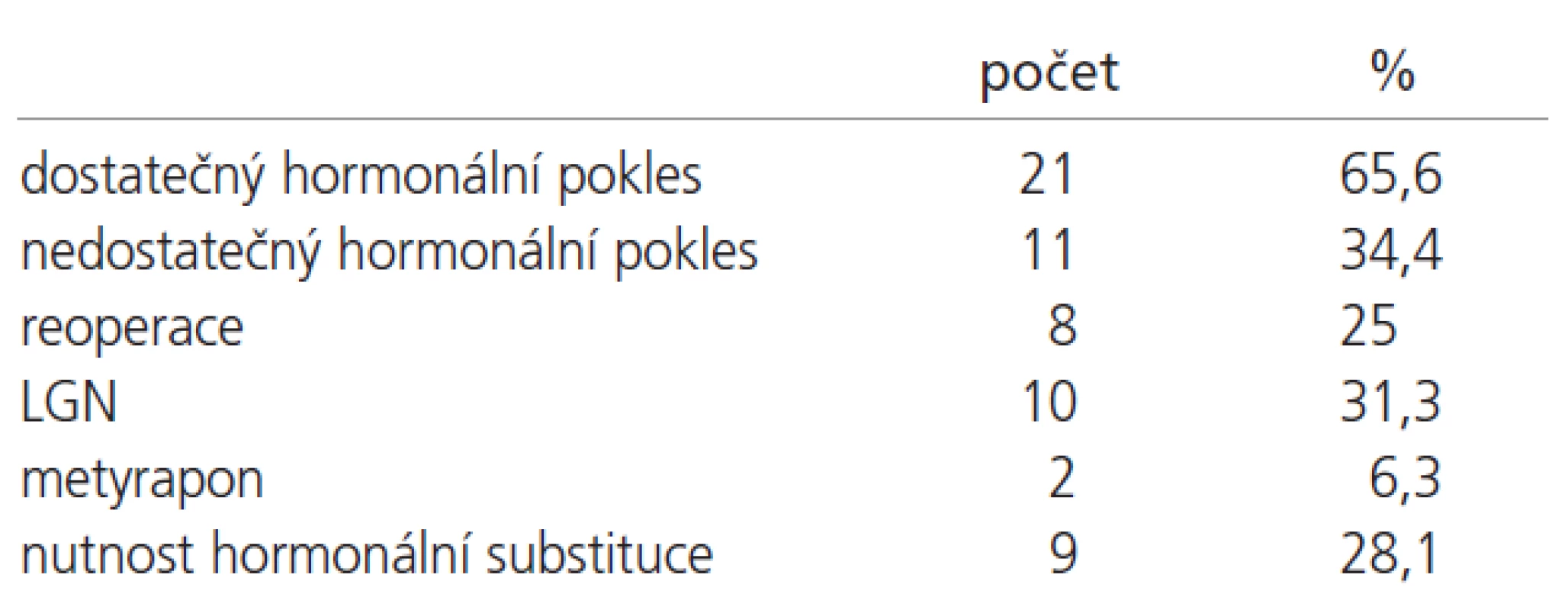
ACTH secernující adenomy: 21 nemocných (65,6 %) mělo dostatečný hormonální pokles po první operaci. Ve zbylých 11 případech (34,4 %) byl použit následující kombinovaný přístup: reoperace 8x (25 %), ozáření na LGN 10x (31,3 %), léčba metyraponem 2x (6,3 %). Celkem 9 pacientů (28,1 %) pacientů vyžadovalo hormonální substituci (tab. 5).
Komplikace: v jednom případě se vyskytla pooperační likvorea, která byla řešena lumbální drenáží a následně operační revizí. K trvalému zhoršení zraku na jednom oku došlo 1x, k přechodnému zhoršení zraku došlo též 1x. Celkem 7 pacientů vyžaduje dlouhodobě substituci adiuretinem.
Diskuse
Chirurgickou léčbu lze považovat za úspěšnou pouze v případě úpravy nadprodukce hormonů a při současné absenci pooperačního hypopituitarizmu. V případě, že nedojde k dostatečnému hormonálnímu poklesu, lze zvolit některou z dalších léčebných alternativ. Výsledný stav je poté dosažen vhodným načasováním ozáření na LGN a medikamentózní léčbou na endokrinologickém pracovišti.
Pouze u 35 % pacientů s prolaktinomy došlo po operaci k dostatečnému hormonálnímu poklesu. Zde je však nutné opět zdůraznit fakt, že indikace k operaci byla v naprosté většině případů (v 82,4 %) jiná než endokrinologická (progredující porucha zraku). Nomikos et al uvádějí úspěšnost chirurgické normalizace hladin prolaktinu v 54-86 % případů [8]. Nelze však opomenout fakt, že v jejich sérii byly hodnoceny i prolaktinomy z doby před érou farmakologické léčby D2 agonisty. V tomto období byli indikováni k chirurgické léčbě i pacienti s mikroadenomy hypofýzy secernujícími PRL. My jsme pochopitelně takový mikroadenom neoperovali ani jeden, všichni naši pacienti měli makroadenomy, u kterých musíme očekávat horší endokrinologické výsledky. Kristof et al hodnotili pouze makroadenomy a dosáhli hormonální normalizace u 27 % pacientů po operaci [9].
Indikace k chirurgické léčbě prolaktinomů: pokud nedochází ke ztrátě zraku v řádu hodin, poté nejprve doporučujeme medikamentózní léčbu. Jakmile nedojde ke zlepšení zraku během medikamentózní léčby (standardně po 3 týdnech léčby), poté indikujeme operační léčbu. Z této indikace jsme operovali celkem 14 pacientů s prolaktinomy. V relativně vzácných případech, kdy prolaktinom nedostatečně reaguje na medikamentózní léčbu (stran hladiny prolaktinu), poté po dohodě s endokrinology indikujeme operaci. Z této indikace jsme operovali pouze 3 pacienty s prolaktinomy.
Nomikos et al publikovali úspěšnost chirurgické léčby STH produkujících adenomů v 57,3 % z 506 primárních transsfenoidálních operací, námi dosažené výsledky jsou obdobné (59,6 %) [10]. Erturk et al dosáhli endokrinologického vyléčení u mikroadenomů v 63 % případů, u makroadenomů v 15 % [11].
Ve skupině pacientů s nadprodukcí ACTH jsou naše výsledky též v souladu s ostatními publikovanými pracemi. Například Chen et al dosáhli hormonální normalizace po první operaci v 70,3 % případů [12], v našem souboru byla chirurgická léčba úspěšná v 65,6 % případů. Výjimečnou úspěšnost chirurgické léčby publikovali Hoffman et al – hormonální normalizace v 75 % případů po první operaci [13]. Nelze však opomenout fakt, že všechny tyto operace provedl R. Fahlbusch, který je jedním z nezkušenejších, ne-li nejzkušenějším odborníkem v oblasti pituitární chirurgie.
Při kritickém zhodnocení chirurgických výsledků je třeba zdůraznit fakt, že pouze pacienti s dostatečným poklesem nadprodukovaného hormonu a zárověn dostatečnou funkcí adenohypofýzy představují optimální výsledky. K tomu, aby se počet pacientů řazených do této skupiny nadále zvyšoval, jsou nutné dva parametry: správná indikační kritéria a zlepšování chirurgické techniky.
Postup u hormonálně aktivních adenomů hypofýzy :
První přístup představuje konzervativní léčba, která je doménou endokrinologů, převažuje u adenomů secernujících prolaktin. Adenomy secernující PRL jsme do skupiny chirurgicky řešených hormonálně aktivních tumorů primárně nezařazovali. Indikací k léčbě těchto tumorů ve většině případů není hormonální aktivita. Operují se pouze v případě selhání endokrinní terapie (po cca 3 týdnech léčby) a ohrožení např. zraku.
Druhý chirurgický přístupje indikován vždy, když konzervativní terapie u hormonálně aktivních tumorů selhává, nebo když jsou v ohrožení nervové struktury v blízkosti tumoru. U chirurgického postupu je vždy zásadou maximální radikalita při minimálních morbiditě. Přednost dáváme transsfenoidálnímu přístupu.
Třetí postup představuje radiochirurgie – významná doplňková metoda u recidivujících, nebo reziduálních adenomů hypofýzy. Význam operací u hormonálně aktivních tumorů je v rychlém poklesu hormonálních hladin. Při léčbě na LGN je pokles pomalý a postupný. Velkým přínosem je však zejména v případě hormonálně aktivních reziduí adenomů hypofýzy, převážně v kavernózním splavu.
Problematika gigantických hormonálně aktivních adenomů hypofýzy přesahuje rámec tohoto textu, proto zde uvádíme pouze základní rozvahu stran chirurgického postupu u těchto pacientů. Pokud významná složka gigantického adenomu roste supraselárně, poté zvažujeme transsfenoidální resekci jako první operaci i s vědomím toho, že nelze očekávat radikální resekci. Cílem je zejména snížení tlaku na chiazma, případně hypotalamus. Dle pooperačního MRI zvažujeme transkraniální resekci v druhé době, nebo dozáření rezidua adenomu na LGN. Pokud roste hlavní část adenomu paraselárně, poté indikujeme transkraniální resekci jako primární výkon.
U adenomů hypofýzy je nezbytná spolupráce více pracovišť. Společná indikace a rozdělení priorit je základem efektivnosti léčby. V našem případě toto představuje spolupráce III. interní kliniky 1. LF UK a VFN Praha, oddělení stereotaktické a radiační neurochirurgie, nemocnice Na Homolce a naší kliniky.
Je sporné, zda budoucnost chirurgických přístupů spočívá v tzv. „minimálně invazivní chirurgii“. Například neadekvátní použití endoskopických technik může naopak vést ke zmenšení operačního prostoru, snížení možnosti radikality u makroadenomů a zvýšení operačních rizik. Naprosto nezbytná je úvaha nad výhodami jednotlivých operačních technik [14]. Kosmetický výsledek je téměř stejný, doba hojení je obdobná, dvou až třídenní nosní tamponáda u pacientů po sublabiálním přístupu neznamená velkou zátěž pro nemocného. Na neurochirurgické klinice 1.LF UK IPVZ a ÚVN Praha se každý rok operuje 60 adenomů hypofýzy ročně. Pokud operace provádějí 2 neurochirurgové, pak každý provádí 30 operací ročně, což považujeme za minimum k udržení chirurgických dovedností a jejich dalšímu rozvoji. Zde je nutné zdůraznit fakt, že na našem pracovišti se provádí nejvíce operací pro selární léze v ČR.
Transsfenoidální přístup je velmi šetrný, nedovoluje však pohled za roh a nedovoluje žádné perioperační násilí – naslepo vedené kyrety nesmí vyvíjet žádný tlak na struktury, ať již ve splavu nebo v supraselární krajině. Jakékoli násilí může mít za následek poranění okohybných nervů, karotidy, chiazmatu, nebo dokonce hypotalamu. Komplikacím se nelze zcela vyhnout, ale jejich frekvence nesmí překročit literaturou udávaná 2 %.
V posledních letech bylo publikováno mnoho studí, které preferují endoskopické resekce adenomů hypofýzy [15-18], včetně hormonálně aktivních [19]. Někteří autoři dokonce doporučují endoskopické operace i v případech recidivujících, či reziduálních adenomů hypofýzy [20]. Endoskopické resekce provádíme na našem pracovišti od poloviny roku 2004, přesto je prozatím neindikujeme u sekundárních operací. V těchto případech je orientace během výkonu obtížnější, proto vzhledem k doposud menší zkušenosti s endoskopickými výkony v těchto případech preferujeme klasický přístup přímý endonazální, nebo sublabiální. Jsme přesvědčeni, že zlepšení operačních výsledků přináší použití bezrámové navigace, která usnadňuje orientaci v operačním poli.
Za perspektivní považujeme použití intraoperační MRI. Schwartz et al použili peroperační MRI o síle pole 0,12 Tesla v 15 případech. Ve 3 případech (20 %) bylo na peroperační MRI nalezeno reziduum adenomu, které bylo v druhé části operace odstraněno [21]. Největšími zkušenostmi s intraoperační MRI o síle 1,5 Tesla disponuje skupina neurochirurgů z Erlangen, Německo. Tyto operace opět prováděl R. Fahlbusch. U 18 pacientů s nadprodukcí STH byla plánována radikální resekce s cílem hormonální hormalizace. Ve 3 případech (16,6 %) intraoperační MRI odhalila resekabilní reziduum adenomu hypofýzy a u 2 z těchto 3 pacientů bylo resekcí rezidua adenomu dosaženo hormonální normalizace [22]. I když se jedná o výsledky z doposud malé studie, považujeme tyto výsledky za významné – zlepšení výsledků o 11,1 % díky intraoperační MRI, i přesto že operace prováděl extrémně zkušený pituitární neurochirurg. Intraoperační MRI odhalí rezidua adenomů hypofýzy, umožní během stejné operace resekci adenomu provést radikálněji, avšak bez zvýšení operačních rizik.
Závěr
Chirurgická léčba dosahuje normalizace nadprodukce hormonů u přibližně 60 % pacientů s hormonálně aktivními adenomy hypofýzy. V ostatních případech je nutná vhodná kombinace chirurgické léčby s medikamentózní léčbou a správně načasovaným ozářením na LGN. Chirurgická léčba včetně operačního přístupu by měla být rutinní a zejména dostatečně bezpečná. Cílem není samotná miniinvazivita chirurgického výkonu, cílem je bezpečnost chirurgického výkonu, samozřejmě za předpokladu udržení dostečného komfortu pacienta, který tuto operaci podstupuje. Bezrámová navigace a použití endoskopu jsou užitečnými doplňky při transsfenoidálních operacích. Další zlepšení chirurgických výsledků lze očekávat od použití intraoperační MRI, která zřejmě umožní zvýšit radikalitu chirurgických výkonů bez zvýšení rizik spojených s operací.
Přijato k recenzi: 13.7.2006
Přijato do tisku: 5.2.2007
Korespondující autor:
MUDr. Václav Masopust
Neurochirurgická klinika 1. LF UK, IPVZ a ÚVN
Ústřední vojenská nemocnice
U vojenské nemocnice 1200
169 02, Praha 6
e-mail: vaclav.masopust@uvn.cz
Zdroje
1. Rosegay H. Cushing’s legacy to transsphenoidal surgery. J Neurosurg 1981; 54: 448-454.
2. Walker EA. A History of Neurological Surgery. Baltimore: Williams a Wilkins 1982.
3. Hardy J. Transsphenoidal hypophysectomy: neurosurgical techniques. J Neurosurg 1971; 34: 582-584.
4. Fusek I, Černý E. Transsphenoidal operation of hypophyseal tumors. J Neurosur Sci 1977; 21: 159-160.
5. Fusek I, Černý E. Naše zkušenosti s indikacemi transsfenoidálních operací nádorů tureckého sedla. Česk Slov Neurol N 1978; 41/74: 107-114.
6. Fusek I. Chirurgické léčení nádorů tureckého sedla transsfenoidálním přístupem. Praha: Avicenum 1986.
7. Náhlovský J, Česák T, Látr I, Čáp J, Žižka J, Krajina A. Komplikace transsfenoidálních operací u našich nemocných – příčiny a řešení. Česk Slov Neurol N 2004; 67/100: 112–119.
8. Nomikos P, Buchfelder M, Fahlbusch R. Current management of prolactinomas. J Neurooncol 2001; 54(2): 139-150.
9. Kristof RA, Schramm J, Redel L, Neuloh G, Wichers M, Klingmuller D. Endocrinological outcome following first time transsphenoidal surgery for GH-, ACTH-, and PRL-secreting pituitary adenomas. Acta Neurochir 2002; 144(6): 555-561.
10. Nomikos P, Buchfelder M, Fahlbusch R. The outcome of surgery in 668 patients with acromegaly using current criteria of biochemical 'cure'. Eur J Endocrinol 2005; 152(3): 379-387.
11. Erturk E, Tuncel E, Kiyici S, Ersoy C, Duran C, Imamoglu S. Outcome of surgery for acromegaly performed by different surgeons: importance of surgical experience. Pituitary 2005; 8(2): 93-7.
12. Chen JC, Amar AP, Choi S, Singer P, Couldwell WT, Weiss MH. Transsphenoidal microsurgical treatment of Cushing disease: postoperative assessment of surgical efficacy by application of an overnight low-dose dexamethasone suppression test. J Neurosurg 2003; 98(5): 967-973.
13. Hofmann BM, Fahlbusch R. Treatment of Cushing's disease: a retrospective clinical study of the latest 100 cases. Front Horm Res 2006; 34: 158-184.
14. Bláha M, Netuka D, Mohapl M, Masopust V, Plas J, Beneš V. Operační přístupy do sfenoidální dutiny při mikrochirurgických operacích nádorů hypofýzy. Rozhl Chir 2003; 82/9: 452-455.
15. Cappabianca P, Cavallo LM, de Divitiis E. Endoscopic endonasal transsphenoidal surgery. Neurosurgery 2004; 55(4): 933-940.
16. Jane JA Jr, Han J, Prevedello DM, Jagannathan J, Dumont AS, Laws ER Jr.
Perspectives on endoscopic transsphenoidal surgery. Neurosurg Focus 2005; 19(6): E2.
17. Har-El G. Endoscopic transnasal transsphenoidal pituitary surgery--comparison with the traditional sublabial transseptal approach. Otolaryngol Clin North Am 2005; 38(4): 723-735.
18. Kabil MS, Eby JB, Shahinian HK. Fully endoscopic endonasal vs. transseptal transsphenoidal pituitary surgery. Minim Invasive Neurosurg 2005; 48(6): 348-354.
19. Netea-Maier RT, van Lindert EJ, den Heijer M, van der Eerden A, Pieters GF, Sweep CG et al. Transsphenoidal pituitary surgery via the endoscopic technique: results in 35 consecutive patients with Cushing's disease. Eur J Endocrinol 2006; 154(5): 675-684.
20. Rudnik A, Zawadzki T, Galuszka-Ignasiak B, Bazowski P, Duda I, Wojtacha M et al. Endoscopic transsphenoidal treatment in recurrent and residual pituitary adenomas - first experience. Minim Invasive Neurosurg 2006; 49(1): 10-14.
21. Schwartz TH, Stieg PE, Anand VK. Endoscopic transsphenoidal pituitary surgery with intraoperative magnetic resonance imaging. Neurosurgery 2006; 58(1Suppl): ONS44-51.
22. Fahlbusch R, Keller B, Ganslandt O, Kreutzer J, Nimsky C. Transsphenoidal surgery in acromegaly investigated by intraoperative high-field magnetic resonance imaging. Eur J Endocrinol 2005; 153(2): 239-248.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2007 Číslo 4
Nejčtenější v tomto čísle
- Cervikální dystonie
- Hladina D-dimerů u pacientů s akutní ischemickou cévní mozkovu příhodou
- Trombóza esovitého splavu – současný pohled na diagnostiku a léčbu
- Repetitivní transkraniální magnetická stimulace a chronický subjektivní nonvibrační tinnitus
