Vliv chemoterapeutické léčby na kognitivní funkce dětí s leukemií
The effect of chemotherapy on cognitive functions in children with leukemia
Leukemia is one of the most common childhood diseases with a malignant course. Fortunately, today there is a high probability of its successful cure. The nature of the disease entails a high risk of initial spread, or later relapse of the disease into the central nervous system. Standard treatment including intrathecal application of cytostatics reduces this risk fundamentally; nevertheless it can damage some cognitive functions. There is extensive research dealing with this issue. Through a systematic literature research, we selected 16 articles that examined cognitive functions through neuropsychological tests. Result analysis indicates a statistically significant decrease in performance in tests of attention, processing speed, working memory and executive functions. Conversely, the overall intelligence quotient, learning ability and long-term memory seem to be only slightly affected by the treatment.
Keywords:
Chemotherapy – Intelligence – cognitive function – leukemia – pediatric hematology/oncology
Autoři:
P. Lhotová 1; L. Šrámková 2; P. Smíšek 2; T. Nikolai 1
Působiště autorů:
Neuropsychologická laboratoř, Neurologická klinika a Centrum klinických neurověd, 1. LF UK a VFN v Praze
1; Klinika dětské hematologie a onkologie 2. LF UK a FN Motol, Praha
2
Vyšlo v časopise:
Cesk Slov Neurol N 2023; 86(6): 369-374
Kategorie:
Přehledný referát
doi:
https://doi.org/10.48095/cccsnn2023369
Souhrn
Leukemie jsou jedny z nejčastějších dětských onemocnění s maligním průběhem. Dnes naštěstí mají vysokou pravděpodobnost úspěšného vyléčení. Charakter onemocnění s sebou nese vysoké riziko iniciálního rozšíření, respektive pozdějšího relapsu onemocnění do CNS. Standardní léčba proto zahrnuje i intratekální aplikaci cytostatik, která toto riziko zásadně snižují, avšak mohou poškodit některé kognitivní funkce. Výzkum zabývající se touto problematikou je široký. Systematickou literární rešerší jsme vybrali 16 článků, které kognitivní funkce zkoumaly prostřednictvím neuropsychologických testů. Analýza výsledků svědčí o statisticky významném poklesu výkonu v testech pozornosti, rychlosti zpracování, pracovní paměti a exekutivních funkcí. Naopak celkový inteligenční kvocient, schopnost učení a dlouhodobá paměť se zdají být léčbou zasaženy jen mírně.
Klíčová slova:
kognitivní funkce – leukemie – chemoterapie – dětská hematologie/onkologie – inteligence
Úvod
Nádorová onemocnění jsou po nehodách druhou nejčastější příčinou úmrtí dětí a adolescentů ve vyspělých zemích [1]. Ročně je onemocněním z této skupiny celosvětově diagnostikováno asi 400 000 dětí [2]. Nádorová onemocnění u dětí a dospělých si jsou podobná ve své podstatě, tj. v nekontrolovatelném růstu a proliferaci abnormálních buněk. Bez léčby jsou neslučitelná se životem. Vlivem odlišné dynamiky jsou dětská nádorová onemocnění citlivější na chemoterapii, než je tomu u nádorů dospělých [2], chemoterapie je proto hlavní léčebnou metodou. Úspěšnost léčby, měřena jako 5 a více let dožití od diagnózy, v posledních několika dekádách roste a překračuje 80 % [3]. S rostoucí úspěšností roste i potřeba sledovat nežádoucí účinky léčby, které se mohou manifestovat na úrovni somatické i neuropsychické.
Nejčastějšími nádorovými onemocněními dětí do 14 let jsou leukemie, jejichž podíl je 30 %, ve věkové skupině do 4 let až 36 % [4]. S věkem incidence leukemií klesá, u adolescentů mezi 15 a 19 lety se pohybuje kolem 15 %, častěji se u nich setkáme s lymfomy a epitelovými nádory [5].
Leukemie je souhrnný název skupiny onemocnění, jejichž společnou charakteristikou je maligní transformace hematopoetických buněk. Dle typu malignitou zasažených buněk rozeznáváme akutní lymfoblastickou leukemii (ALL), akutní myeloblastickou leukemii (AML) a chronickou myeloidní leukemii (CML). Pro děti je nejtypičtější ALL, čítající asi 80 % případů [4,6].
Leukemie je chemosenzitivní nemoc. Léčba trvá přibližně 2 roky a kombinace cytostatik a intenzita léčby se odvíjejí od odpovědi na léčbu v první, tzv. indukční fázi [7]. Z neurologického pohledu se nejvyšší riziko vzniku nežádoucích účinků pojí s vinkristinem, který může způsobovat polyneuropatii [8,9]. Souběžným vlivem glukokortikoidů a leukemie samotné pak může dojít k osteoporóze (a kompresivním fakturám obratlů ovlivňujícím míšní nervy) [10,11].
Leukemické buňky mají schopnost projít přes hematoencefalickou bariéru, infiltrovat se do CNS a zachytit se v mozkových plenách. Zde mohou díky své adaptabilitě dlouho přežívat, ev. začít proliferovat [12]. Cytostatika penetrují hematoencefalickou bariéru pouze v nízkém rozsahu [13], a tudíž nemusí leukemické buňky zasáhnout. Přeživší leukemické buňky později dokáží způsobit relaps onemocnění [14]. Bez systémové profylaxe, která je již běžnou součástí léčby, docházelo k CNS relapsu u 30–50 % dětí [4,14].
Původní metodou CNS profylaxe byla radioterapie krania, která sice zvýšila podíl vyléčených až k současným 80–90 % [15], nicméně ozařování způsobovalo pokles některých kognitivních funkcí, nekontrolovatelné epileptické záchvaty, mozková krvácení, endokrinopatie či sekundární tumory CNS [16,17]. Radioterapii proto u většiny dětí nahradila intratekální aplikace metotrexátu, která přináší srovnatelné výsledky ohledně relapsů v CNS při současně nižší neurotoxicitě [17]. Radioterapie dnes zůstává součástí léčebných protokolů dětí s nejvyšším rizikem, tj. asi u 15 % všech dětí s leukemií [7]. Děti s nedostatečnou odpovědí na léčbu v indukční fázi a pravděpodobností vyléčení menší než 50 % jsou indikovány k transplantaci kostní dřeně [18].
Bohužel i šetrnější chemoterapeutická profylaxe s sebou nese riziko poškození CNS. Výzkumy potvrzují souvislost mezi intratekální aplikací cytostatik a leukoencefalopatií [19,20]. Intratekálně podávaný metotrexát může způsobit bezprostřední toxicitu a vést tak k narušení šedé hmoty mozkové a/nebo demyelinizovat vlákna bílé hmoty [21,22]. Takto vznikající leukoencefalopatie může probíhat jako akutní („stroke-like“ symptomy, epiparoxyzmy, afázie), ale i bezpříznakově. Další riziko přináší sekundární imunologická odpověď na metotrexát vyvolávající zánětlivou reakci, jejímž působením může dojít k mikrovaskulárnímu poranění. Leukoencefalopatie i vaskulární poranění mohou vést k poklesu mentálního výkonu. Zasaženy jsou zejména schopnosti kritické pro úspěšnost ve škole [23], např. pozornost a osvojování si nových znalostí (kapacita učení), vizuálně prostorové schopnosti a další [24]. Obtíže ve zvládání školní látky mohou následně způsobit zvětšení již existujícího rozdílu mezi dětmi s leukemií a zdravými vrstevníky [25].
Kognitivní funkce dětí s leukemií byly sledovány mnoha různými autory. V našem článku se chceme pokusit shrnout výsledky studií posledních 10 let, zaměřit se na inteligenční úroveň a nejčastěji sledované kognitivní funkce a porovnat výsledky jednotlivých autorů, resp. vědeckých skupin. Literární rešerši jsme vypracovali v reakci na opakující se obtíže dětí zvládat studijní nároky při návratu do běžného školního režimu po léčbě leukemie. Výsledky rešerše mohou sloužit jako podklad pro dlouhodobé sledování kognitivního výkonu dětí s leukemií a následné sestavení vhodných pedagogicko-psychologických podpůrných opatření.
Metodologie
Pro přehledný referát jsme vyhledali všechny anglicky psané publikace vztahující se k tématu kognitivních funkcí a inteligenční úrovně u dětí s leukemií publikované v období od ledna 2011 do prosince 2021. Publikace byly vyhledávány v elektronické databázi PubMed na základě kombinace klíčových slov a výrazů: (leukemia or ALL) AND (child*) AND (neurocognit* or neuropsych* or cognit*). Rešerši jsme dále doplnili články z databáze Google Scholar, kde jsme použili stejná klíčová slova a časové omezení. Třetím zdrojem byly reference, na které odkazovaly relevantní články nalezené a studované v rámci rešerše.
První rešerší v databázi PubMed jsme získali 439 článků, z nichž bylo 114 vybráno na základě názvu. V dalším kroku jsme dle abstraktu, případně na základě čtení článku, vybrali příspěvky, které splňovaly níže uvedená kritéria:
a) diagnóza leukemie v dětském věku;
b) léčba vedená čistě chemoterapeuticky, s intratekální aplikací cytostatik;
c) vyšetření kognitivních funkcí bylo provedeno výkonovými testy;
d) uvedení dosažených hodnot neuropsychologických testů a odchylek, resp. statistické významnosti ve srovnání s kontrolní skupinou;
e) minimální počet 20 dětí ve výzkumném souboru.
Články získané dalšími metodami se dublovaly, případně nesplňovaly některé z kritérií výběru.
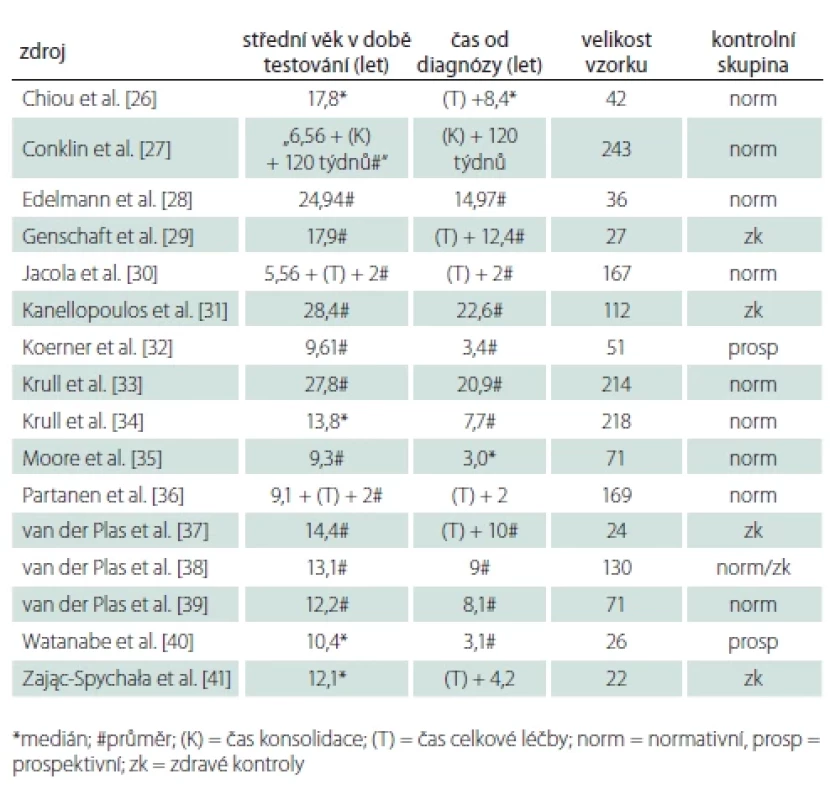
Stanoveným kritériím odpovídalo 16 studií (tab. 1) [26–41]. Velikost zkoumaných skupin se pohybovala v rozmezí 22–243, s mediánem 71 pacientů. Výsledky byly v devíti studiích srovnávány s populačními normami, ve čtyřech studiích se zdravými, demograficky párovanými kontrolami. Jedna studie [38] srovnávala výsledky inteligenčních testů se zdravými kontrolami, dílčí testy kognitivních funkcí s populačními normami. Konečně dvě skupiny byly sestaveny prospektivně, tj. sledovaly změnu výkonu dětí s leukemií v čase.
Studie, které jsme získali literární rešerší, vycházely z různých předpokladů a klinických studií. Jejich výběr sledovaných kognitivních funkcí se tudíž lišil. V článku se zabýváme inteligenční úrovní a kognitivními funkcemi, které představují průsečík studií, tj. nejčastěji sledované kognitivní funkce jsme operacionalizovali následovně: celkový inteligenční kvocient (CIQ), schopnost učení a paměť, pozornost, rychlost zpracování, pracovní paměť a exekutivní funkce. Jsme si vědomi, že definice výše uvedených kognitivních funkcí se mohou lišit, a to zejména u exekutivních funkcí a pracovní paměti. V článku užíváme pojem exekutivní funkce v souladu s výkladem Lezaka et al. [42] jako soubor vzájemně interagujících schopností nezbytných pro plánování záměrného chování a realizace dílčích kroků k dosažení chtěného cíle. Pracovní paměť pak jako schopnost dočasného udržení informací v paměti za účelem jejich použití pro komplexnější mentální operace.

prolekare.web.text.media.image_type_.cs
Výsledky
Statistická významnost
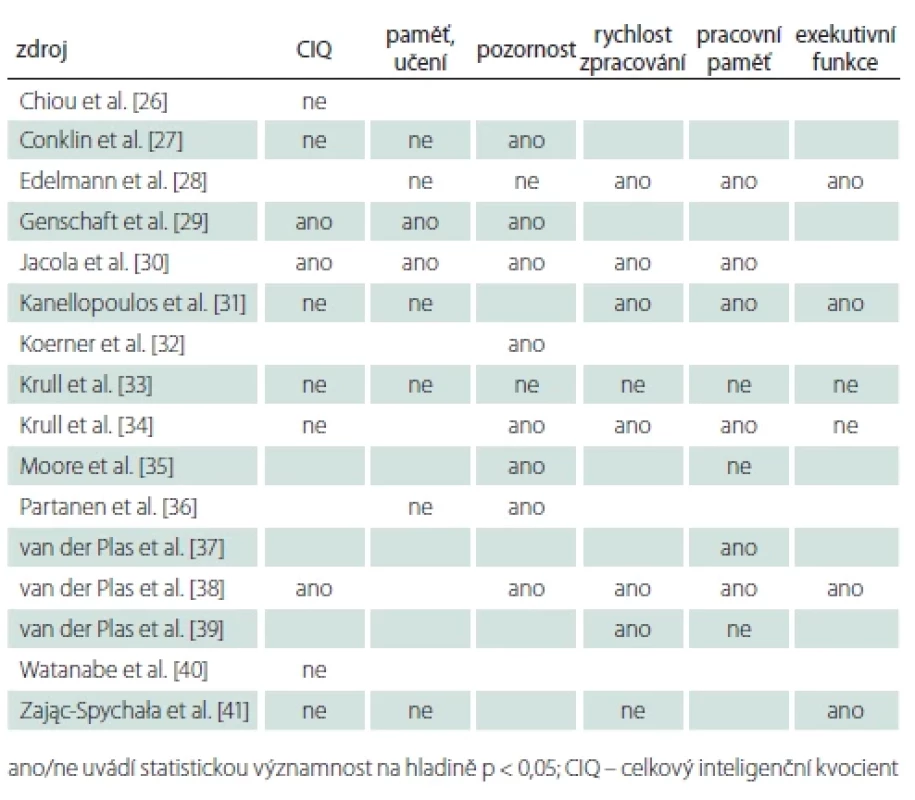
Statistickou významnost, tj. předpoklad poškození kognitivních funkcí CNS profylaxí, uvádíme na hladině významnosti p < 0,05 a adekvátních hodnot, tedy s 95% pravděpodobností. Přehled výsledků, tj. jejich statistické významnosti vzhledem ke kritériím výše je uveden v tab. 2 [26–41]. Statisticky významné poškození některé ze sledovaných kognitivních funkcí uvádělo 14 ze 16 studií. Ve výsledcích dáváme stejnou váhu všem studiím, případný nežádoucí efekt extrémních hodnot jsme kontrolovali součtem všech testovaných dětí z cílové skupiny a kontrolou poměrů i v této veličině. Počet testovaných se pohyboval od 732 u exekutivních funkcí až po 1 326 u pozornosti. Procentuální podíl výsledků svědčících pro poškození je srovnatelný, sledujeme-li poměr studií a poměr počtu dětí zahrnutých v těchto studiích (obr. 1). Výsledky se odlišují pouze u exekutivních funkcí, kde pro poškození svědčí 67 % studií. Sečteme-li však všechny děti zahrnuté ve sledovaných studiích, poškození se ukazuje pouze u 41 % z nich. Rozdíl může být způsoben metodologicky (viz dále).
Sledovaná skupina
Všichni testovaní onemocněli v dětském věku leukemií a byli léčeni pouze chemoterapií. Součástí léčby byl ve všech případech i intratekálně podávaný metotrexát. Dávky metotrexátu byly určovány dle aktuálně platných mezinárodních léčebných protokolů, ev. upraveny dle klinického stavu a snášenlivosti léčby jednotlivými dětmi. Průměrné množství nebo počet dávek uvádí pouze několik studií [28,31,33,34], hodnoty jsou velmi podobné a pohybují se kolem 170 g/mm2.
Čas testování od diagnózy, věk probandů
Čas testování dětí od diagnózy leukemie byl heterogenní a pohyboval se od 2 či 3 let [27,32,35,40] až do více než 20 let [31,33]. Studie realizované do 5 let od diagnózy uváděly častěji signifikantní snížení výkonu v dílčích doménách (10 ze 14 sledovaných domén, pozn. dále v článku užíváme slovo doména jako nadřazený pojem pro CIQ a popisované dílčí kognitivní funkce), a to i přes to, že výsledky byly ve většině případů srovnávány s normativními daty (viz dále). Studie realizované s více než 5letým odstupem od diagnózy reportovaly poškození přibližně v polovině případů (22 ze 41 sledovaných domén), přičemž více než polovina z nich srovnávala výsledky se zdravými kontrolami. Medián věku dětí v době testování byl 13,1 let a střední věk uváděný v jednotlivých studiích se pohyboval od 9 [27,32,35] do 28 let [31,33]. Protože studie uvádějí pouze střední věky dětí, nebyla možná detailnější analýza vlivu věku při diagnóze onemocnění na výsledky. Průměrný věk dětí v době stanovení diagnózy byl orientačně v rozmezí od 2,4 do 9,9 let s mediánem přibližně 6 let.
Kontrolní skupina
Výkony byly nejčastěji porovnávány s normativními daty (9 ze 16 studií). Čtyři studie porovnávaly výkon se zdravými, demograficky párovanými vrstevníky a pouze dvě studie srovnávaly výsledky prospektivně [32,40]. Jedna studie [38] porovnávala výsledky inteligenčních testů se zdravými kontrolami, dílčí kognitivní funkce pak s normativními daty. Studie srovnávající výsledky s normativními daty a zdravými kontrolami sledovaly podobné množství domén, v průměru 3,9, resp. 3,6 domén. Celkové výsledky byly při srovnávání s normativními daty pozitivnější a uváděly poškození „pouze“ ve 49 % případů. Při srovnání výsledků se zdravými kontrolami bylo poškození uváděno u 72 % případů. Prospektivní studie jsou zastoupeny minimálně – dvě studie, každá sledující jednu doménu. Bez ohledu na statistickou významnost a kontrolní skupinu všichni autoři uváděli u sledovaných kognitivních funkcí nižší výkon dětí po prodělané léčbě leukemie. Pouze Watanabe et al. [40] sledovali mírné zvýšení výkonu v CIQ.
Domény
Cekový IQ byl sledován v deseti studiích, přičemž sedm z nich nenašlo statisticky významnou změnu výkonu u dětí s leukemií. Pouze studie autorů Watanabe et al. [40] uváděla i další rozklad výsledků CIQ. Ten ukazoval na slabší výkon ve verbálních než v performačních subtestech, což korespondovalo se staršími studiemi [43,44].
Schopnost učení a paměť
Schopností zapamatovat si informace, udržet a s odstupem vybavit se zabývalo osm studií. Dvě uvádějí statisticky významný pokles výkonu u dětí po chemoterapeutické léčbě leukemie [29,30] – Genschaft et al. [29] ve verbální i neverbální paměti, Jacola et al. [30] zejména v kapacitě učení. Výsledky zbývajících studií svědčily pouze o mírném poškození jak u krátkodobé, tak u dlouhodobé paměti. Výsledky jsou srovnatelné u různých kontrolních skupin i v různém čase od diagnózy.
Pozornost
Do této kategorie byly zařazeny studie, které měřily pozornost některým z neuropsychologických testů pozornosti nebo sledovaly počty chyb z přehlédnutí v rámci komplexních testových baterií. Osm z deseti studií, které testy pozornosti zařadily do výzkumu, uvádělo statisticky významný pokles. Zbývající dvě studie [28,33] byly administrovány v nejdelším čase od diagnózy, tj. téměř 21 a 15 let. Střední doba mezi diagnózou a administrací testů se u zbývajících studií pohybovala mezi 2 [27] a 9 lety [38].
Rychlost zpracování
Rychlost zpracování byla ve studiích měřena různými testy. Z analýzy jsme vyloučili testy čistě motorické, jejichž výsledek může být ovlivněn i dalšími vedlejšími účinky léčby, zejména neuropatií. Pro úplnost můžeme uvést, že v případě motorických testů tři ze čtyř studií uváděly statisticky významné snížení výkonu. V článku uváděná skupina testů zahrnuje testy verbální, vizuální a vizuomotorické, přičemž většina studií měřila rychlost zpracování kombinací více psychodiagnostických metod. Výsledky různých subtestů ve smyslu statisticky významného či nevýznamného snížení výkonu se většinou v rámci téže studie shodovaly, ev. z několika psychodiagnostických testů vyšel pouze jeden jako nesignifikantní jako např. u autorů Zając-Spychała et al. [41]. Šest z osmi studií uvádělo signifikantní pokles výkonu v rychlosti zpracování.
Pracovní paměť
Pracovní paměť, schopnost dočasně si v paměti udržet informace a pracovat s nimi, je řazena společně s kontrolou inhibice a kognitivní flexibilitou mezi exekutivní funkce [45]. Z důvodu jejich přímého vztahu vůči akademické úspěšnosti [46] často bývá testována samostatně. Z 16 studií se na pracovní paměť zaměřilo devět, přičemž čtyři z nich hodnotily pouze výkon v pracovní paměti, nikoliv už exekutivní funkce. Signifikantně nižší výkon uvádělo šest studií z devíti. Všechny tři studie nesvědčící pro významnější snížení výkonu porovnávaly výsledky s normativními daty, ostatní rovnoměrně se zdravými kontrolami a normativními daty.
Exekutivní funkce
Exekutivní funkce hodnotilo šest studií, pět z nich zároveň i pracovní paměť. Výsledky byly většinou souhlasné, tedy v rámci studie byl nebo nebyl snížen výkon pracovní paměti i exekutivních funkcí. Statisticky významné snížení výkonu uváděly čtyři ze šesti studií. Všechny studie byly realizovány v období delším než pět let od diagnózy.
Diskuze
Předmětem našeho výzkumu bylo sledování možného vlivu čistě chemoterapeutické léčby leukemie v dětském věku na kognitivní funkce. V první části našeho review jsme systematickou literární rešerší vybrali 16 článků, které inteligenci a kognitivní funkce zkoumaly prostřednictvím výkonových neuropsychologických testů. Do review jsme následně zařadili ty domény, které byly sledovány nejméně šesti různými výzkumy. Pro účely našeho review jsme publikované výsledky rozdělili do dvou pásem, tj. svědčících vs. nesvědčících pro pokles výkonu, a to dle kvantitativních výsledků na hladině 95% spolehlivosti. Závěry z analýzy ukazují, že intratekální aplikace cytostatik při léčbě leukemie má významný negativní vliv na pozornost, rychlost zpracování, pracovní paměť a exekutivní funkce. Nižší výkon byl zaznamenán i u CIQ a paměti a schopnosti učení, pokles však nebyl statisticky významný.
Poškození pouze některých funkcí může být dáno jejich lokalizací. Funkce, u nichž bylo sledováno snížení výkonu, jsou asociovány s činností frontálního laloku, kdežto struktury zásadní pro paměť a učení jsou lokalizovány především v parietálním a temporálním laloku a hipokampu. Tato úvaha koresponduje i se zjištěním Krulla et al [34], kteří při vyšetření funkční MR dětí z námi sledované skupiny popisují strukturální změny ve frontálním laloku a intaktní parietální a okcipitální lalok. V souladu s výše uvedeným se nabízí hypotéza, že fluidní složky inteligence (tzv. fluidní „ g“), které zahrnují i některé aspekty pracovní paměti a exekutivních funkcí, mohou sice být léčbou leukemie postižené, nicméně protože je CIQ silně syceno i krystalickými schopnostmi (tzv. krystalické „ g“), které jsou naštěstí poškozeny méně, nedosahují rozdíly CIQ mezi zdravými a léčenými dětmi statisticky významných hodnot. Podobně jako CIQ jsou sestaveny i testy exekutivních funkcí, tj. výsledek vychází z výkonu ve více kognitivních doménách. Tyto jsou však závislé především na integritě prefrontálního kortexu.
Další proměnnou ve výzkumu je velký rozptyl v čase, který uběhl mezi vyšetřeními a diagnózou, resp. léčbou. Do 5 let od diagnózy proběhlo šest ze 16 námi analyzovaných studií. Autoři ve svých článcích důvody neuváděli. Vliv na výběr času studie by mohla mít distribuce onemocnění v jednotlivých věkových skupinách. Nejvyšší incidence leukemie je u dětí mezi 2 a 6 lety, kdy jsou vyšetření dílčích kognitivních funkcí obtížně realizovatelná z důvodu nezralosti CNS a vysokého rozptylu výsledků i v normální populaci. Vyřazení mladších dětí by tak mohlo významně zmenšit výzkumný vzorek. Úvahu by podporoval i profil sledovaných funkcí, kdy většina časně realizovaných výzkumů se zaměřuje na komplexnější schopnosti (CIQ, paměť a učení), které u mladších dětí zhodnotíme poměrně spolehlivě.
I přes výše uvedené pokládáme srovnání výzkumů realizovaných do a nad 5 let od diagnózy jako velmi zajímavé. U analyzovaných studií bylo patrné, že výsledky studie realizované s větším odstupem vycházejí pozitivněji, a to u všech sledovaných domén. Podobně mírně pozitivní trend uvádějí u CIQ ve své studii i Watanabe et al. [40], kteří ve své prospektivní studii testovali děti ve třech časových bodech. Zlepšení může nastávat díky zrání mozku, pozitivnímu vlivu plasticity mozku, ale také díky kognitivnímu tréninku.
Další proměnnou, která může ovlivňovat zde uvedené výsledky, je kontrolní skupina. Výsledky srovnávající výkon dětí s normativním vzorkem mohou být mírně nadhodnocené. Důvodem mohou být možnost lépe kontrolovat zdravotní stav a kognitivní výkon dětí, zdravých i vyléčených, vstupujících do výzkumu, vyšší ochota vzdělanějších rodičů participovat ve výzkumu a konečně i lepší porozumění důvodům testování, a tedy vyšší motivace dětí po leukemii.
Získané výsledky mohou být ovlivněny několika proměnnými, které jsme pro účely našeho přehledu nemohli kontrolovat. Kromě typu kontrolní skupiny, kterou jsme zmiňovali výše, považujeme za klíčové níže uvedené body.
1)
Studie sledující jednotlivé kognitivní funkce pracovaly s rozdílnou testovou baterií. Jednotlivé metody užité ve studiích se liší svou náročností, ev. také tím, na který aspekt kognitivní funkce se zaměřují.
2)
Jak je naznačeno v úvodu, léčba leukemie u dětí se liší ve frekvenci a dávce cytostatik. V souladu s dostupnými zdroji lze předpokládat, že s vyšší dávkou intratekálně podávaných cytostatik roste riziko i míra poškození kognitivních funkcí [27,47]. Bohužel ze zde zahrnutých studií nelze hodnotit interindividuální rozdíly ve výkonech v závislosti na intenzitě léčby.
3)
Vliv může mít i věk, ve kterém léčba probíhá. Závislostí míry poškození kognitivních funkcí na věku se zabývá více výzkumů, typicky ale rozdělují děti do a nad pět let věku v době stanovení diagnózy. Ukazuje se, že velmi malé děti jsou více náchylné k poškození kognitivních funkcí [30,48]. Otázkou zůstává efekt léčby leukemií na starší děti, neboť v adolescenci probíhá intenzivní vývoj vyšších korových funkcí, a lze tak očekávat jejich vyšší zranitelnost [49].
Závěr
Chemoterapeutická léčba leukemie vč. intratekální aplikace cytostatik kromě jednoznačných zdravotních benefitů přináší i riziko vedlejších účinků ve formě snížení výkonu některých kognitivních funkcí. Jako vysoce vulnerabilní se zdají především kognitivní funkce s centry ve frontálním laloku mozku – pozornost, rychlost zpracování informací, pracovní paměť a exekutivní funkce. Méně pak CIQ a paměť a učení. Pokles výkonu ve výše uvedených schopnostech může mít významný negativní dopad na školní prospěch i běžný život dětí po léčbě leukemie, a proto je vhodné jej pravidelně monitorovat a v případě potřeby časně rehabilitovat a kompenzovat.
Poděkování
Děkuji doc. Mgr. Ondřejovi Bezdíčkovi, Ph.D. za pomoc a cenné rady při přípravě článku.
Grantová podpora
Podpořeno Grantovou agenturou Univerzity Karlovy (GAUK 260121).
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem práce nemají žádný konflikt zájmů.
Zdroje
1. Ssenyonga N, Stiller C, Nakata K et al. Worldwide trends in population-based survival for children, adolescents, and young adults diagnosed with leukaemia, by subtype, during 2000–14 (CONCORD-3): analysis of individual data from 258 cancer registries in 61 countries. Lancet Child Adolesc Health 2022; 6 (6): 409–431. doi: 10.1016/S2352-4642 (22) 00095-5.
2. World Health Organization. CureAll framework: WHO global initiative for childhood cancer: increasing access, advancing quality, saving lives. [online]. Dostupné z: https: //www.medscape.co.uk/viewarticle/who-childhood-cancer-2023a1000it6.
3. Pritchard-Jones K, Pieters R, Reaman GH et al. Sustaining innovation and improvement in the treatment of childhood cancer: lessons from high-income countries. Lancet Oncol 2013; 14 (3): e95–e103. doi: 10.1016/S1470-2045 (13) 70010-X.
4. Kaplan JA. Leukemia in children. Pediatr Rev 2019; 40 (7): 319–331. doi: 10.1542/pir.2018-0192.
5. Steliarova-Foucher E, Fidler MM, Colombet M et al. Changing geographical patterns and trends in cancer incidence in children and adolescents in Europe, 1991–2010 (Automated Childhood Cancer Information System): a population-based study. Lancet Oncol 2018; 19 (9): 1159–1169. doi: 10.1016/S1470-2045 (18) 30423-6.
6. Heidari N, Saki N, De Filippis L et al. Central nervous system niche involvement in the leukemia. Clin Transl Oncol 2016; 18 (3): 240–250. doi: 10.1007/s12094-015-1370-3.
7. Starý J. Akutní leukemie u dětí. Solen 2010; 4 (2): 120–124.
8. Jain P, Gulati S, Seth R et al. Vincristine-induced neuropathy in childhood ALL (acute lymphoblastic leukemia) survivors: prevalence and electrophysiological characteristics. J Child Neurol 2014; 29 (7): 932–937. doi: 10.1177/0883073813491829.
9. Kroczka S, Stepien K, Witek-Motyl I et al. Polyneuropathy in acute lymphoblastic leukemia long-term survivors: clinical and electrophysiological characteristics with the impact of radiotherapy. Front Pediatr 2021; 8: 526235. doi: 10.3389/fped.2020.526235.
10. Ahn MB, Suh B-K. Bone morbidity in pediatric acute lymphoblastic leukemia. Ann Pediatr Endocrinol Metab 2020; 25 (1): 1–9. doi: 10.6065/apem.2020. 25.1.1.
11. Rossi F, Tortora C, Paoletta M et al. Osteoporosis in childhood cancer survivors: physiopathology, prevention, therapy and future perspectives. Cancers 2022; 14 (18): 4349. doi: 10.3390/cancers14184349.
12. Deak D, Gorcea-Andronic N, Sas V et al. A narrative review of central nervous system involvement in acute leukemias. Ann Transl Med 2021; 9 (1): 68. doi: 10.21037/atm-20-3140.
13. Jin M-W, Xu S-M, An Q. Central nervous disease in pediatric patients during acute lymphoblastic leukemia (ALL): a review. Eur Rev Med Pharmacol Sci 2018; 22 (18): 6015–6019. doi: 10.26355/eurrev_201809_15937.
14. Lenk L, Alsadeq A, Schewe DM. Involvement of the central nervous system in acute lymphoblastic leukemia: opinions on molecular mechanisms and clinical implications based on recent data. Cancer Metastasis Rev 2020; 39 (1): 173–187. doi: 10.1007/s10555-020-09848-z.
15. Pui C-H, Evans WE. Treatment of acute lymphoblastic leukemia. N Engl J Med 2006; 354 (2): 166–178. doi: 10.1056/NEJMra052603.
16. Wilejto M, Giuseppe GD, Hitzler J et al. Treatment of young children with CNS-positive acute lymphoblastic leukemia without cranial radiotherapy. Pediatr Blood Cancer 2015; 62 (11): 1881–1885. doi: 10.1002/ pbc.25620.
17. Swaiman KF, Ashwal S, Ferriero DM et al. Swaiman’s pediatric neurology: principles and practice. Edinburgh, New York: Elsevier 2018.
18. Merli P, Algeri M, Del Bufalo F et al. Hematopoietic stem cell transplantation in pediatric acute lymphoblastic leukemia. Curr Hematol Malig Rep 2019; 14 (2): 94–105. doi: 10.1007/s11899-019-00502-2.
19. Reddick WE, Shan ZY, Glass JO et al. Smaller white-matter volumes are associated with larger deficits in attention and learning among long-term survivors of acute lymphoblastic leukemia. Cancer 2006; 106 (4): 941–949. doi: 10.1002/cncr.21679.
20. Rijmenams I, Moechars D, Uyttebroeck A et al. Age- and intravenous methotrexate-associated leukoencephalopathy and its neurological impact in pediatric patients with lymphoblastic leukemia. Cancers 2021; 13 (8): 1939. doi: 10.3390/cancers13081939.
21. Zeller B, Tamnes CK, Kanellopoulos A et al. Reduced neuroanatomic volumes in long-term survivors of childhood acute lymphoblastic leukemia. J Clin Oncol 2013; 31 (17): 2078–2085. doi: 10.1200/JCO.2012.47.4031.
22. Bhojwani D, Sabin ND, Pei D et al. Methotrexate-induced neurotoxicity and leukoencephalopathy in childhood acute lymphoblastic leukemia. J Clin Oncol 2014; 32 (9): 949–959. doi: 10.1200/JCO.2013.53.0808.
23. Cheung YT, Sabin ND, Reddick WE et al. Leukoencephalopathy and long-term neurobehavioural, neurocognitive, and brain imaging outcomes in survivors of childhood acute lymphoblastic leukaemia treated with chemotherapy: a longitudinal analysis. Lancet Haematol 2016; 3 (10): e456–e466. doi: 10.1016/S2352-3026 (16) 30110-7.
24. Lisá IA, Lisý Ľ. Akútne leukoencefalopatie – diferenciálna diagnostika. Neurol Praxi 2007; 2: 94–98.
25. Lofstad GE, Reinfjell T, Weider S et al. Neurocognitive outcome and compensating possibilities in children and adolescents treated for acute lymphoblastic leukemia with chemotherapy only. Front Psychol 2019; 10: 1027. doi: 10.3389/fpsyg.2019.01027.
26. Chiou S, Lin P, Liao Y et al. A cross-sectional follow-up study of physical morbidities, neurocognitive function, and attention problems in post-treatment childhood acute lymphoblastic leukemia survivors. Kaohsiung J Med Sci 2019; 35 (6): 373–378. doi: 10.1002/kjm2.12061.
27. Conklin HM, Krull KR, Reddick WE et al. Cognitive outcomes following contemporary treatment without cranial irradiation for childhood acute lymphoblastic leukemia. J Natl Cancer Inst 2012; 104 (18): 1386–1395. doi: 10.1093/jnci/djs344.
28. Edelmann MN, Krull KR, Liu W et al. Diffusion tensor imaging and neurocognition in survivors of childhood acute lymphoblastic leukaemia. Brain 2014; 137 (11): 2973–2983. doi: 10.1093/brain/awu230.
29. Genschaft M, Huebner T, Plessow F et al. Impact of chemotherapy for childhood leukemia on brain morphology and function. PLoS One 2013; 8 (11): e78599. doi: 10.1371/journal.pone.0078599.
30. Jacola LM, Krull KR, Pui C-H et al. Longitudinal assessment of neurocognitive outcomes in survivors of childhood acute lymphoblastic leukemia treated on a contemporary chemotherapy protocol. J Clin Oncol 2016; 34 (11): 1239–1247. doi: 10.1200/JCO.2015.64.3205.
31. Kanellopoulos A, Andersson S, Zeller B et al. Neurocognitive outcome in very long-term survivors of childhood acute lymphoblastic leukemia after treatment with chemotherapy only. Pediatr Blood Cancer 2016; 63 (1): 133–138. doi: 10.1002/pbc.25690.
32. Koerner KM, Insel KC, Hockenberry MJ et al. Impact of childhood leukemia treatment on attention measured by the continuous performance test factor structure. Oncol Nurs Forum 2019; 46 (4): E98–E106. doi: 10.1188/19.ONF.E98-E106.
33. Krull KR, Brinkman TM, Li C et al. Neurocognitive outcomes decades after treatment for childhood acute lymphoblastic leukemia: a report from the St Jude lifetime cohort study. J Clin Oncol 2013; 31 (35): 4407–4415. doi: 10.1200/JCO.2012.48.2315.
34. Krull KR, Cheung YT, Liu W et al. Chemotherapy pharmacodynamics and neuroimaging and neurocognitive outcomes in long-term survivors of childhood acute lymphoblastic leukemia. J Clin Oncol 2016; 34 (22): 2644–2653. doi: 10.1200/JCO.2015.65.4574.
35. Moore IMK, Koerner KM, Gundy PM et al. Changes in oxidant defense, apoptosis, and cognitive abilities during treatment for childhood leukemia. Biol Res Nurs 2018; 20 (4): 393–402. doi: 10.1177/1099800418763124.
36. Partanen M, Phipps S, Russell K et al. Longitudinal trajectories of neurocognitive functioning in childhood acute lymphoblastic leukemia. J Pediatr Psychol 2021; 46 (2): 168–178. doi: 10.1093/jpepsy/jsaa086.
37. van der Plas E, Schachar RJ, Hitzler J et al. Brain structure, working memory and response inhibition in childhood leukemia survivors. Brain Behav 2017; 7 (2): e00621. doi: 10.1002/brb3.621.
38. van der Plas E, Erdman L, Nieman BJ et al. Characterizing neurocognitive late effects in childhood leukemia survivors using a combination of neuropsychological and cognitive neuroscience measures. Child Neuropsychol 2018; 24 (8): 999–1014. doi: 10.1080/ 09297049.2017.1386170.
39. van der Plas E, Noakes TLS, Butcher DT et al. Cognitive and behavioral risk factors for low quality of life in survivors of childhood acute lymphoblastic leukemia. Pediatr Res 2021; 90 (2): 419–426. doi: 10.1038/s41390-020-01230-7.
40. Watanabe S, Azami Y, Ozawa M et al. Intellectual development after treatment in children with acute leukemia and brain tumor: intelligence in children with cancer. Pediatr Int 2011; 53 (5): 694–700. doi: 10.1111/j.1442-200X.2011.03355.x.
41. Zając-Spychała O, Pawlak MA, Karmelita-Katulska K et al. Long-term brain structural magnetic resonance imaging and cognitive functioning in children treated for acute lymphoblastic leukemia with high-dose methotrexate chemotherapy alone or combined with CNS radiotherapy at reduced total dose to 12 Gy. Neuroradiology 2017; 59 (2): 147–156. doi: 10.1007/s00234-016-1777-8.
42. Lezak MD. Neuropsychological assessment. Oxford, New York: Oxford University Press 2012.
43. Harila MJ, Winqvist S, Lanning M et al. Progressive neurocognitive impairment in young adult survivors of childhood acute lymphoblastic leukemia. Pediatr Blood Cancer 2009; 53 (2): 156–161. doi: 10.1002/pbc.21992.
44. Lofstad GE, Reinfjell T, Hestad K et al. Cognitive outcome in children and adolescents treated for acute lymphoblastic leukaemia with chemotherapy only. Acta Paediatr 2009; 98 (1): 180–186. doi: 10.1111/j.1651-2227.2008.01055.x.
45. Diamond A. Executive functions. Handb Clin Neurol 2020; 173: 225–240. doi: 10.1016/B978-0-444-64150-2.00020-4.
46. Friso-van den Bos I, van de Weijer-Bergsma E. Classroom versus individual working memory assessment: predicting academic achievement and the role of attention and response inhibition. Memory 2020; 28 (1): 70–82. doi: 10.1080/09658211.2019.1682170.
47. Buizer AI, de Sonneville LMJ, van den Heuvel-Eibrink MM et al. Chemotherapy and attentional dysfunction in survivors of childhood acute lymphoblastic leukemia: effect of treatment intensity. Pediatr Blood Cancer 2005; 45 (3): 281–290. doi: 10.1002/pbc.20397.
48. Insel K, Hockenberry M, Harris L et al. Declines noted in cognitive processes and association with achievement among children with leukemia. Oncol Nurs Forum 2017; 44 (4): 503–511. doi: 10.1188/17.ONF.503-511.
49. Fuhrmann D, Knoll LJ, Blakemore S-J. Adolescence as a sensitive period of brain development. Trends Cogn Sci 2015; 19 (10): 558–566. doi: 10.1016/j.tics.2015.07.008.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2023 Číslo 6
Nejčtenější v tomto čísle
- Přehled difuzních gliomů dle WHO klasifikace 2021 1. část – difuzní gliomy dospělého typu
- Efekt psychoedukačního programu u pacientů s CMP v postakutní péči
- Paměťová rezerva a údržba paměti u superúspěšně stárnoucích osmdesátníků
- Atypické případy cycloplegie způsobené durmanem obecným
