Koagulopatia pri kraniocerebrálnom poranení u detí a mladistvých
A Coagulopathy Following Craniocerebral Injury in Children and Adolescents
Aim:
To examine a relationship between coagulation parameters (prothrombin time, international normalized ratio, activated partial thromboplastin time, thrombin time and platelet count) and outcome in children after isolated craniocerebral injury.
Methods:
A retrospective study included 51 children (33 males and 18 females) aged 1–17 years, who undergone a surgery between 1. 1. 2005 and 1. 3. 2011. Coagulation parameters, examined within 6 hours after the injury, were compared for different types of craniocerebral injury and correlated with neurological status after injury and after treatment.
Results:
Coagulation parameters correlated with neurological status after injury and after treatment and differed significantly for different types of craniocerebral injury (except platelet count).
Conclusion:
A coagulation disorder occurring after an isolated craniocerebral injury in children is a negative prognostic factor that requires an urgent and aggressive therapy.
Key words:
craniocerebral injury – coagulopathy – prognosis
Autoři:
M. Benčo 1; J. De Riggo 1; S. Nosáľ 2; M. Fedor 2; J. Šutovský 1; R. Opšenák 1
Působiště autorů:
UN Martin
Neurochirurgické oddelenie
1; UN Martin
Klinika detskej anestéziológie a intenzívnej medicíny JLF UK v Martine
2
Vyšlo v časopise:
Cesk Slov Neurol N 2012; 75/108(4): 432-437
Kategorie:
Původní práce
Souhrn
Cieľ:
Vyhodnotenie vzťahu parametrov koagulácie (protrombínový čas, medzinárodný normalizovaný pomer, aktivovaný parciálny tromboplastínový čas, trombínový čas a počet trombocytov) u detí a mladistvých po izolovanom kraniocerebrálnom poranení k neurologickému stavu po úraze, typu poranenia a prognóze.
Súbor a metodika:
Do retrospektívnej štúdie sme zahrnuli 51 detí a mladistvých (33 chlapcov a 18 dievčat) vo veku 1–17 rokov, ktorí boli operovaní na našom pracovisku od 1. 1. 2005 do 1. 3. 2011. Parametre koagulácie, ktoré boli vyšetrené do 6 hodín po úraze, sme porovnali pri rôznych typoch kraniocerebrálneho poranenia a štatisticky korelovali so vstupným a výstupným neurologickým stavom.
Výsledky:
Parametre koagulácie sa štatisticky významne líšili pri rôznych typoch kraniocerebrálneho poranenia a korelovali so vstupným a výstupným neurologickým stavom.
Záver:
Porucha koagulácie, ktorá vzniká po izolovanom kraniocerebrálnom poranení u detí a mladistvých, je nepriaznivým prognostickým faktorom, ktorý vyžaduje rýchlu a agresívnu liečbu.
Klíčová slova:
kraniocerebrálne poranenie – koagulopatia – prognóza
Úvod
Každý rok zomiera vo svete viac ako 20 000 detí na následky poranení, ktoré vznikli následkom dopravných nehôd, pádov a pri bicyklovaní [1]. Poranenie hlavy je hlavnou príčinou morbidity a mortality u detí medzi 1. a 14. rokom života, ktoré zapríčiňuje viac ako 70 % všetkých úmrtí detí po úrazoch [2]. Finančné a spoločenské náklady, ktoré sú potrebné na liečbu a rehabilitáciu týchto pacientov spolu s nákladmi spojenými s ich invalidizáciou sú enormné. Aj napriek dlhodobému úsiliu lekárov a dosiahnutým pokrokom v liečbe a rehabilitácii len 40–50 % pacientov po kraniocerebrálnom poranení (KCP) dosahuje úplné uzdravenie bez trvalého neurologického postihnutia [3,4]. Doterajšie úsilie vynakladané k zlepšeniu výsledkov liečby pacientov po KCP bolo zamerané na prevenciu vzniku sekundárneho poškodenia mozgu v dôsledku hypoperfúzie a hypoxie a liečbu poúrazovej neuroendokrinnej dysfunkcie [5–7]. Ukazuje sa však, že KCP vedie aj k aktivácii koagulácie, ktorá významne ovplyvňuje výsledky liečby [8].
KCP vedie k spusteniu vonkajšej aj vnútornej cesty aktivácie koagulácie. Aktivácia vonkajšej cesty začína uvoľnením tkanivového aktivátora – tkanivový tromboplastín (faktor III), ktorý je vo veľkom množstve obsiahnutý hlavne v cerebrálnom kortexe. Aktivácia vnútornej cesty začína kontaktom krvi s odhaleným subendoteliálnym kolagénom v dôsledku mechanického poškodenia cievnej steny a extravaskulárnych tkanív. Po KCP dominuje aktivácia koagulácie vonkajšou cestou [8]. Vonkajšia cesta aktivácie koagulácie spočíva v aktivácii faktora X (Stuartov-Prowerovej faktor) uvoľneným tkanivovým tromboplastínom, ktorý vytvára komplex s faktorom VII (prokonvertín). Aktivovaný faktor X, spolu s faktorom V (proakcelerín), vytvárajú komplex, tzv. aktivátor protrombínu, ktorý štiepi protrombín (faktor II) na trombín [9]. Dochádza k vzniku trombov a poškodenie nervového tkaniva je spôsobené poruchou mikrocirkulácie [8].
Aktivácia koagulácie po KCP predstavuje fyziologický proces vedúci k minimalizácii a zástave krvácania. Spôsobuje však aj poruchu mikrocirkulácie v dôsledku tvorby trombov a konzumpciu koagulačných faktorov, ktoré môžu viesť v extrémnej situácii ku vzniku disseminovanej intravaskulárnej koagulácie a krvácavým komplikáciám. Mnohé štúdie poukázali na to, že zmeny v parametroch koagulácie korelujú s veľkosťou objemu poškodeného mozgového tkaniva vizualizovaného CT vyšetrením a sú indikátorom vzniku diseminovanej intravaskulárnej koagulácie (DIC) a hemoragických komplikácií [10,11].
Cieľom predkladanej štúdie je vyhodnotenie vzťahu parametrov koagulácie u detí a mladistvých po izolovanom kraniocerebrálnom poranení k neurologickému stavu po úraze, typu poranenia a prognóze.
Súbor a metodika
Na základe retrospektívnej analýzy dokumentácie 60 detí a mladistvých po KCP, realizovanej jedným autorom (MB), sme do štúdie zaradili 51 pacientov, ktorí boli hospitalizovaní od 1. 1. 2005 do 1. 3. 2011 pre izolované kraniocerebrálne poranenie a ktorých stav vyžadoval operačnú liečbu. Z nich bolo 33 chlapcov a 18 dievčat. Priemerný vek chlapcov bol 9,31 roka (smerodajná odchýlka SD = 4,52 roka, najmladší 1 rok, najstarší 17 rokov), priemerný vek dievčat bol nižší, 6,35 roka (SD = 5,34 roka, najmladšia 1 rok, najstaršia 17 rokov).
Kritériá, ktoré vylučovali pacientov zo štúdie, boli polytrauma alebo pridružená trauma, známa porucha koagulácie a stavy nevyžadujúce operačnú liečbu. Pacientom bolo určené Glasgow Coma Scale (GCS) pri príjme, resp. pred zatlmením. Z periférnej krvi boli do 6 hodín po úraze odobraté vzorky na vyšetrenie základných parametrov koagulácie – protrombínový čas (Quickov čas, PT), Medzinárodný normalizovaný pomer (INR), aktivovaný parciálny tromboplastínový čas (APTT), trombínový čas (TT) a počet trombocytov (PLT). V prípade, že parametre koagulácie boli vyšetrené neskôr ako 6 hodín po úraze alebo až po operačnej liečbe, alebo ich vyšetreniu predchádzal invazívny výkon väčšieho rozsahu, pacienti neboli zaradení do štúdie. Do štúdie boli zaradené len tie deti a mladiství, u ktorých bola medikácia ovplyvňujúca koaguláciu podávaná až po vyšetrení parametrov koagulácie. U každého pacienta bolo realizované vyšetrenie intrakránia počítačovou tomografiou (CT) a stanovené Glasgow Outcome Score (GOS) 3 mesiace po úraze. GOS 1 = smrť; GOS 2 = vegetatívny stav; GOS 3 = nažive, ale funkčne postihnutý; GOS 4 = minimálna dysfunkcia a GOS 5 = neurologický stav ako pred poranením. CT nálezy sme podľa predpokladanej, zvyšujúcej sa miery poškodenia nervového tkaniva a vaskulárnych štruktúr rozdelili na tri skupiny – fraktúra kalvy alebo lebečnej spodiny (FR), extracerebrálny hematóm – subdurálny alebo epidurálny (ECH) a hemoragická kontúzia, resp. úrazový intracerebrálny hematóm (HK). V prípade KCP, ktoré bolo kombináciou nami zvolených typov poranení, sme dieťa zaradili do skupiny s predpokladaným vyšším poškodením nervového tkaniva a vaskulárnych štruktúr.
Štatistické hodnotenie
Štatistickou analýzou sme vyhodnotili:
- koreláciu parametrov koagulácie s CT nálezom pred operačnou liečbou,
- koreláciu parametrov koagulácie so vstupným neurologickým sta-vom (GCS),
- koreláciu parametrov koagulácie s výstupným neurologickým stavom tri mesiace po úraze (GOS),
- rozdiely v parametroch koagulácie pri jednotlivých typoch KCP,
- rozdiely v parametroch koagulácie medzi deťmi a mladistvými, ktoré poranenie prežili, a zomrelými,
- rozdiely v parametroch koagulácie medzi deťmi a mladistvými, u ktorých sa vyskytla pooperačná komplikácia a bez pooperačných komplikácií.
K štatistickému vyhodnoteniu a koreláciám sme použili Spearmanov rho (rs) korelačný koeficient, Kruskal-Wallisov test a Mann-Whitneyho U test vypočítané počítačový softwarom StasDirect®. Všetky testy boli dvojstranové, štatistická významnosť bola nastavená na p = 0,05. K interpretácii Spearmanovho korelačného koeficientu sme použili schému podľa Cohena – absolútne hodnoty do 0,1 predstavujú triviálnu koreláciu, hodnoty medzi 0,1 a 0,3 predstavujú slabú koreláciu, 0,3–0,5 stredne silnú koreláciu a hodnoty nad 0,5 silnú koreláciu [12].
Výsledky
U všetkých pacientov, ktorí boli zaradení do štúdie, bolo prvotné vyšetrenie parametrov koagulácie realizované do 6 hodín po úraze. Priemerný čas od úrazu po odber krvi na vyšetrenie parametrov koagulácie bol 2 hodiny a 42 minút, priemerný čas od úrazu po operačnú liečbu bol 12 hodín 15 minút. Priemerná doba hospitalizácie v nami sledovanom súbore bola 23 dní (tab. 1).
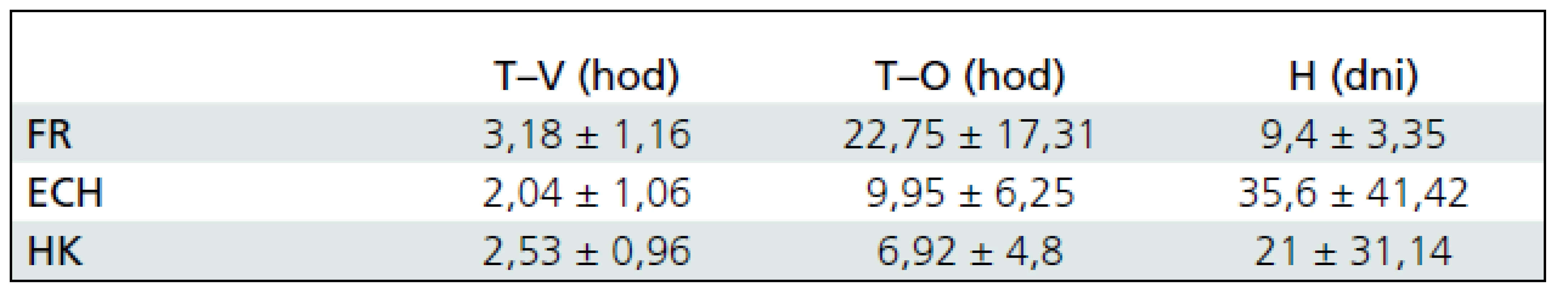
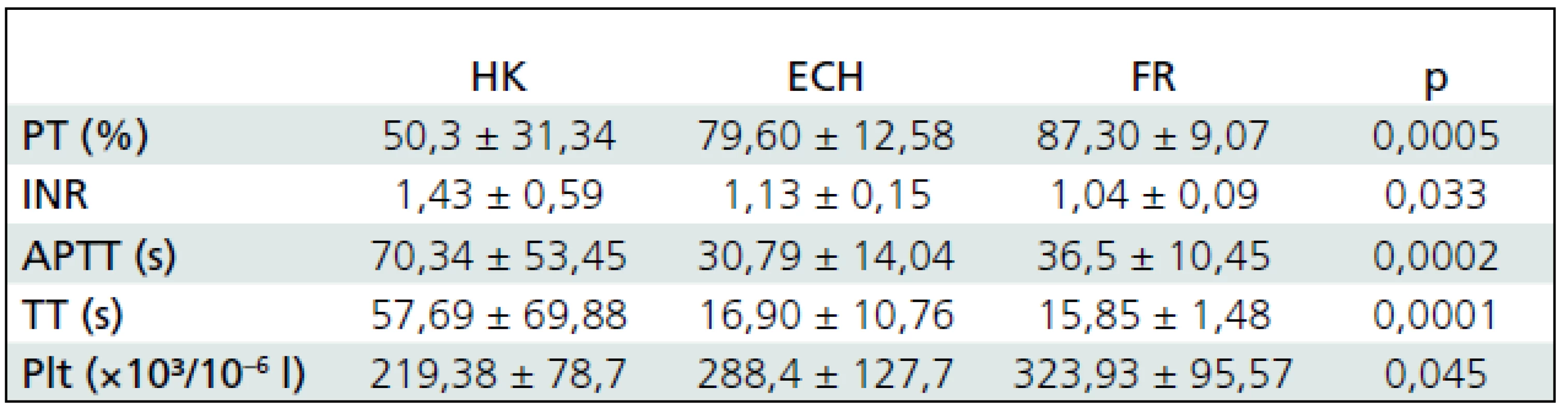
CT vyšetrením sme u 13 pacientov verifikovali fraktúru kalvy alebo lebečnej spodiny, u 22 pacientov extracerebrálny hematóm (subdurálny alebo epidurálny) a u 16 pacientov hemoragickú kontúziu alebo traumatický intracerebrálny hematóm. Patologická hodnota aspoň v jednom sledovanom laboratórnom parametri koagulácie bola prítomná u 11 pacientov s hemoragickou kontúziou a u 6 pacientov s extracerebrálnym hematómom a nebola prítomná ani u jedného pacienta s fraktúrou. Porovnaním parametrov koagulácie u všetkých detí a mladistvých zaradených do súboru pri jednotlivých typoch KCP sme zistili štatisticky významné rozdiely v absolútnych hodnotách všetkých sledovaných parametrov koagulácie (tab. 2). V podsúbore detí a mladistvých s extracerebrálnym hematómom a hemoragickou kontúziou sme korelovali objem hematómov a kontúzií, ako aj presun stredočiarových štruktúr s parametrami koagulácie, zistené korelácie boli len triviálne.
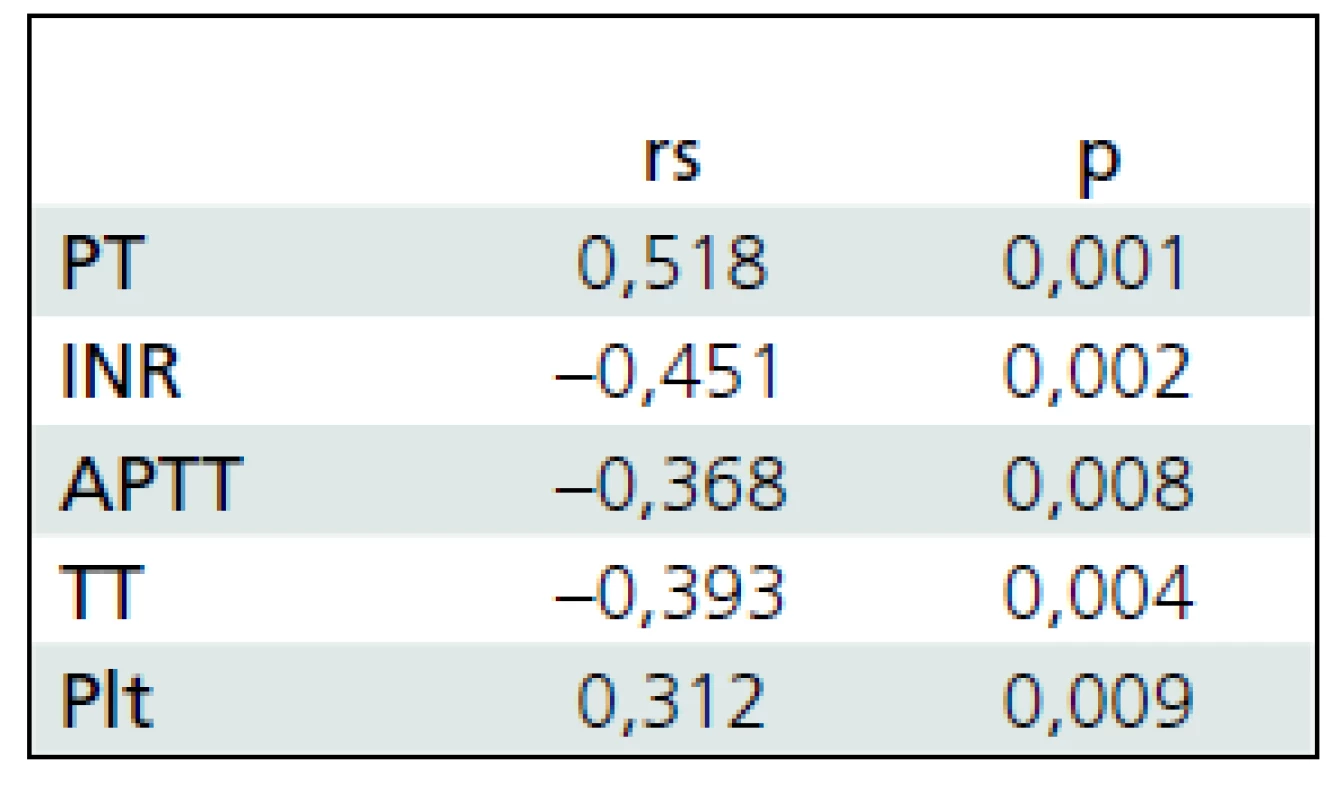
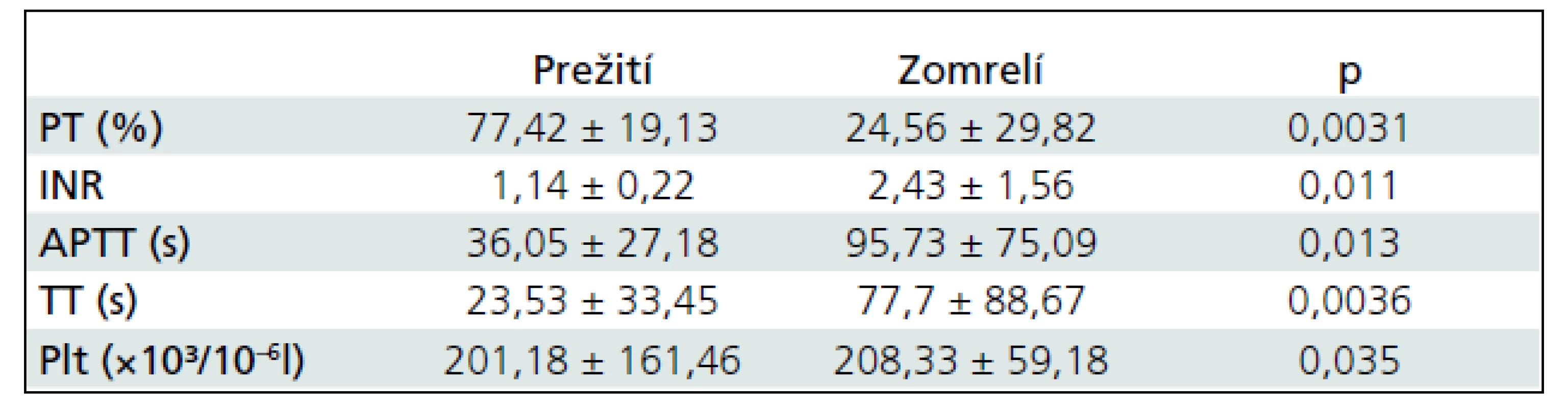
Vyhodnotením prítomnosti poruchy koagulácie v závislosti od neurologického stavu pri príjme a o 3 mesiace po poranení sme zistili, že patologické hypokoagulačné hodnoty aspoň v jednom sledovanom parametri koagulácie mali všetci pacienti so vstupným GCS 3–4 body, 50 % pacientov s GCS 5–6 bodov, 13 % pacientov s GCS 7–8 bodov a žiaden pacient s GCS 9 bodov a viac (graf 1). Taktiež z hľadiska neurologického stavu po liečbe mali patologické hypokoagulačné hodnoty všetci pacienti s GOS 1, 50 % pacientov s GOS 2, 22 % pacientov s GOS 3, 18 % pacientov s GCS 4 a 7 % pacientov s GOS 5 (graf 2). Štatistickou koreláciou neurologického stavu pacientov bezprostredne po poranení (GCS) a 3 mesiace po poranení (GOS) s parametrami koagulácie sme zistili silnú koreláciu protrombínového času s GCS a stredne silnú koreláciu ostatných sledovaných parametrov s GCS (tab. 3) a stredne silnú koreláciu všetkých parametrov okrem Plt (slabá korelácia) s GOS (tab. 4). Štatisticky významné rozdiely v sledovaných parametroch koagulácie boli tiež nájdené medzi deťmi, ktoré poranenie prežili, a zomrelými (tab. 5).



Pooperačná komplikácia sa vyskytla v nami sledovanom súbore u 8 pacientov, pričom v 6 prípadoch došlo k pooperačnému vzniku extracerebrálneho hematómu (v štyroch prípadoch subdurálneho hematómu a v dvoch prípadoch epidurálneho hematómu), v jednom prípade sa objavila likvorea z operačnej rany, ktorá vyžadovala operačnú revíziu a v jednom prípade sa vyskytol absces v operačnej rane. Štatistickým porovnaním sme nezistili významné rozdiely v sledovaných parametroch koagulácie medzi deťmi a mladistvými, ktoré prekonali operačnú liečbu bez komplikácie a s komplikáciou (tab. 6).

Diskusia
Kraniocerebrálne poranenie je vedúcou príčinou mortality u detí starších ako 1 rok. K dosiahnutiu optimalizácie terapeutického postupu je preto nevyhnutné identifikovať faktory, ktoré predisponujú k nepriaznivým výsledkom liečby [13]. V našej štúdii sme použili GCS ako všeobecne akceptovaný štandard pre určenie miery poruchy vedomia a GOS pre vyhodnotenie neurologického stavu po KCP [14].
Pacienti, ktorí boli zaradení do štúdie, boli rozdelení do podsúborov tak, že v prípade prítomnosti kombinácie nami zvolených typov poranenia sme pacienta zaradili do skupiny s predpokladaným vyšším poškodením nervového tkaniva a vaskulárnych štruktúr. Toto rozdelenie nebolo totožné s rozdelením podľa indikácie k operačnej liečbe. Aj v prípadoch, keď bol indikáciou k operácii napr. extracerebrálny hematóm s drobnou hemoragickou kontúziou, sme pacienta zaradili do skupiny „hemoragická kontúzia, resp. úrazový intracerebrálny hematom“. Toto rozdelenie považujeme za vhodnejšie, ako delenie podľa indikácie k operačnej liečbe, nakoľko lepšie zohľadňuje vplyv typu poranenia na poruchu koagulácie.
V sledovanom súbore pacientov bolo realizované prvotné vyšetrenie parametrov koagulácie do 6 hodín po úraze. Absolútna hodnota sledovaných parametrov bola štatisticky porovnaná pri rôznych typoch poranení a korelovaná so vstupným neurologickým stavom a stavom po liečbe. Domnievame sa, že absolútna hodnota parametrov koagulácie, ktorá bola vyšetrená pred zahájením akejkoľvek liečby, najlepšie odzrkadľuje stav hemokoagulácie alterovanej len kraniocerebrálnym poranením. Sledovanie dynamiky zmeny parametrov koagulácie, ktoré bolo realizované v niektorých štúdiách, naráža na viaceré úskalia [14]. Na jednej strane substitúcia konzumpcie koagulačných faktorov, na druhej strane realizovaná operačná liečba rôzneho rozsahu spôsobujú zmeny v parametroch koagulácie, ktorých mieru ovplyvnenia je metodicky komplikované odlíšiť od vplyvu KCP. Preto sme v nami sledovanom súbore vychádzali z prvotného vyšetrenia, ktoré objektivizovalo stav koagulácie, ktorý bol ovplyvnený len kraniocerebrálnym poranením.
Kraniocerebrálne poranenia zahŕňa širokú skupinu stavov, ktoré je možné liečiť len konzervatívne, ako aj stavy vyžadujúce urgentnú operačnú intervenciu. V prípadoch, ktoré vyžadujú urgentnú operačnú intervenciu je vznik koagulopatie limitujúcim faktorom, ktorý operačnú liečbu v určitom okamihu neumožňuje. Pri súčasných terapeutických možnostiach terapie koagulopatie je práve časový faktor urgentnosti operačnej liečby určujúcim pre použitý postup. Pri porovnaní liečby koagulopatie po KCP mrazenou plazmou a faktorom VII sa ukazuje, že podávanie faktora VII nielen skracuje čas potrebný ku korekcii koagulopatie, a tým aj k neurochirurgickej intervencii, ale umožňuje aj zníženie celkových nákladov na liečbu [15,16].
Stein et al vo svojej štúdii realizovanej na 253 pacientoch preukázali, že zmeny v parametroch koagulácie korelujú s veľkosťou objemu poškodeného mozgového tkaniva vizualizovaného CT vyšetrením [11]. V nami sledovanom súbore pacientov táto korelácia potvrdená nebola. Predpokladáme, že táto diskrepancia mohla byť spôsobená jednak rozdielnou štatistickou metodikou (v nami sledovanom súbore bola korelovaná absolútna hodnota parametrov koagulácie), ako aj rozdielnou veľkosťou súboru. Taktiež nemôžeme vylúčiť možnosť, že korelácia grafického nálezu a parametrov koagulácie je v detstve a v dospelosti rozdielna. Odpoveď na tieto otázky vyžaduje rozsiahlejší súbor detí a ďalší výskum.
Vzťah GCS ako prediktora GOS je známy a všeobecne akceptovaný [17]. V našej štúdii sme zistili, že hladina koagulačných parametrov po KCP u detí koreluje s GCS a aj GOS. Silná korelácia protrombínového času s GCS v porovnaní so stredne silnou koreláciou APTT potvrdzuje, že aktivácia vonkajšej cesty zrážania krvi je po KCP dominujúca. Najslabšou sa ukazuje korelácia počtu trombocytov. Príčinu tohto javu nevieme vysvetliť, ale podobnú slabú koreláciou preukázali aj iní autori [8].
Štatisticky významné rozdiely, ktoré sme zistili v absolútnych hodnotách sledovaných parametrov koagulácie pri rôznych typoch kraniocerebrálneho poranenia, poukazujú na skutočnosť, že miera poškodenia nervového tkaniva a vaskulárnych štruktúr cerebrálneho kortexu je určujúca pre množstvo uvoľneného tkanivového tromboplastínu, a tým aj pre rozvoj koagulopatie a výsledný nepriaznivý outcome. Otázkou ostáva, či je rozvoj koagulopatie po KCP následkom závažného poranenia mozgu, ktoré predisponuje k nepriaznivému outcome, alebo je príčinou nepriaznivého outcome. Vavilala et al vo svojej štúdii upozorňujú na skutočnosť, že zatiaľ čo pri GCS 3–6 bodov a 13–15 bodov silne koreluje GCS a GOS, pri GCS 7–12 bodov parametre koagulácie výrazne lepšie korelujú s GOS ako s GCS [13]. Je teda možné predpokladať, že miera aktivácie koagulácie je pri týchto pacientoch rozhodujúcejší faktor, ktorý rozhoduje o priaznivom alebo nepriaznivom outcome, ako vstupný neurologický stav.
Štatistickým porovnaním sme zistili významné rozdiely v parametroch koagulácie medzi deťmi a mladistvými, ktorí poranenie prežili, a zomrelými. Zároveň sme nezistili rozdiely medzi deťmi a mladistvými, ktorí museli byť opätovne operovaní, a pacientmi bez pooperačnej komplikácie. Predpokladáme, že vznik koagulopatie pravdepodobne neovplyvňuje riziko vzniku pooperačných komplikácií. Odzrkadľuje však mieru konzumpcie faktorov zrážania v dôsledku vzniku trombov a rozsah poruchy mikrocirkulácie, ktorý sa spolupodieľa na sekundárnom poškodení mozgu.
Aktivácia koagulácie po KCP vedie k poruche mikrocirkulácie v dôsledku tvorby trombov, ale aj konzumpciou koagulačných faktorov predisponuje k možnému rozvoju DIC, a tým aj k hemoragickým komplikáciám [8,10,11]. Do predkladanej štúdie boli zaradené tri deti, ktoré KCP neprežili. Nezomreli však na následky DIC, ale na následky poranenia mozgu. Dve deti, ktoré zomreli na následky DIC, do štúdie neboli zaradené, nakoľko obidve prekonali polytraumu, takže ovplyvnenie koagulácie nevzniklo len na základe KCP. V našom súbore teda KCP samostatne neviedlo k rozvoju DIC. Predpokladáme však, že bez adekvátnej liečby (podávanie hemostyptík, mrazenej plazmy a faktora VII), ktorá bola u detí realizovaná, by pravdepodobne k rozvoju DIC mohlo dôjsť. Ukazuje sa teda, že po samostatnom KCP pri adekvátnej liečbe ohrozuje pacienta výraznejšie porucha mikrocirkulácie ako DIC a hemoragické komplikácie.
Predkladaná štúdia, realizovaná retrospektívne, má svoje limity. V nami sledovanom súbore sme v štatistickom porovnaní a koreláciách vychádzali z absolútnej hodnoty sledovaných parametrov koagulácie, ktorá bola verifikovaná prvotným vyšetrením krvi. Individuálne rôzny časový odstup operačnej liečby od prvotného vyšetrenia parametrov koagulácie, rozdiely v medikácii, ktorá bola predoperačne podávaná, ale hlavne rozdielny vplyv operačnej liečby, ktorá bola realizovaná pri rozdielnych typoch kraniocerebrálnych poranení znemožňuje odlíšiť vplyv KCP, medikácie a peroperačnej konzumpcie na zmenu parametrov koagulácie. Sledovanie dynamiky zmeny parametrov koagulácie bolo problematické aj v dôsledku rozdielneho časového odstupu prvotného a následného vyšetrenia parametrov koagulácie. Taktiež vplyv operačnej liečby, ktorá ovplyvňuje koaguláciu rozdielne pri operačných výkonoch rôzneho rozsahu v závislosti od typu KCP, nebol u pacientov zaradených do súboru uniformný. Ukazuje sa, že nielen dynamika zmeny parametrov koagulácie, ale aj ich absolútna hodnota bezprostredne po KCP predisponuje pacienta k priaznivému alebo nepriaznivému neurologickému stavu po liečbe [10].
Aktivácia koagulácie po KCP u detí je dôležitým faktorom, ktorý rozhoduje o výsledku liečby. Prítomnosť poruchy koagulácie je nepriaznivým prognostickým faktorom. V prípade stredne ťažkého poranenia mozgu má dokonca väčšiu prediktívnu hodnotu ako GCS [13]. Ak je teda pri vstupnom GCS 7–12 bodov indikovaná operačná liečba, nevyhnutne musí konzumpciou koagulačných faktorov zvyšovať riziko nepriaznivého outcome, ktorému má práve zabrániť. Je teda nevyhnutné operačnú liečbu realizovať len v indikovaných prípadoch s precízne vykonávanou hemostázou k prevencii vzniku poruchy koagulácie.
Otázkou ostáva, či porucha koagulácie po KCP vzniká u detí častejšie a či je závažnejšia ako u dospelých. Štatistické porovnanie parametrov koagulácie detí a dospelých má svoje limity, preto presnú odpoveď nie je ľahké nájsť. Predpokladáme však, že uvoľnenie tkanivového aktivátora pri rovnakom KCP u detí má rovnaké následky na mikrocirkuláciu ako u dospelých. Rozdiel je však vo vyššej konzumpcii koagulačných faktorov u detí vzhľadom na absolútne nižšie množstvo koagulačných faktorov pripadajúcich na kortex viazaný tromboplastín, ako u dospelých. Tento rozdiel pravdepodobne predisponuje deti po KCP k rozvoju DIC a hemoragickým komplikáciám výraznejšie ako dospelých. Odpoveď na túto otázku však vyžaduje rozsiahlejší súbor pacientov a ďalší výskum.
Záver
V predkladanej štúdii sme potvrdili rozdielnu mieru ovplyvnenia parametrov koagulácie pri rôznych typoch KCP u detí a mladistvých a koreláciu všetkých sledovaných parametrov koagulácie s GCS po poranení a s GOS (okrem hladiny Plt) tri mesiace po liečbe.
Klinická implementácia týchto poznatkov je nasledovná:
- bezprostredne po KCP u detí je nevyhnutné pátrať po vznikajúcej poruche koagulácie a aj v prípade, že nevznikla, pravidelne kontrolovať parametre koagulácie,
- v prípade jej vzniku je potrebná rýchla a agresívna liečba v prevencii nepriaznivého outcome,
- precízna hemostáza počas operačnej liečby po KCP u detí predchádza znížením konzumpcie koagulačných faktorov zhoršeniu ich prognózy.
Podpora Grantu „OPV – 26110230031/02/PD2010“.
MUDr. Martin Benčo, PhD.
Neurochirurgické oddelenie UN
Kollárova 2
036 01 Martin
e-mail: benco.martin@gmail.com
Prijaté k recenzii: 27. 6. 2011
Prijaté do tlače: 14. 2. 2012
Zdroje
1. Stein SC, Spettell CM. Delayed and progressive brain injury in children and adolescents with head trauma. Pediatr Neurosurg 1995; 23(6): 299–304.
2. Bruce DA. Head trauma. In: Eichelberger MR (ed). Pediatric Trauma. St. Louis: Mosby Year Book 1993 : 353–361.
3. Kirsch TD, Lipinski AC. Head injury. In: Tintinalli JE (ed). Emergency medicine: A comprehensive study guide. 6th ed. New York: McGraw-Hill 2004 : 1557–1569.
4. Valadka AB. Injury to the cranium. In: Mattox KL, Feliciano DV, Moore EE (eds). Trauma. 4th ed. New York: McGraw-Hill 2000 : 377–399.
5. Smrčka M. Monitoring pacientů s těžkým poraněním mozku. Cesk Slov Neurol N 2011; 74/107(1): 9–21.
6. Zapletalová J, Aleksijević D, Smolka V, Krahulík D, Fryšák Z. Posttraumatický hypopituitarizmus u dětí a dospívajících. Cesk Slov Neurol N 2010; 73/106(4): 398–401.
7. Aleksijević D, Zapletalová J, Smolka V, Klásková E, Wiedermann J, Krahulík D et al. Neuroendokrinní dysfunkce u dětí a dospívajících po úrazu mozku. Cesk Slov Neurol N 2010; 73/106(4): 409–414.
8. Bayir A, Kalkan E, Koçak S, Ak A, Cander B, Bodur S. Fibrinolytic markers and neurologic outcome in traumatic brain injury. Neurol India 2006; 54(4): 363–365.
9. Bauer J. Antikoagulační terapie v prevenci a léčbě ischemických iktů. Cesk Slov Neurol N 2010;73/106(5): 480–491.
10. Engström M, Romner B, Schalén W, Reinstrup B. Thrombocytopenia predicts progressive hemorrhage after head trauma. J Neurotrauma 2005; 22(2): 291–296.
11. Stein SC, Young GS, Talucci RC, Greenbaum BH, Ross SE. Delayed brain injury after head trauma: significance of coagulopathy. Neurosurgery 1992; 30(2): 160–165.
12. Cohen J. Statistical power analysis for the behavioral sciences. 2nd ed. Hillsdale: Lawrance Earlbaum Associates 1998.
13. Vavilala MS, Dunbar PJ, Rivara FP, Lam AM. Coagulopathy predicts poor outcome following head injury in children less than 16 years of age. J Neurosurg Anesthesiol 2001; 13(1): 13–18.
14. String T, Robinson AJ, Blaisdell FW. Massive trauma: effect of intravascular coagulation on prognosis. Arch Surg 1971; 102(4): 406–411.
15. Dutton RP. Factor VII and the brain: time to get this research done! Crit Care 2007; 11(4): 161.
16. Stein DM, Dutton RP, Kramer ME, Scalea TM. Reversal of coagulopathy in critically ill patients with traumatic brain injury: recombinant factor VIIa is more cost--effective than plasma. J Trauma 2009; 66(1): 63–72.
17. Jennett B, Teasdale G, Braakman R, Minderhoud J, Knill-Jones R. Predicting outcome in individual patients after severe head injury. Lancet 1976; 1(7968): 1031–1034.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2012 Číslo 4
-
Všechny články tohoto čísla
- Komentář k minimonografii P. Štourače
- Imunomodulační léčba roztroušené sklerózy mozkomíšní v klinických a zobrazovacích parametrech
- Prostorová orientace při fyziologickém a patologickém stárnutí
- Porucha spánku s rytmickými pohyby
- Meningeomy pochev zrakového nervu – přehled současných léčebných možností
- Stanovení prognostických faktorů trombolytické léčby u pacientů s akutním mozkovým infarktem – analýza registru SITS
- Koagulopatia pri kraniocerebrálnom poranení u detí a mladistvých
- Léčba obstrukční spánkové apnoe pomocí CPAP snižuje nezávisle hladinu A-FABP a CRP
- Přístrojově asistované kvantitativní testování senzitivity – normativní data
- Vyšetření hustoty intraepidermálních nervových vláken z kožní biopsie – normativní data
- Oswestry dotazník, verze 2.1a – výsledky u pacientů s lumbální spinální stenózou, srovnání se starší verzí dotazníku
- Peroperační elektromyografie svěračového komplexu anorekta dětí s anorektálními malformacemi
- Vliv novorozenecké žloutenky na vznik autizmu
- Izolovaná sfenoidální sinusitida – možná příčina bolestí hlavy a závažných komplikací
- Mozkové arachnoidální cysty u dospělých – retrospektivní analýza výsledků chirurgické terapie
- Hyperbarická oxygenační terapie závažných kraniocerebrálních poranění u dětí a adolescentů
- Primárně extradurální meningeom prezentující se Garcinovým syndromem – kazuistika
- Austrianův syndrom: pneumokoková meningitida, pneumonie a endokarditida – kazuistika
- Lewisův- Sumnerův syndrom – kazuistika
- Webové okénko
-
Analýza dat v neurologii
XXXIV. Bayesovské sítě - V. neuromuskulární kongres, 3.–4. května 2012 v Brně
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Mozkové arachnoidální cysty u dospělých – retrospektivní analýza výsledků chirurgické terapie
- Porucha spánku s rytmickými pohyby
- Izolovaná sfenoidální sinusitida – možná příčina bolestí hlavy a závažných komplikací
- Oswestry dotazník, verze 2.1a – výsledky u pacientů s lumbální spinální stenózou, srovnání se starší verzí dotazníku
