2020 AAN Highlights Dlouhodobá data o účinnosti deplece CD20+ B-buněk v léčbě RS
Autoři:
Ing. Šárka Spáčilová 1; doc. MUDr. Dana Horáková, Ph.D. 2
Působiště autorů:
šéfredaktorka Terapie. digital a Florence
1; Neurologická klinika 1. LF UK a VFN v Praze
2
Vyšlo v časopise:
Cesk Slov Neurol N 2020; 83/116(4): 453-454
Kategorie:
Zprávy z odborných akcí
Prvním a dosud jediným registrovaným přípravkem pro léčbu pacientů jak s relabující RS (RRS), tak s primárně progresivní RS (PPRS) je ocrelizumab (Ocrevus [Roche, Basilej, Švýcarsko]). Tato rekombinantní humanizovaná monoklonální protilátka selektivně cílí na B-buňky exprimující povrchový antigen CD20.
Imunomodulační účinek ocrelizumabu je zprostředkovaný více mechanismy, mezi něž patrně patří buněčná fagocytóza závislá na protilátkách, cytototoxicita závislá na protilátkách i komplementu a apoptóza, a vede k selektivnímu snížení počtu CD20+ B-buněk a jejich funkce.
V průběhu webcastu vysílaného 28. dubna v rámci virtuální platformy 2020 AAN Highlights, která v čase pandemie COVID-19 nahradila letošní výroční kongres American Academy of Neurology, zazněla nová data o dlouhodobé účinnosti a bezpečnosti podávání ocrelizumabu v klinické praxi. Přednesl je Dr. Paulo Fontoura, Ph.D., Global Head Neuroscience and Rare Diseases Clinical Development společnosti Roche.
Data pocházející od více než 150 000 pacientů z celého světa svědčí o setrvale příznivém bezpečnostním profilu ocrelizumabu, vč. nulového výskytu případů progresivní multifokální leukoencefalopatie. Dlouhodobá sledování potvrzují i konzistentní zlepšení ukazatelů progrese RS – klinických i na MR.
O 49 % nižší riziko invalidity oproti IFN-β
Mezi klinickými ukazateli Dr. Fontoura zdůraznil klíčovou úlohu hodnoty na rozšířené stupnici stavu invalidity (expanded disability status scale; EDSS) ≥ 6, při jejímž dosažení již pacient není schopen chůze bez hole a výrazně u něj stoupá riziko nevratné disability a trvalého snížení schopnosti pracovat.
V programu dvojitě zaslepených klinických studií 3. fáze OPERA I/II byli pacienti s RRS randomizováni k podávání ocrelizumabu (n = 837), nebo interferonu beta (IFN-b) (n = 829). Po 96 týdnech trvání studie činilo zastoupení pacientů s EDSS ≥ 6 přetrvávající po dobu min. 48 týdnů 0,8 % v rameni s ocrelizumabem vs. 3,1 % v rameni s IFN-b.
Po odslepení mohli pacienti užívající IFN-b přestoupit do ramene s ocrelizumabem. Po dalších 4 letech trvání této otevřené extenze studijního programu OPERA, tedy na konci 288. týdne celkového sledování, efekt časného užívání ocrelizumabu nadále přetrvává, riziko EDSS ≥ 6 je u pacientů léčených ocrelizumabem od samého počátku o 49 % nižší oproti nemocným, kteří na léčbu přešli až po 2 letech užívání IFN-b, a to statisticky významně (p = 0,0042).
Vyšší míra zachování objemu mozku
Senzitivním ukazatelem korelujícím s mírou progrese RS a disability je celková a/nebo regionální atrofie mozku a míchy při zobrazení na MR. Její zpomalení, resp. zastavení je tedy v současnosti jedním z hlavních cílů léčby RS.
V již zmíněném programu klinických studií OPERA I/II měli ve 48. týdnu pacienti užívající ocrelizumab o 41 % menší úbytek objemu talamu oproti výchozímu stavu při zařazení do studie než nemocní zařazení do ramene s IFN-b (úbytek objemu –1,28 vs. –2,17 %; p < 0,001). Na konci zaslepené fáze studie v 96. týdnu se jednalo o rozdíl o 42 % (–1,67 vs. –2,91 %; p < 0,001) ve prospěch ocrelizumabu (obr. 1).
Fig. 1. Ocrelizumab eff ect on slowdown of thalamic atrophy in patients with RMS and PPMS.
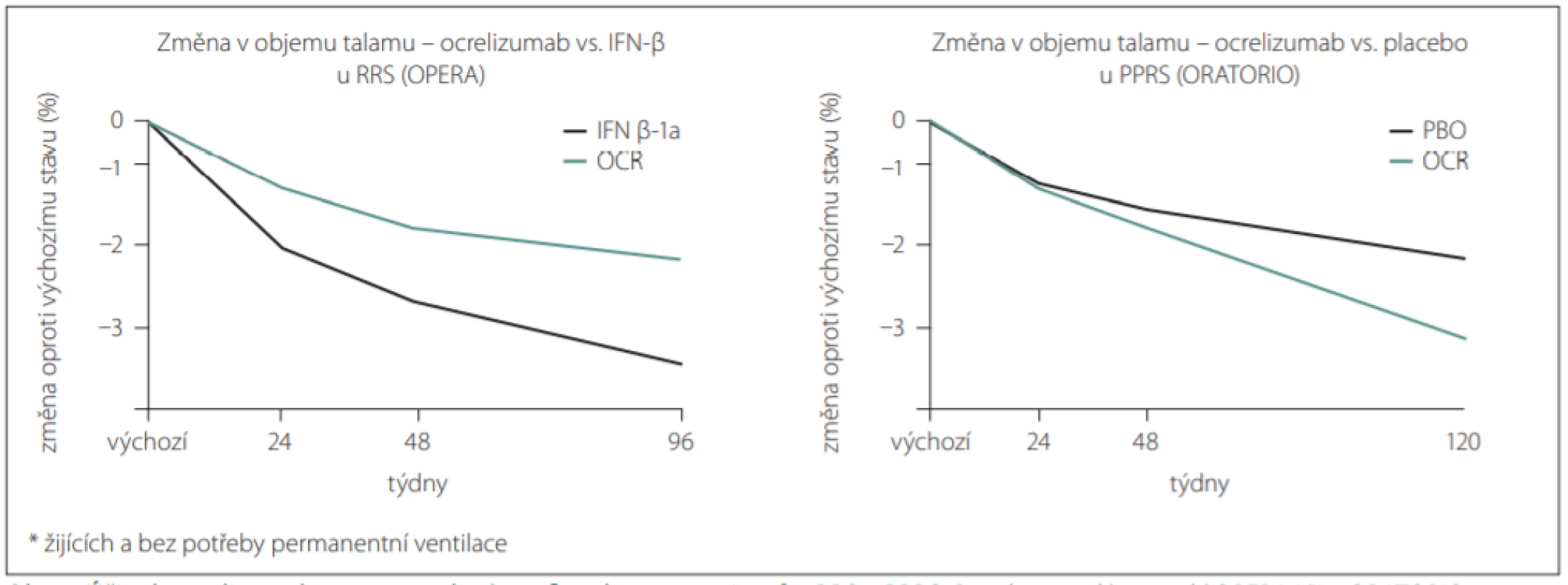
Post-hoc analysis of OPERA I/II
and ORATORIO studies.
IFN-β – interferon beta; OCR – ocrelizumab; PBO – placebo; PPMS – primary progressive MS; RMS – relapsing MS
Stejný ukazatel byl sledován i ve studii ORATORIO, která zařadila pacienty s PPRS a studovala podávání ocrelizumabu oproti placebu. Ve 48. týdnu měli pacienti užívající ocrelizumab o 18 % menší úbytek objemu talamu oproti výchozímu stavu při zařazení do studie než nemocní užívající placebo (úbytek objemu –1,06 vs. –1,29 %; p = 0,069), v 96. týdnu činil rozdíl statisticky významných 35 % (–1,67 vs. –2,59 %; p < 0,001), opět ve prospěch ocrelizumabu.
Dvě hodiny na podání infuze stačí
Ocrelizumab je standardně podáván v infuzích 600 mg v intervalu 6 měsíců (po iniciálních 2 infuzích 300 mg po 2 týdnech). Data z reálné praxe svědčí o tom, že půlroční perioda je pro pacienty dostatečně komfortní, což vede k vyšší míře jejich setrvání na léčbě.
Dr. Fontoura prezentoval data z výzkumu mezi pacienty s RS užívajícími ocrelizumab (n = 718) nebo jiné chorobu modifikující léky – infuzní (n = 208), perorální (n = 1094) nebo injekční (n = 652). Ve skupině s ocrelizumabem setrvávalo na léčbě dlouhodobě 91 % pacientů, oproti tomu bylo upravené relativní riziko přerušení léčby RS u jiných infuzních léků 2,4× vyšší, u perorálních 3,1× a u injekčních léků 4,2× vyšší.
Standardní podávání ocrelizumabu vyžaduje 3,5h infuzi (bez času potřebného pro premedikaci a sledování po aplikaci). To, zda je možné komfort pacientů ještě zlepšit a snížit zátěž, kterou délka infuze představuje pro ně i pro zdravotnické zařízení, ověřila studie ENSEMBLE PLUS. Srovnávala standardní 3,5h dobu podávání infuze ocrelizumabu s dobou zkrácenou na 2 h.
Míra výskytu reakcí spojených s infuzí (infusion-related reaction; IRR) i jejich závažnost byly u pacientů se standardní i zkrácenou dobou podání infuze plně srovnatelná. Jakékoli IRR zaznamenalo 23,1 % sledovaných pacientů při standardní době a 24,57 % při zkrácené době podání. Z toho bylo ve skupině se standardní dobou podání 15,86 % mírných a 7,24 % středně závažných IRR. Ve skupině se zkrácenou dobou podání bylo 16,26 % mírných, 7,96 % středně závažných a 0,35 % (1 pacient) závažných IRR. Na základě těchto výsledků byla podána žádost o schválení zkrácené 2h infuze ocrelizumabu americké Food and Drug Administration (FDA) i Evropské lékové agentuře.
Tento článek vyšel s podporou firmy Roche.
Ing. Šárka Spáčilová
šéfredaktorka Terapie.digital a Florence
doc. MUDr. Dana Horáková, Ph.D.
Neurologická klinika 1. LF UK a VFN v Praze
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2020 Číslo 4
-
Všechny články tohoto čísla
- Editorial
- Cytotoxické léze corpus callosum (CLOCCs)
- Poranění radiálního nervu při zlomeninách diafýzy pažní kosti
- Je jasné, kdy operovat výhřez bederní meziobratlové ploténky?
- Současná diagnostika sekundárně progresivní formy roztroušené sklerózy a léčba siponimodem
- Roztroušená skleróza – odhalené tajemství imunity
- Hygiena dýchacích cest u pacientů s Parkinsonovou nemocí – přehled problematiky a možnosti fyzioterapeutické intervence
- Klinické a sociální prediktory kvality života u dětí a mladších dospělých s poruchou autistického spektra
- Bezpečnost karotické endarterektomie s ohledem na její načasování po ischemické cévní mozkové příhodě
- Glatiramer acetát – léčba roztroušené sklerózy monitorovaná v registru ReMuS
- Intenzivní rehabilitace kognitivních funkcí u osob s roztroušenou sklerózou – výsledky 12týdenní randomizované studie hodnocené počítačovým programem
- Účinnost a bezpečnost urgentní mikrochirurgické embolektomie při selhání intravenózní trombolýzy a mechanické trombektomie u pacientů s akutním ischemickým iktem – protokol systematického review
- Vliv pandemie COVID-19 na spánkovou medicínu v České republice a na Slovensku
- Prevalence a charakteristika epilepsie u pacientů s relabující-remitující formou roztroušené sklerózy léčených imunomodulační terapií
- Syndrom moyamoya doprovázený polycystickou chorobou ledvin – kazuistika vzácného onemocnění a přehled literatury
- Souběh dvou oportunních infekcí jako první projev HIV
- Dropped head syndrom u pacientky s progredující bulbární paralýzou
- Karotický paragangliom, velmi vzácný nádor v dětském věku
- Využití kvantitativní MR venografie v indikaci stentingu stenózy žilního splavu
- Transvenózna embolizácia prasknutej piálnej arteriovenóznej malformácie
- CGRP monoklonální protilátky v léčbě migrény – indikační kritéria a terapeutická doporučení pro Českou republiku
- Recenze knih
- 2020 AAN Highlights Dlouhodobá data o účinnosti deplece CD20+ B-buněk v léčbě RS
- 2020 AAN Highlights Jak mění malá molekula průběh spinální svalové atrofie?
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Je jasné, kdy operovat výhřez bederní meziobratlové ploténky?
- CGRP monoklonální protilátky v léčbě migrény – indikační kritéria a terapeutická doporučení pro Českou republiku
- Cytotoxické léze corpus callosum (CLOCCs)
- Dropped head syndrom u pacientky s progredující bulbární paralýzou
