Subakutně probíhající reverzibilní hypertenzní leukoencefalopatie – kazuistika
Subacute Hypertensive Reversible Leukoencephalopathy – a Case Report
Hypertensive encephalopathy induced by essential or secondary arterial hypertension is characterised by a sudden onset of symptoms pointing to diffuse encephalopathy (headache, nausea, vomiting, vision problems, confusion or epileptic seizures) linked with an increase in blood pressure (BP, hypertensive crisis). In such case, the imaging methods applied, especially magnetic resonance (MR), show leukoencephalopathy. Both clinical symptoms and MR imaging findings are reversible after the blood pressure values have been normalised. We report a case of a 37-year old man who developed non-specific symptoms of encephalopathy over the period of one year (cephalea, vision disorders, behaviour changes, atactic walk). CT and MRI of the patient’s brain showed diffuse affection of the white matter of the brain, cerebellum and of the cerebral trunk. Inflammatory, demyelinisating, ischaemic, oncologic, metabolic and toxic aetiologies of leukoencephalopathy were excluded. In spite of absence of anamnestic data on arterial hypertension, and of normotensive values at admission, a hypertension crisis developed and clinical symptoms progressed into a picture of delirium. Blood pressure compensation resulted in the regression of clinical symptoms and a significant attenuation of cardiologic signs of encephalopathy, which was a confirmation of hypertensive etiology of leukoencephalopathy. Subsequently, the presence of chronic idiopathic arterial hypertension was confirmed, and secondary causes of hypertension including phaeochromocytoma were excluded. Hypertensive encephalopathy should be considered also in the case of protracted and fluctuating symptoms of encephalopathy and normal results for current blood pressure measurements.
Key words:
hypertensive encephalopathy – leukoencephalopathy
:
A. Haluzová 1; R. Jura 1; J. Bednařík 1; S. Skutilová 1; T. Andrašinová 1; M. Keřkovský 2; A. Křivanová 3
:
Neurologická klinika LF MU a FN Brno
1; Radiologická klinika LF MU a FN Brno
2; Interní kardiologická klinika LF MU a FN Brno
3
:
Cesk Slov Neurol N 2008; 71/104(6): 726-731
:
Case Report
Hypertenzní encefalopatie vzniklá na podkladě esenciální či sekundární arteriální hypertenze je onemocnění charakterizované náhlým rozvojem příznaků svědčících pro difuzní encefalopatii (bolesti hlavy, nauzea, vomitus, poruchy vizu, zmatenost či epileptické záchvaty) spojených s vzestupem hodnot krevního tlaku (TK, hypertenzní krize). Zobrazovací metody, zejména magnetická rezonance (MR), prokazují leukoencefalopatii. Klinické symptomy i zobrazovací nálezy jsou reverzibilní po normalizaci hodnot TK. Prezentujeme případ 37letého muže, u kterého se rok rozvíjely nespecifické příznaky encefalopatie (cefalea, poruchy vizu, změny chování, ataktická chůze). Počítačová tomografie (CT) i MR mozku prokázaly difuzní postižení bílé hmoty mozku, mozečku i mozkového kmene. Byla vyloučena zánětlivá, demyelinizační, ischemická, onkologická, metabolická a toxická etiologie leukoencefalopatie. Navzdory absenci anamnestických údajů o arteriální hypertenzi a normotenzním hodnotám při přijetí došlo k rozvoji hypertenzní krize a progresi klinické symptomatiky do obrazu deliria. Kompenzací hodnot krevního tlaku došlo k praktické regresi klinické symptomatiky a výraznému zmírnění radiologických známek encefalopatie, což potvrdilo hypertenzní etiologii leukoencefalopatie. Následně byla potvrzena přítomnost chronické idiopatické arteriální hypertenze a vyloučeny byly sekundární příčiny hypertenze, včetně feochromocytomu. Na hypertenzní encefalopatii je nutné pomýšlet i při protrahovaném a fluktuujícím průběhu příznaků encefalopatie a aktuálně zjištěné normotenzi.
Klíčová slova:
hypertenzní encefalopatie – leukoencefalopatie
Úvod
Průkaz difuzního postižení bílé hmoty mozkových hemisfér, mozečku a mozkového kmene pomocí zobrazovacích metod, zejména magnetické rezonance (MR) – difuzní leukoencefalopatie – představuje často svízelný diferenciálně diagnostický problém. Etiologické spektrum leukoencefalopatie je poměrně široké a zahrnuje příčiny zánětlivé, infekční, vaskulární, metabolické, postradiační, toxické, genetické a onkologické povahy [1]. Jednou z možných příčin akutní leukoencefalopatie může být i těžká arteriální hypertenze primární či sekundární etiologie, která vede k tzv. hypertenzní encefalopatii (HE). Ta v typické formě vzniká náhle, je spojena s výraznou dekompenzací arteriální hypertenze a je charakterizována souborem klinických příznaků, jako jsou bolesti hlavy, nauzea, vomitus, poruchy vizu až korová slepota, psychiatrické symptomy, kognitivní poruchy, epileptické záchvaty, poruchy vědomí [2]. Klinický obraz HE je však značně variabilní. Zejména u případů nově vzniklé arteriální hypertenze se mohou příznaky HE rozvinout i při hodnotách krevního tlaku (TK), které nejsou považovány za „maligní“. Definitivní průkaz hypertenzní etiologie přinese obvykle až reverzibilita klinické symptomatiky i leukoencefalopatie v MR obraze [1]. Pozorovali jsme případ reverzibilní leukoencefalopatie, u které vzhledem k pozvolnému rozvoji příznaků encefalopatie a normálním hodnotám TK během prvních dvou dnů hospitalizace nebyla HE původně v rámci diferenciálně diagnostické rozvahy zvažována.
Kazuistika
37letý muž přichází na vyšetření k praktickému lékaři pro jeden rok trvající intermitentní cefaleu, poruchy vizu charakteru neostrého vidění, ataktickou chůzi, zpomalení psychomotorického tempa a poruchy chování pozorované rodinou, výrazný váhový úbytek, parestezie horních končetin a obličeje. Dosud zdráv, nekuřák, abstinent. Ambulantně byla provedena počítačová tomografie (CT) mozku s nálezem splývajících hypodenzit bílé hmoty v obou mozkových hemisférách. Dále bylo provedeno vyšetření očního pozadí, kde byl zjištěn edém papil s prominencí nepřesahující jednu dioptrii. Vzhledem k těmto nálezům byl pacient přijat k dalším vyšetřením na Neurologickou kliniku FN Brno.
Při přijetí na kliniku byl pacient při vědomí, spolupracující, afebrilní, normotenzní, v objektivním neurologickém nálezu dominovala pyramidová symptomatika - hyperreflexie a pozitivní spastické pyramidové jevy v kvadrudistribuci.
Třetí den hospitalizace došlo k náhlému vzestupu krevního tlaku na hodnoty pohybující se nad 200/100 mmHg a současně ke zhoršení stavu pacienta s intermitentně vyjádřenými projevy hyperaktivního deliria. Stav byl hodnocen jako urgentní hypertenzní krize, pacient byl přeložen na semiintenzivní lůžko k pravidelnému monitorování krevního tlaku a kontinuální intravenózní antihypertenzní terapii. Vzhledem k neobjasněné etiologii byl pacient léčen antiedémovou léčbou manitolem, furosemidem a metylprednizolonem v dávce třikrát 1 000 mg.
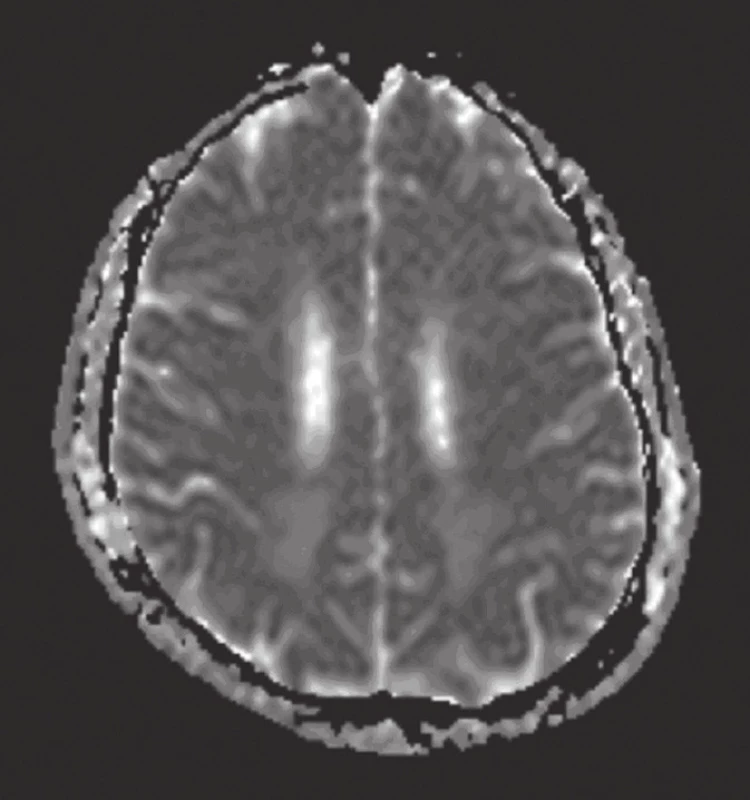
MR mozku provedená po vzestupu krevního tlaku prokázala obraz difuzní leukoencefalopatie postihující bílou hmotu mozku, mozečku i mozkového kmene (obr. 1–4).
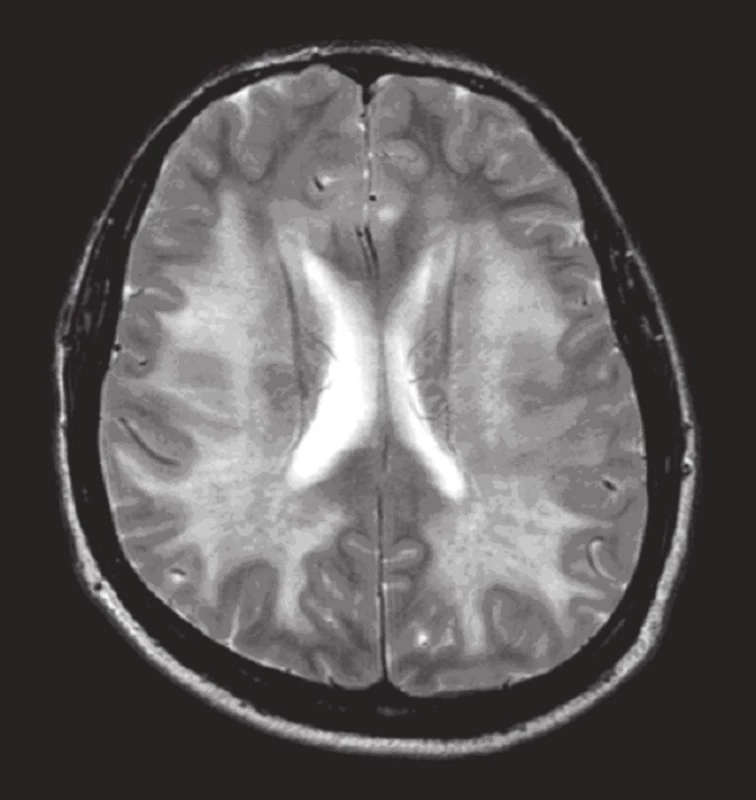
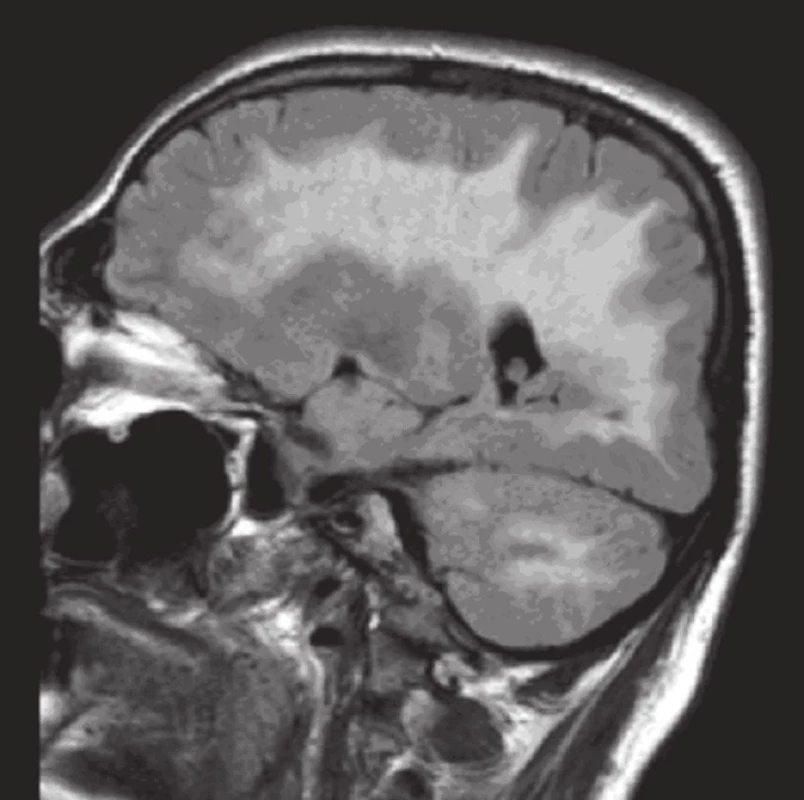
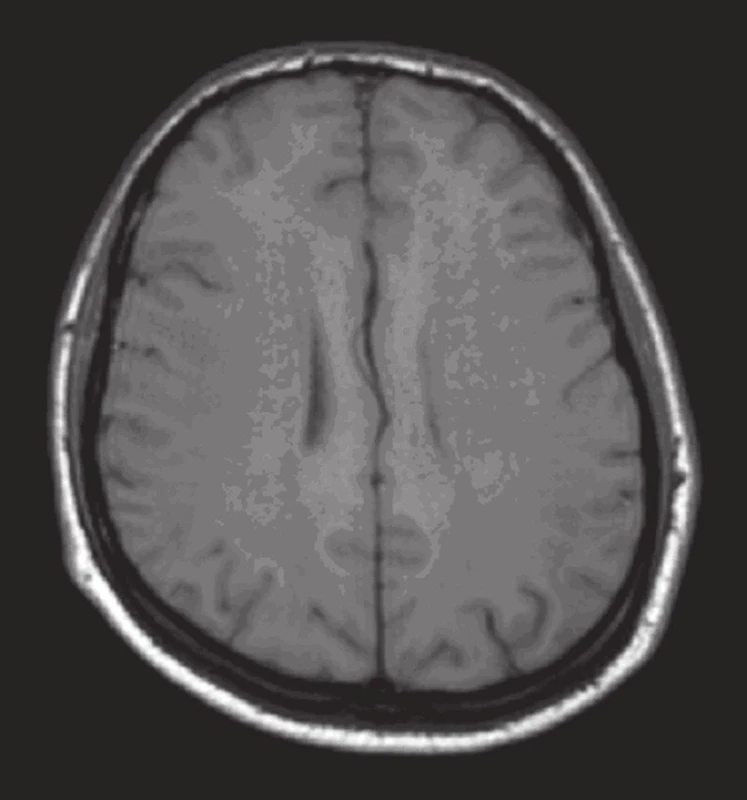
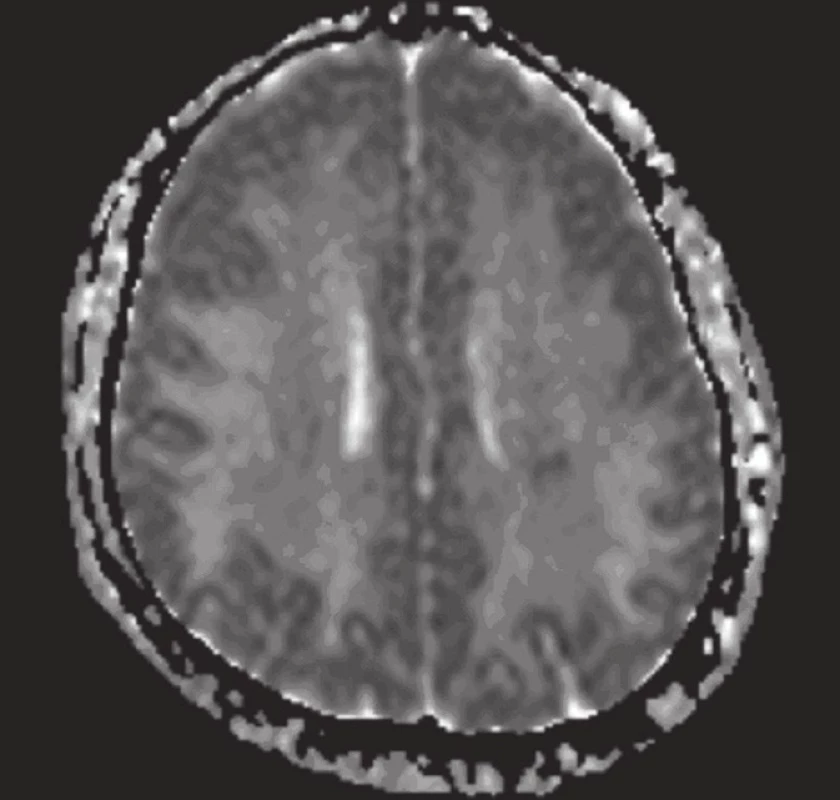
Duplexní ultrazvukové vyšetření magistrálních mozkových tepen prokázalo gracilní pravou vertebrální tepnu s redukovaným průtokem, bez nálezu aterosklerotických plátů extrakraniálně. Transkraniální barevná sonografie (TCCS) prokázala normální nález na detekovaných bazálních cerebrálních tepnách Willisova okruhu, indexy rezistence byly v normě. Hodnota na a. cerebri media vlevo byla 0,52 a vpravo 0,58 [3].
Na očním pozadí byl nález oboustranného zneostření obou papil, nepotvrzena prominence popsaná ambulantně, hodnoceno jako projev neuroretinopatie. V mozkomíšním moku byl zjištěn normální počet buněčných elementů, bez nálezu nádorových buněk, normální hladina bílkoviny, kultivace neprokázala infekční agens, oligoklonální pásy a paraneoplastické protilátky byly negativní.
Sérologickým vyšetřením byly vyloučeny borelióza, syfilis, HIV, klíšťová encefalitida, onemocnění způsobená virem Herpes simplex a parotitida. Byla zjištěna lehce zvýšená hladina TSH (4,79), hladina FT4 byla v normě.
Elektromyografie a kondukční studie neprokázaly známky periferní neuropatie či myopatie.
Skríning na leukodystrofie a autoprotilátky k vyloučení systémových vaskulitid byl negativní.
Vzhledem k uvedeným nálezům a k objevení hypertenzní krize spojené se zvýrazněním klinických známek encefalopatie byla vyslovena pracovní diagnóza hypertenzní encefalopatie, o níž se původně neuvažovalo vzhledem k déletrvajícímu průběhu a absenci historie hypertenze i normálním hodnotám TK při přijetí.
Krevní tlak byl postupně kompenzován kombinací pěti perorálních antihypertenziv. Během několika dnů po úpravě hodnot krevního tlaku ustoupily příznaky deliria, do jednoho měsíce pak i ostatní subjektivní i objektivní neurologické příznaky, jako poruchy vizu, cefalea, ataktická chůze, parestezie horních končetin a obličeje. V objektivním nálezu přetrvávala pouze lehká hyperreflexie v kvadrudistribuci. Následná vyšetření potvrdila postižení dalších orgánů svědčících pro pravděpodobnou déletrvající a neléčenou arteriální hypertenzi. Transtorakální echokardiografie prokázala významný stupeň hypertrofie stěn levé srdeční komory koncentrického typu. Na retinálních arteriích byly přítomny výrazné hypertonické změny. Byly přítomny i laboratorní známky nefropatie: mikroalbuminurie a retence dusíkatých látek.
Diagnóza hypertenzní encefalopatie byla definitivně podpořena postupným zlepšením klinického nálezu po kompenzaci hodnot krevního tlaku spolu s regresí nálezu na kontrolní magnetické rezonanci mozku provedené s odstupem jednoho měsíce (obr. 5–7) a další regresí nálezu s odstupem čtyř měsíců (obr. 8–11), jenž prokázal ústup difuzního zvýšení signálu bílé hmoty mozkové infra - i supratentoriálně.



Pátrání po etiologii arteriální hypertenze neprokázalo renální původ arteriální hypertenze (normální dopplerovský nález na renálních tepnách). Pátrali jsme i po přítomnosti feochromocytomu. Byla sice zjištěna lehce vyšší hladina chromograninu A a symetricky zvýšená kumulace v obou nadledvinkách při celotělové scintigrafii pomocí MIBG (123I metaiodinebenzyl guanidinu), avšak při dalších vyšetřeních nebyla zaznamenána nadprodukce katecholaminů či jejich metabolitů (epinefrinu a norepinefrinu) v plazmě nebo v moči/24 hod; další strukturální vyšetření (UZ břicha, CT nadledvin) byla taktéž negativní. Nebyl potvrzen primární hyperaldosteronizmus ani hyperkortizolizmus.
Výsledkem multioborové spolupráce bylo stanovení diagnózy hypertenzní encefalopatie vzniklé na podkladě těžké primární arteriální hypertenze dle WHO stupně III s orgánovým postižením u mladého pacienta.
Diskuze
Leukoencefalopatie představují poměrně heterogenní skupinu encefalopatií definovanou převážně nálezem na zobrazovacích metodách. Na CT detekujeme hypodenzní oblasti, na MR hypointenzní signál na T1 vážených obrazech, hyperintenzní změny signálu v T2 vážení a FLAIR sekvencích v oblasti bílé hmoty mozku [4]. Nálezy zobrazovacích metod stejně jako klinická symptomatika jsou nespecifické a obvykle neumožňují, ažna výjimky, bližší určení etiologické diagnózy leukoencefalopatie. Podle příčiny můžeme leukoencefalopatie rozdělit na zánětlivé, infekční a parainfekční, vaskulárně‑ischemické, metabolické, toxické, endokrinní, postiradiační, paraneoplastické a další [1]. Určitým vodítkem je rychlost rozvoje klinické symptomatiky. Mezi možné příčiny zejména akutně se rozvíjející leukoencefalopatie patří hypertenzní encefalopatie spojená s akutní elevací hodnot krevního tlaku. Jde o relativně vzácnou komplikaci arteriální hypertenze postihující < 1 % populace hypertoniků [5]. Klinický obraz se rozvíjí akutně, v průběhu hodin až dnů. Příznaky jsou nespecifické a svědčí spíše pro difuzní postižení charakteru encefalopatie: bolesti hlavy, nauzea, zvracení, zrakové poruchy (až charakteru korové slepoty či Antonova syndromu), psychické změny, apatie, dezorientace, epileptické záchvaty, kvantitativní poruchy vědomí [2]. Rozvoj HE je klasicky spojen s vzestupem hodnot krevního tlaku. Pro vzestup TK nad hodnoty 180/120 mmHg se používá termín hypertenzní krize a dělí se na urgentní (dříve akcelerovaná hypertenze) beze změny funkce některého z orgánů, a emergentní provázené dysfunkcí některého z orgánů (včetně mozku) [6]. Pro charakteristické změny na očním pozadí se používá termín hypertonická neuroretinopatie a pro vzestup tlaku spojený s neuroretinopatií termín maligní hypertenze [6].
Současný názor na patogenezi HE se opírá o selhání autoregulačního mechanizmu mozkového průtoku s dilatací arteriol, porušením hematoencefalické bariéry, otevřením těsných endoteliálních spojení, mozkovou hyperperfuzí a následným vazogenním edémem mozku. Tato představa nahradila dřívější hypotézu vysvětlující rozvoj HE vazospazmy, i když jsou popsány případy encefalopatií s obdobným obrazem jako u HE s angiografickým průkazem difuzních vazospazmů [7].
V roce 1996 popsali Hinchey et al variantu HE s predilekčním postižením bílé hmoty v zadní části hemisfér okcipito-parieto-temporálně – Posterior Reversible Encephalopathy Syndrome (PRES) [8]. Následně byla publikována řada souborů pacientů s tímto obrazem [4,9]. Byly popsány i případy s izolovaným postižením mozkového kmene [10] vedoucí až k obstrukčnímu hydrocefalu [11], a dokonce i postižení míchy [12]. Převažující postižení v oblasti zadní cirkulace dokládá i práce Weingartena et al, jejichž série 36 nemocných zaznamenala ve 42 % (15/36) kmenovou lézi a ve 30 % (11/36) mozečkovou lézi [13]. Možným vysvětlením je fakt, že tepny přední mozkové cirkulace jsou bohatě inervovány sympatickými nervy, které stimulují vazokonstrikci a poskytují nemocným s akutní arteriální hypertenzí protekci před hyperperfuzí. Vertebrobazilární arterie mají relativně méně sympatické inervace, což činí zadní mozkovou cirkulaci náchylnější k vazogennímu edému [14].
PRES byl však popsán i u řady případů bez vzestupu TK, zejména po podání některých léků: cyklosporinu, tacrolimu, interferonu alfa, fludarabinu, cisplatiny, gemcitabinu, erytropoetinu, ifosfamidu, a dále u některých stavů: akutní intermitentní porfyrie, HIV, trombotické trombocytopenické purpury, hepatorenálního syndromu, sepse, po krevní transfuzi [15]. Předpokládá se podíl poruchy hematoencefalické bariéry v důsledku toxického postižení endotelu.
V případě našeho nemocného jsme na hypertenzní příčinu encefalopatie zpočátku nemysleli, jelikož se jednalo o mladého muže, který dosud netrpěl arteriální hypertenzí a navíc příznaky encefalopatie byly přítomny již celý rok. Ani při přijetí či v několika prvních dnech hospitalizace nebyly hodnoty krevního tlaku zvýšené. Až v dalším průběhu došlo k dekompenzaci krevního tlaku s přechodnou nutností podávat vysoké dávky antihypertenziv, včetně infuzní aplikace.
Proto jsme v úvodu nejprve postupně provedenými pomocnými vyšetřeními vyloučili zánětlivé postižení (akutní diseminovaná encefalomyelitida či rhombencefalitida), tumorózní proces, systémové onemocnění včetně vaskulitidy, demyelinizaci, trombózu venózních splavů, adrenoleukodystrofie. Vzhledem k rozvoji dekompenzace krevního tlaku, následně zjištěným známkám pravděpodobné neléčené arteriální hypertenze (hypertrofii levé srdeční komory, hypertonickým změnám na očním pozadí, počínající nefropatie) a velmi dobré klinické odezvě na podávání antihypertenzní medikace spolu s regresí známek encefalopatie v MR obraze byla stanovena diagnóza pravděpodobné HE.
Ačkoliv elevace TK nad normu je u HE obvyklá a často splňuje kritéria hypertenzní krize, mohou se HE či PRES rozvinout zejména u nemocného s čerstvě vzniklou arteriální hypertenzí i při hodnotách TK, které nejsou obvykle považovány za maligní. U našeho nemocného však šlo o neobvyklý průběh onemocnění, kdy se klinické známky leukoencefalopatie zjištěné na MR rozvíjely subakutně až chronicky (dle anamnézy minimálně jeden rok) a nebyly zaznamenány zvýšené hodnoty TK jak během tohoto období, tak první dva dny hospitalizace. Lze spekulovat o tom, zda k vzestupu TK spojenému s rozvojem encefalopatie nedocházelo epizodicky a tyto epizody unikly pozornosti. Z tohoto důvodu by se nabízela zejména možnost feochromocytomu charakteristická paroxysmy arteriální hypertenze s normotenzí mezi paroxysmy [15]. U našeho nemocného byla zaznamenána lehce vyšší hladina chromograninu Aa symetricky zvýšená kumulace v obou nadledvinkách při celotělové scintigrafii pomocí MIBG. Při dalších vyšetřeních však nebyla zaznamenána nadprodukce katecholaminů či jejich metabolitů (epinefrinu a norepinefrinu) v plazmě nebo v moči/24 hod a další strukturální vyšetření (UZ břicha, CT nadledvin) byla taktéž negativní. V případě popsané scintigrafie šlo zřejmě o chybnou interpretaci vyšetření a pravděpodobná falešná pozitivita chromograninu A v séru byla pravděpodobně způsobena léčbou kortikosteroidy, které nemocný zpočátku dostával v rámci antiedémové terapie.
Alternativně jsme zvažovali PRES vyskytující se příležitostně i u normotoniků (opakovaný MR nález ukazuje predilekci postižení okcipitálně a v oblasti kmene a mozečku). Nebyla však zjištěna aplikace potenciální toxické medikace, ani přítomnost stavů popisovaných v souvislosti s PRES [4].
Vzhledem k prevalenci postižení v zadních (okcipito-parieto-temporálních) oblastech hemisfér, mozkového kmene a mozečku u PRES je třeba v některých případech odlišit ischemii ve vertebrobazilárním povodí včetně aa. cerebri posteriores, kde mohou pomoci novější MR modality: difuzí vážené obrazy (Diffusion Weighted Image – DWI) a ADC (Apparent Diffusion Coefficient) mapy: na rozdíl od hyperintenzit v DWI a hypointenzit v ADC se u HE nachází izo - či hypoinzitenzity v DWI a hyperintenzity v ADC mapách [16]. Tato diferenciace je zásadní i vzhledem k léčbě HE/PRES, kterou je razantní normalizace krevního tlaku, přičemž u ischemie by tento postup mohl vést k prohloubení klinického deficitu.
Závěr
Na HE je nutno pomýšlet nejen u všech nemocných s akutně vzniklou nespecifickou encefalopatickou symptomatikou, nálezem leukoencefalopatie na MR a současně zjištěnou hypertenzní krizí, ale i u jedinců s aktuální normotenzí a protrahovaným a fluktuujícím průběhem klinické symptomatiky a MR známek leukoencefalopatie, dle literatury pak i u nemocných s lokalizovaným postižením bílé hmoty v oblasti zadní mozkové cirkulace.
MUDr. Adéla Haluzová
Neurologická klinika
LF MU a FN Brno
Jihlavská 20
602 00 Brno
e‑mail: adela.haluzova@email.cz
Přijato k recenzi: 30. 4. 2008
Přijato do tisku: 8. 9. 2008
Sources
1. Lisá I, Lisý Ľ. Akútne leukoencefalopatie – diferenciálna diagnostika. Neurol pro praxi 2007; 8(2): 90–94.
2. Herzig R. Neurologické komplikace arteriální hypertenze. Interní Med 2003; 5 : 11–15.
3. Václavík D, Školoudík D. Diagnostika postižení drobných mozkových tepen pomocí barevné transkraniální sonografie hodnocením rezistenčního indexu. Cesk Slov Neurol N 2004, 67/100(2): 99–103.
4. Mizra A. Posterior reversible encephalopathy syndrome: a variant of hypertensive encephalopathy. J Clin Neurosci 2006; 13 : 590–595.
5. Williams GH. Hypertensive vascular disease. In: Braunwald E, Fauci AS, Kasper DL, Hauser, SL, Longo, DL, Jameson JL (eds). Harrison’s Principles of Internal Medicine. New York: McGraw-Hill 2001 : 1428–1429.
6. Ambler Z, Bauer J. Cévní onemocnění mozku. In: Bednařík J, Ambler Z, Růžička E (eds). Klinická neurologie – část speciální. Praha: Triton 2008. In press.
7. Ducros A, Boukobza M, Porcher R, Sarov M, Valade D, Bousser MG. The clinical and radiological spectrum of reversible cerebral vasoconstriction syndrome. A prospective series of 67 patients. Brain 2007; 130(12): 3091–3101.
8. Hinchey J, Chaves C, Appignani B, Breen J, Pao L, Wang A et al. A reversible posterior leukoencephalopathy syndrome. N Engl J Med 1996; 334(8): 494–500.
9. Garg RK. Posterior leukoencefalopathy syndrome. Postgrad Med J 2001; 77(903): 24–28.
10. Thambisetty M, Biousse V, Newman NJ. Hypertensive brainstem encephalopathy: clinical and radiographic features. J Neurol Sci 2003; 208(1–2): 93–99.
11. Lee SY, Dinesh SK, Thomas J. Hypertension‑induced reversible posterior leukoencephalopathy syndrome causing obstructive hydrocephalus. J Clin Neurosci 2008; 15(4): 457–459.
12. Milia A, Moller J, Pilia G, Mascia MG, Marchi P, Mura M et al. Spinal cord involvement during hypertensive encephalopathy: clinical and radiological findings. J Neurol 2008; 255(1): 142–143.
13. Weingarten K, Barbut D, Filippi C, Zimmerman RD. Acute hypertensive encephalopathy: findings on spin‑echo and gradient-echo MR imaging. AJR Am J Roentgenol 1994;162(3): 665–670.
14. Donnan GA. Posterior leucoencephalopathy syndrome. Lancet 1996; 347(9007): 988.
15. Manger WM. An overview of pheochromocytoma: history, current concepts, vagaries, and diagnostic challenges. Ann NY Acad Sci 2006; 1073 : 1–20.
16. Ay H, Buonanno FS, Schaefer PW, Le DA, Wang B, Gonzalez RG et al. Posterior leucoencephalopathy without severe hypertension: utility of diffusion-weighted MRI. Neurology 1998; 51(5): 1369–1376.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2008 Issue 6
-
All articles in this issue
- Adult Age Sleep Apnoea
- Brain Tissue Oxygen Monitoring
- Multiple Sclerosis and Magnetic Resonance Imaging: Present Status and New Trends
- The Relation between Amygdala Atrophy and Other Selected Brain Structures and Emotional Agnosia in Alzheimer Disease
- Pharmacoepidemiological Study of 427 Patients with Epilepsy
- Protein 14-3-3 Detection in Cerebrospinal Fluid – Clinico-Pathological Correlation
- Cubital Tunnel Syndrome. Comparison of Surgical Methods of Simple Decompression and Anterior Transposition of the Ulnar Nerve
- Endonasal Endoscopic Transsphenoidal Technique of Sellar Lesions Resection
- Anterior Cervical Microforaminotomy in the Treatment of Unilateral Monosegmental Radiculopathy (a Prospective Pilot Study Involving 15 Patients)
- Extraoperative Mapping by Means of Cortical Grid before Resection of Diffuse Oligodendroglioma in Dominant Hemisphere – an Alternative of “Awake Craniotomy” – a Case Report
- Absence Status in Geriatric Patient with Recent Diagnosis of Idiopathic Generalised Epilepsy – a Case Report
- Subacute Hypertensive Reversible Leukoencephalopathy – a Case Report
- Gender Differences in the CAG Repeats and Clinical Picture Correlations in Huntington’s Disease
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Multiple Sclerosis and Magnetic Resonance Imaging: Present Status and New Trends
- Adult Age Sleep Apnoea
- Subacute Hypertensive Reversible Leukoencephalopathy – a Case Report
- Protein 14-3-3 Detection in Cerebrospinal Fluid – Clinico-Pathological Correlation





