Degenerace krční meziobratlové ploténky – indikace a možnosti chirurgické léčby
Cervical Intervertebral Disc Degeneration – Surgical Treatment Indications and Options
There are a growing number of patients presenting with complaints related to pain in the cervical spine. In order to discover the underlying causes, both the acquired clinical knowledge and a number of modern examination methods are utilised. Usually, the cause resides in a degenerative disease, and if the patient is not affected by a significant or progressing neurological deficit, conservative therapy should be applied. In the opposite case, or if conservative therapy proves ineffective, surgery is considered as a therapeutic option. The objective of the overview article is to describe pathological conditions related to cervical intervertebral disc degeneration, to systematize their morphological diagnosis and to provide the reader with clear guidelines for the selection of patients who could benefit from surgical intervention. The subsequent section pursues the objective of describing, in simple terms, current methods of surgical treatment of cervical intervertebral space. Each of the procedures described therein has its strong and weak points. None of the methods described is endorsed by the necessary body of evidence in relevant literature and similar results can be expected from the application of any one of them. However, the basic prerequisites are correct indication based on the harmony of clinical and morphological findings and excellence of surgical technique. Of equal importance is long-term follow-up of patients and standardized evaluation of the results of the surgeons' efforts. The doctor sending his or her patient for surgery should always know what the results of the surgery team have been, and should be in permanent contact with them. Experience in performing similar procedures and adequate equipment of the centre should be another criterion for successful cooperation. The Czech Spine Surgery Society JEP monitors on a long-term basis the parametres of the different spine surgery centres and classifies their performance. For better orientation among spine surgery centres, the referring neurologist, orthopaedist or rehabilitation specialist can use the database of approved spine surgery centres published at www.spine.cz on an annual basis.
Key words:
cervical spine – degenerative disease – cervical spine surgery – discectomy
Autoři:
P. Suchomel
Působiště autorů:
Neurochirurgické oddělení, Neurocentrum, Krajská nemocnice Liberec a. s.
Vyšlo v časopise:
Cesk Slov Neurol N 2008; 71/104(3): 246-261
Kategorie:
Minimonografie
Souhrn
V praxi se stále častěji setkáváme s nemocnými, jejichž obtíže souvisejí s bolestmi v krční páteři. K odhalení příčiny využíváme nejen našich klinických zkušeností, ale i celé řady moderních vyšetřovacích metod. Příčinou je obvykle degenerativní onemocnění, a pokud není nemocný stižen významným nebo progredujícím neurologickým deficitem, je na místě konzervativní terapie. V opačném případě nebo při neúspěchu konzervativních postupů uvažujeme o možnostech chirurgického řešení. Překládaný přehled si klade za cíl popsat patologické stavy související s degenerací krční meziobratlové ploténky, utřídit jejich morfologickou diagnostiku a dát čtenáři srozumitelný návod, jak postupovat při výběru kandidátů, kteří by mohli profitovat z chirurgické intervence. Další text je pak veden snahou pokud možno jednoduše popsat současné metody chirurgického ošetření krčního meziobratlového prostoru. Každý z popsaných postupů má své výhody a nevýhody. Pro žádnou z popsaných metod není v literatuře dostatečná důkazní opora, a tak je dosud možné použít všechny s očekáváním obdobných výsledků. Podmínkou je ale správná indikace plynoucí z harmonie klinického a morfologického nálezu a kvalitní technické provedení operace. Neméně důležité je i dlouhodobé sledování léčených a standardizované hodnocení výsledků chirurgického úsilí. Lékař odesílající nemocného k operaci by vždy měl znát výsledky operujícího týmu a být s ním v trvalém kontaktu. Zkušenost s prováděním podobných výkonů, stejně jako adekvátní vybavení pracoviště, by měly být dalším kritériem úspěšné spolupráce. Česká spondylochirurgická společnost JEP dlouhodobě sleduje parametry jednotlivých spondylochirurgických pracovišť a jejich výkonnost kategorizuje. K orientaci mezi spondylochirurgickými pracovišti může referující neurolog, ortoped či rehabilitační specialista užít databáze společností garantovaných pracovišť, jež je každoročně zveřejňována na www.spine.cz.
Klíčová slova:
krční páteř – degenerativní postižení – chirurgie krční páteře – diskektomie
Úvod
S prodlužující se délkou života a změnou životního stylu se v denní praxi stále častěji setkáváme s nemocnými, jejichž hlavními obtížemi jsou bolesti krční páteře, související kořenová bolest horních končetin, hlavy či vegetativní symptomy spojené s pohybem krku. Vesměs se jedná o pacienty s degenerativním postižením krční páteře. Moderní diagnostické metody, zvláště zobrazení magnetickou rezonancí (MRI) odhalují degenerativní postižení meziobratlové ploténky často dříve, než je běžné doposud. Rozhodnutí, zda má být pacient léčen konzervativně, či by mohl profitovat z chirurgické léčby, se tak stává složitějším. Často máme tendenci indikovat k agresivní léčbě pouze grafické zobrazení patologie a ne individuální pacienty s harmonickým souladem klinických obtíží a morfologického obrazu. Mnohdy naší indikaci ani nepředchází kvalitní konzervativní léčba přesto, že nález chirurgickou urgenci nepředstavuje. Také v případě, kdy je chirurgická intervence indikována, panuje celá řada nejasností, který způsob operace by mohl být pro daného jedince přínosný. Naši pacienti tak obvykle nemají jasnou představu, která z nabízených léčebných modalit by jim mohla pomoci. Pokud nemocné zahltíme rozdílnými nebo dokonce i protichůdnými informacemi, můžeme v extrémním případě ztratit jejich důvěru. Tito pacienti pak nezřídka končí v kategorii psychosomatických onemocnění a ani finálně správný postup nevede k úplnému uzdravení.
Cílem předloženého shrnutí je informovat zejména referující lékaře – neurology, fyzioterapeuty, rehabilitační lékaře a ortopedy o současných diagnostických možnostech a souvislostech z toho plynoucích pro indikaci a zejména metodu chirurgické intervence u nemocných s degenerativním postižením ploténky krční páteře (CDDD – Cervical Degenerative Disc Disease) – tedy postižením limitovaným na meziobratlový prostor.
Etiopatogeneze degenerativního onemocnění krční páteře
Degenerace disku
Degenerace meziobratlové ploténky je v literatuře považována za startující moment degenerace pohybového segmentu [1]. Proces stárnutí ploténky je dobře popsán pro bederní disk [2,3], nicméně stejný charakter změn lze předpokládat na všech úrovních páteře, tedy i v krční oblasti. Degenerace ploténky začíná na biochemické a celulární úrovni neschopností produkovat adekvátní množství extracelulární hmoty normálního složení. V normálním disku je zajištěna rovnováha mezi produkcí a degradací této matrix. Simultánně dochází i ke zvyšování hladiny kolagen degradujících enzymů – proteáz. Jedním z rozhodujících faktorů spouštějících degradaci extracelulární matrix disku je pravděpodobně omezení výživy buněk tuto hmotu tvořících. Je prokázáno, že hlavní nutriční cestou je průnik důležitých substancí z disku přilehlých krycích lišt – „endplate“ [4].
Změny v krevním zásobovaní těchto lišt jsou popisovány již v druhém deceniu života jedince [1]. První změny při degeneraci či stárnutí disku jsou pozorovány v nucleus pulposus, ve kterém dochází ke zvýšení hladiny kolagenu, a tak se postupně stírá rozdíl mezi charakterem hmoty nukleu a anulu. Dochází k radiálním trhlinám v anulu. V dané situaci může i malá neadekvátní zátěž způsobit výhřez středových hmot disku přes poškozený anulus. Chronicky se postupná ztráta vody, proteoglykanů a snížení produkce kolagenu projeví snížením disku. Tyto morfologické změny již lze detekovat na magnetické rezonanci a byla také vytvořena 5stupňová klasifikace těchto změn [1]. Za předchozích podmínek je možné, aby se původně avaskulární disk (normálně se vyskytují cévy řídce pouze po obvodu anulu) měnil v důsledku infiltrace a neovaskularizace, ne nepodobné zánětu, ve strukturu obsahující nervově cévní svazečky. Trhlinami mohou pronikat i nociceptivní nervová vlákna [2,5], a tím je vysvětlena i tzv. diskogenní bolest [6].
Snížení disku, ztráta vody a poškození elasticity mají vážné biomechanické důsledky na další struktury pohybového segmentu, zejména na intervertebrální klouby.
Degenerace intervertebrálních kloubů
Meziobratlové klouby jsou jedinými pravými synoviálními klouby páteře. Zatímco disk nese tíhu vpředu, klouby nesou asi 2/5 tíhy vzadu a navíc stabilizují páteř zejména ve flexi, extenzi a chrání disk před extrémní rotací. Je všeobecně přijímáno, že degenerace kloubů následuje po postižení disku. Snížením disku dochází k inkongruenci kloubních ploch a vlastně k subluxačnímu přetížení kloubních chrupavek. Následná eroze povrchu a degradace chrupavek mají stejné důsledky jako artróza jiných kloubů včetně možné nestability. Deformace kloubů s remodelací subchondrální kosti je pak vyvrcholením tohoto procesu. Hypertrofické klouby se často podílejí na vzniku laterální stenózy páteřního kanálu. Je zřejmé, že přitom dochází k napínání a často i k destrukci nervově zásobených kloubních pouzder, nicméně takto vzniklá bolest či tzv. facetální syndrom jako izolovaná jednotka jsou dosud předmětem diskuse.
Degenerace ligament a svalů
Ligamenta jsou významným prvkem stability páteře proto, že limitují pohyb v jednotlivých segmentech. Vazy páteře mají většinou vysoký obsah kolagenu. Pouze žlutý vaz rozepjatý mezi oblouky má vyšší obsah elastinu, který umožňuje natažení ligamenta ve flexi a kontrakci v extenzi. Degenerací či přibývajícím věkem ve vazech přibývá kolagenu, a tak zejména podélné dlouhé vazy dystrofují a jejich stabilizační funkce se zhoršuje. Ligamenta flava naopak zesilují a často se stávají částí struktur dorzálně zužujících kanál páteřní.
Degenerativní změny kostí
Kost je statickou složkou páteře. K degenerativním změnám v kostech dochází až sekundárně. Jedná se obvykle o přestavbu ve smyslu pozitivním - osteofyty. Přestavba ve smyslu negativním – poróza - spíše souvisí se stárnutím a metabolickými změnami.
Degenerace svalstva
Svaly jsou jedinou složkou statodynamického aparátu páteře, která nemusí podléhat degeneraci souvisle s předchozími. Svalová aktivita je to jediné, čím předchozími změnami postižený jedinec může zpomalovat progresi degenerativních změn. Necvičené svaly ale na druhé straně přispívají k urychlování negativního vývoje. Podobný efekt mohou mít i některá svalová onemocnění.
Klinické syndromy vyplývající z degenerativního postižení ploténky krční páteře
Radikulopatie
Nervový kořen vychází z páteře skrze foramen intervertebrale. Jeho útlak přímo v tomto otvoru, ale i těsně před a za ním, způsobuje klinickou symptomatologii typickou pro daný kořen. Poškození může být způsobeno mechanickým neměnným tlakem, dynamicky se měnící kompresí, ale i omezením krevního zásobení. Klinicky se tento jev odehrává ve 2 rovinách – neuropatická bolest a výpad kořenové funkce.
Senzitivní či motorický výpad funkce nervového kořene považujeme obvykle za alarmující situaci směřující k operační indikaci. V případě dokončené zkázy nervového kořene sice ustává bolest, ale také vzniká nevratný výpad funkce.
Mícha má v krční oblasti 8 segmentů a tudíž je pro lokalizaci útlaku kořenů nutná znalost vertebro-medulární topografie. Kořen C1 vychází mezi lebkou a obratlem C1, takže v nejčastěji postiženém úseku C5/6 opouští páteř kořen C6.
Myelopatie
Mícha je zejména v oblasti krční intumescence velmi náchylná reagovat na zmenšený prostor páteřního kanálu (za hraniční šíři se obvykle považuje 14 mm). Dosud není zcela prokázáno, zda v etiologii krční myelopatie má dominantní úlohu prostá komprese míšní tkáně či omezení krevního zásobení. S největší pravděpodobností jsou míšní výpady způsobeny kombinací obou předchozích složek. Etiologicky je většina myelopatií způsobena osteodegenerativním onemocněním. V literatuře se dokonce uvádí, že cervikální spondylogenní myelopatie je nejčastější formou poškození míchy u jedinců starších 15 let [7,8].
V hodnocení závažnosti klinického obrazu myelopatie dnes již nevystačíme s popisným neurologickým závěrem, ale užíváme objektivnější škály. Nejčastěji v literatuře užívaná JOA škála (Japanese Orthopedic Association Scale) je mimo asijské země obtížně interpretovatelná, protože k hodnocení jemné motoriky rukou užívá schopnost ovládat jídelní hůlky. V našich podmínkách lze užít její různé modifikace, kde je předchozí problém řešen např. schopností pacienta jíst příborem, psát či si zapnout knoflíčky u košile [9,10].
Kombinace radikulo/myelopatie
Poměrně často, zejména u výhřezů, které jsou lokalizovány mediálně nebo paramediálně, ale i v případě tlaku v těchto oblastech způsobeného kostními změnami, nacházíme pacienty s kombinacemi radikulopatie a myelopatie.
Ostatní
V poslední době se v literatuře stále častěji objevují zprávy dokumentující úspěch chirurgické intervence u pacientů s bolestmi v oblasti krční páteře [11–13] bez projevů radikulo/myelopatie. Tyto bolesti se obvykle zvýrazňují po zátěži, a to častěji po statickém jednostranném axiálním zatížení než po dynamickém přetížení. Stejně tak se k operacím indikují dnes i pacienti s cervikogenní bolestí hlavy [14,15] nebo závratěmi či jinými příznaky zvýšeného tonu sympatiku [16]. K fúzním operacím jsou také indikováni nemocní s prevalentním klinickým postižením meziobratlových kloubů krční páteře [17].
Předchozí symptomy nebo jejich kombinace mohou vést až k velmi složitým indikačním rozvahám, při kterých si mnohdy i přes dokonale dokumentovaný klinický obraz a grafická vyšetření nejsme jisti, zda má být pacient operován, či konzervativně léčen.
Grafické vyšetřovací metody – morfologický korelát CDDD
Degenerativní změny na krční páteři bez korespondující klinické symptomatologie jsou graficky detekovatelné více než u poloviny populace v 5. deceniu [18].
Nativní RTG vyšetření
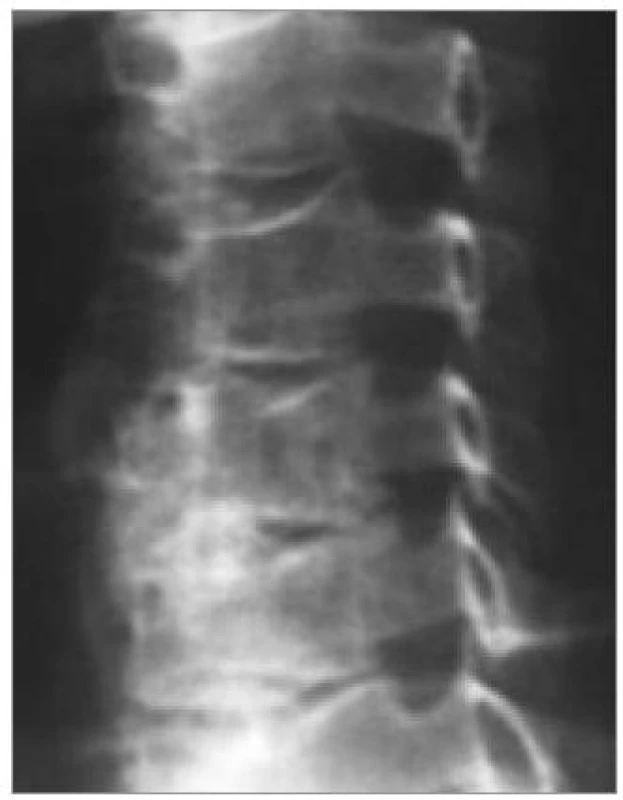
Je standardně prováděno v předozadní a bočné projekci (obr. 1). Podmínkou kvalitního zhodnocení není pouze grafická kvalita, ale i zachycení celé krční páteře až po cerviko-torakální přechod.

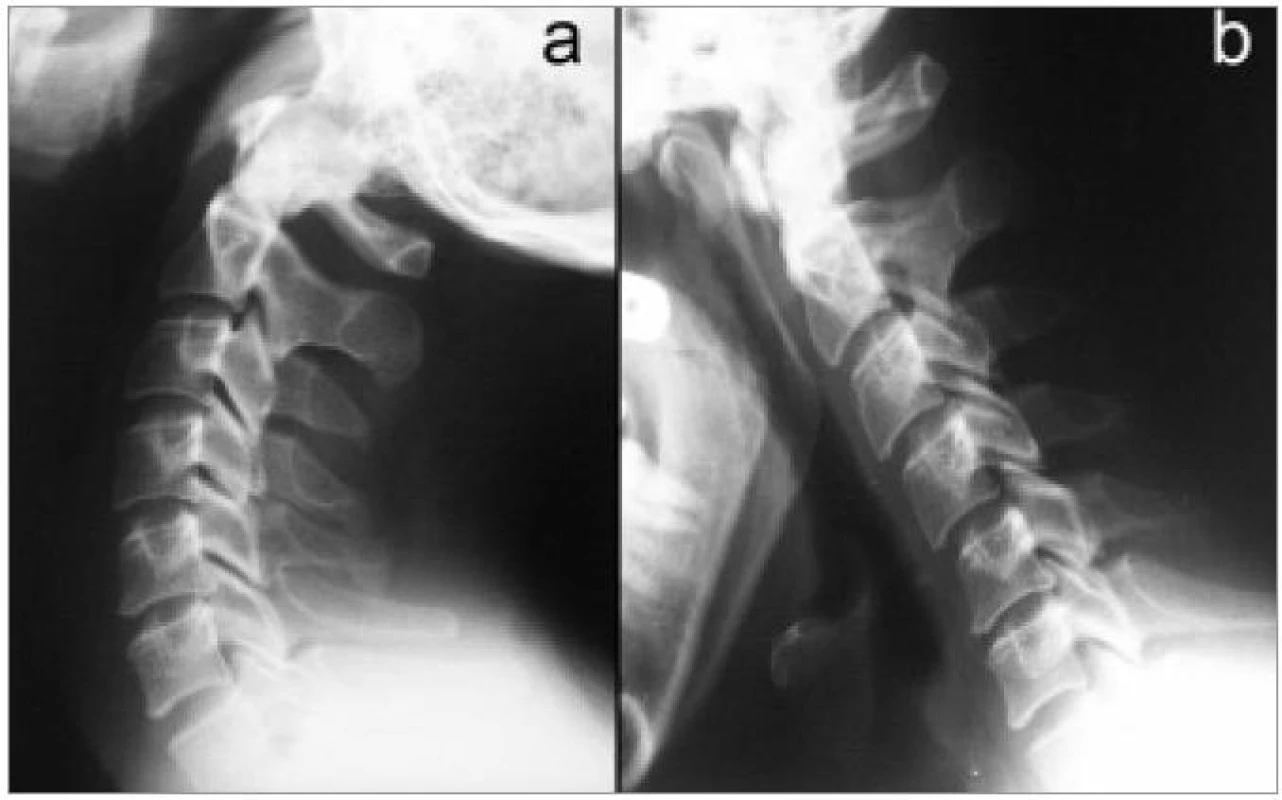
V některých případech, zejména pokud neplánujeme další metody, je prováděno vyšetření v šikmých projekcích k zobrazení foramin a kloubů (obr. 2) a v poslední době stále častěji i dynamické vyšetření v maximální aktivní flexi a extenzi (obr. 3). Z nativního zobrazení můžeme vyhodnotit tvar krční páteře v příslušných rovinách, snížení meziobratlového prostoru, kostní změny na kloubech a obratlových koncových lištách, unkovertebrální neoartrózy atd. Nativní vyšetření je také důležité při záchytu destruktivních lézí. Všichni pacienti by toto vyšetření měli podstoupit jako základní.
Perimyelografie
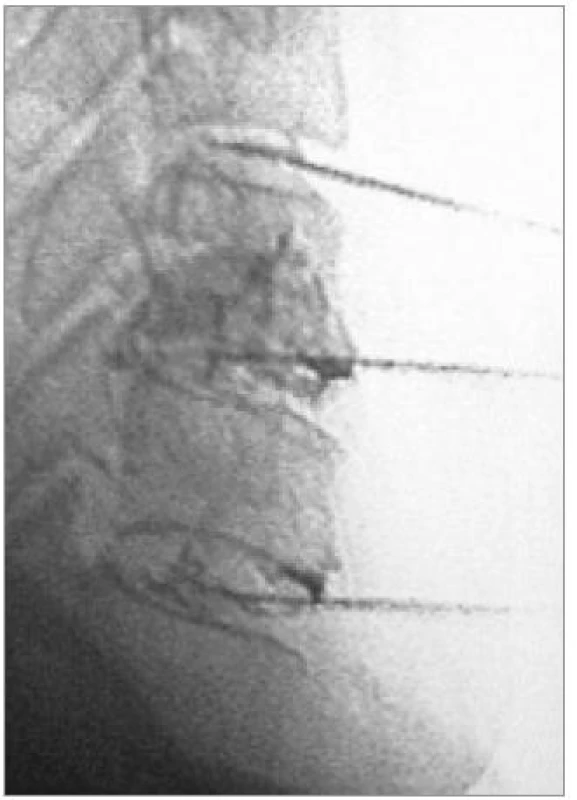
Perimyelografii dnes v diagnostice degenerativních onemocnění krční páteře používáme výjimečně (obr. 4). Zejména v případech, ve kterých nelze použít vyšetření magnetickou rezonancí (pacient má kardiostimulátor apod), má toto invazivní vyšetření své opodstatnění.
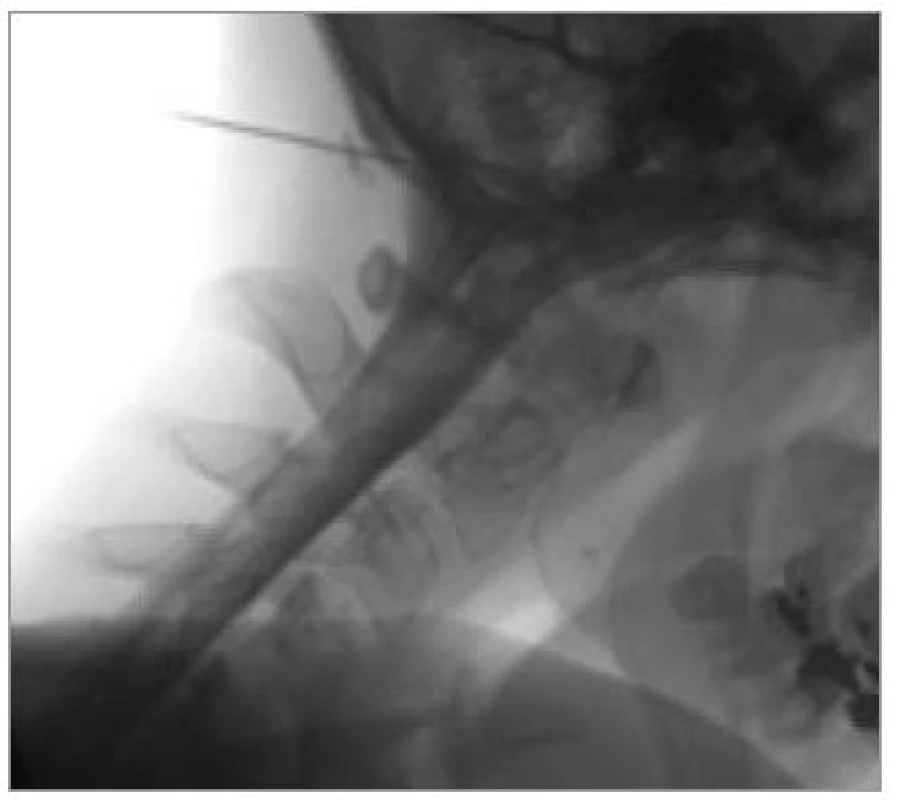
Invazivitu perimyelografie lze také snížit lumbální aplikací kontrastní látky a následným CT-vyšetřením – pak hovoříme o CT-perimyelografii.
Indikací může být někdy i víceetážová stenóza kanálu páteřního nebo významná deformita, u které není ani po provedení MRI zřejmé, zda je rozhodující útlak subarachnoidálního prostoru lokalizován zpředu či zezadu, což je zásadní pro stanovení chirurgického postupu. Kontrastní vyšetření je také vhodné v případě přítomnosti kovových implantátů, které při zobrazení počítačovými metodami tvoří artefakty.
Počítačová tomografie (CT)
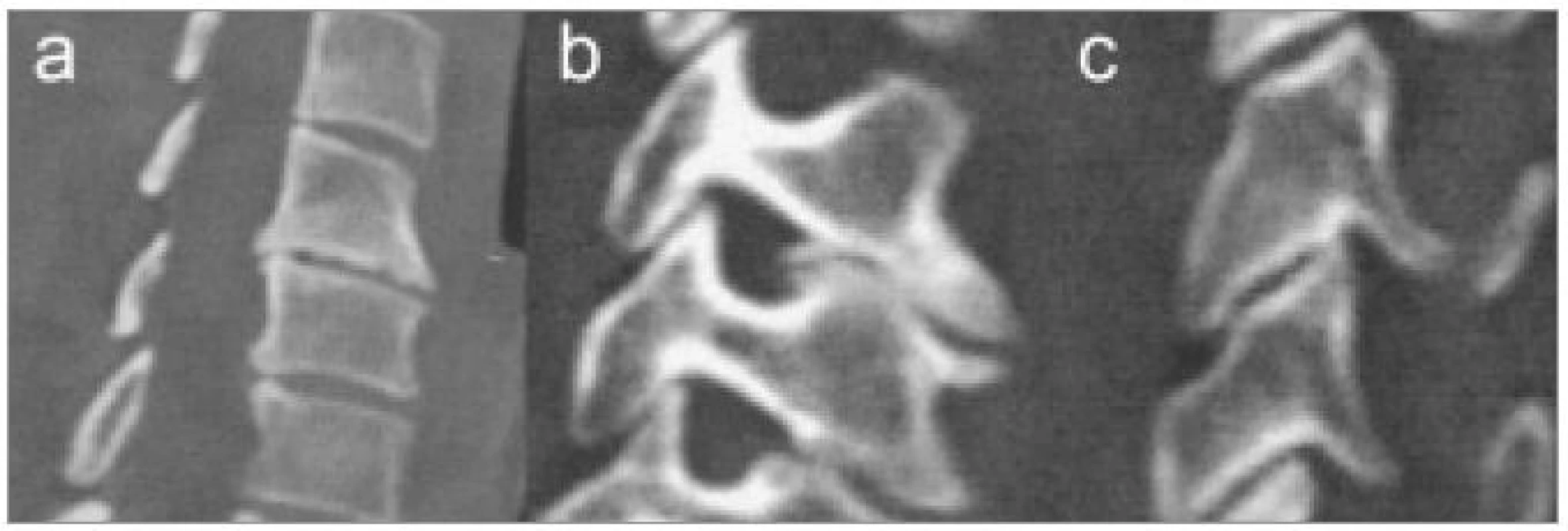
Počítačová tomografie je stále velmi často užívanou metodou zejména v menších nemocnicích. Je snadno dostupná. V případě CDDD je však její význam omezen a také představuje pro pacienta zbytečnou radiační zátěž. V současné době ji za rutinní předoperační vyšetření rozhodně nepovažujeme. CT indikujeme pouze, pokud je žádoucí zobrazit útlak způsobený kostí či kalcifikacemi. Příkladem mohou být kalcifikace v zadním podélném vazu nebo osteofyty zúžené foramen intervertebrale (obr. 5,6).
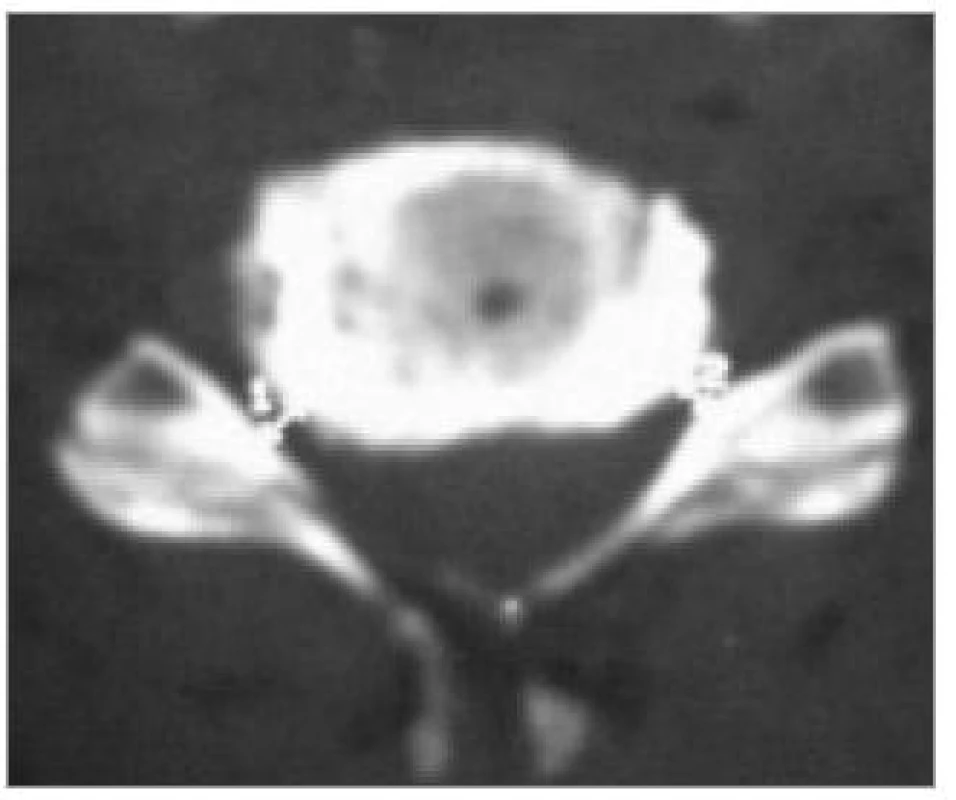
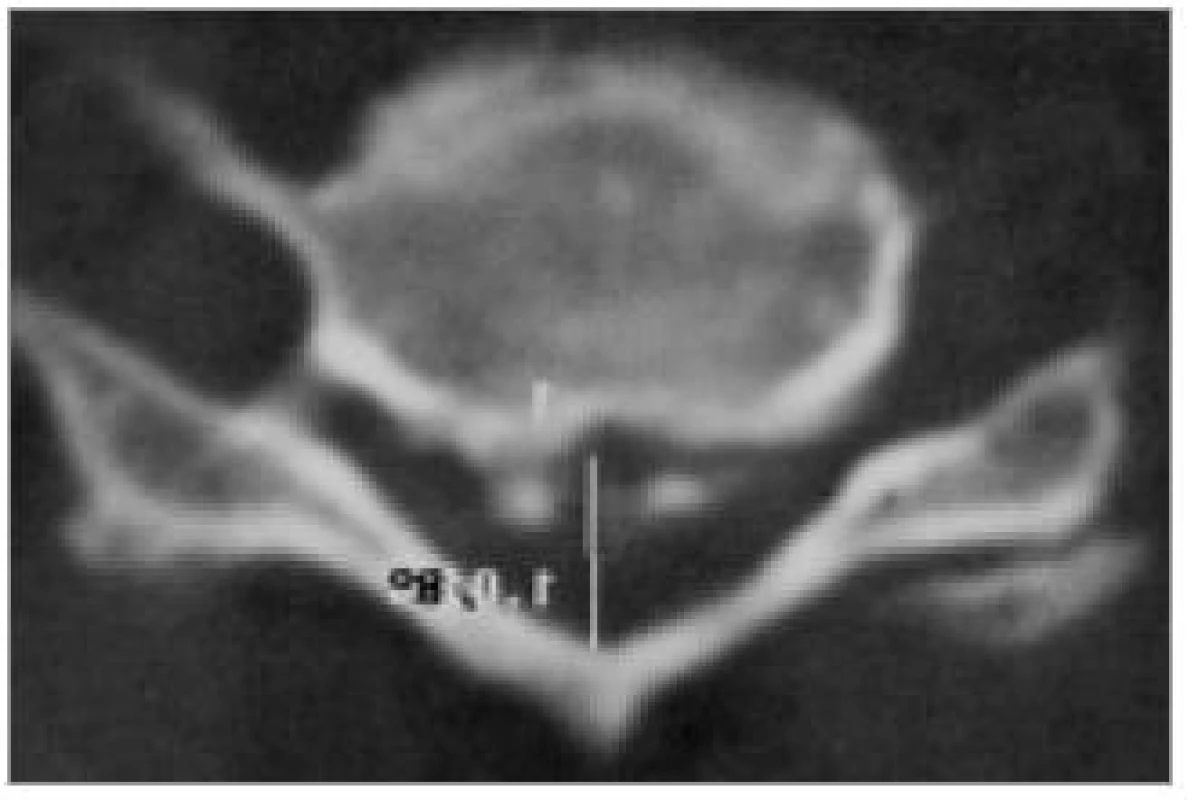
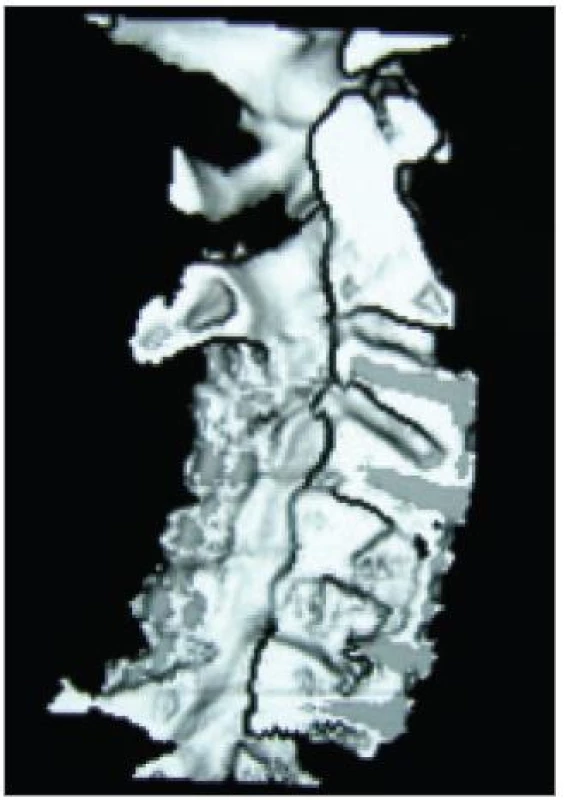
Moderními spirálními CT-přístroji lze méně invazivně zobrazit průběh arteriae vertebrales nebo provést prostorovou (3D) rekonstrukci kanálu páteřního (obr. 7) či cíleně znázornit jednotlivé kostní struktury (obr. 8), přičemž expozice se omezí a čas vyšetření významně zkrátí. I přes zmíněné výhody se ale stále jedná o iradiaci, což řadí CT, jinak velmi cennou v diagnostice úrazů či nádorových destrukcí, v případě degenerativních onemocnění krční páteře až do druhé řady.
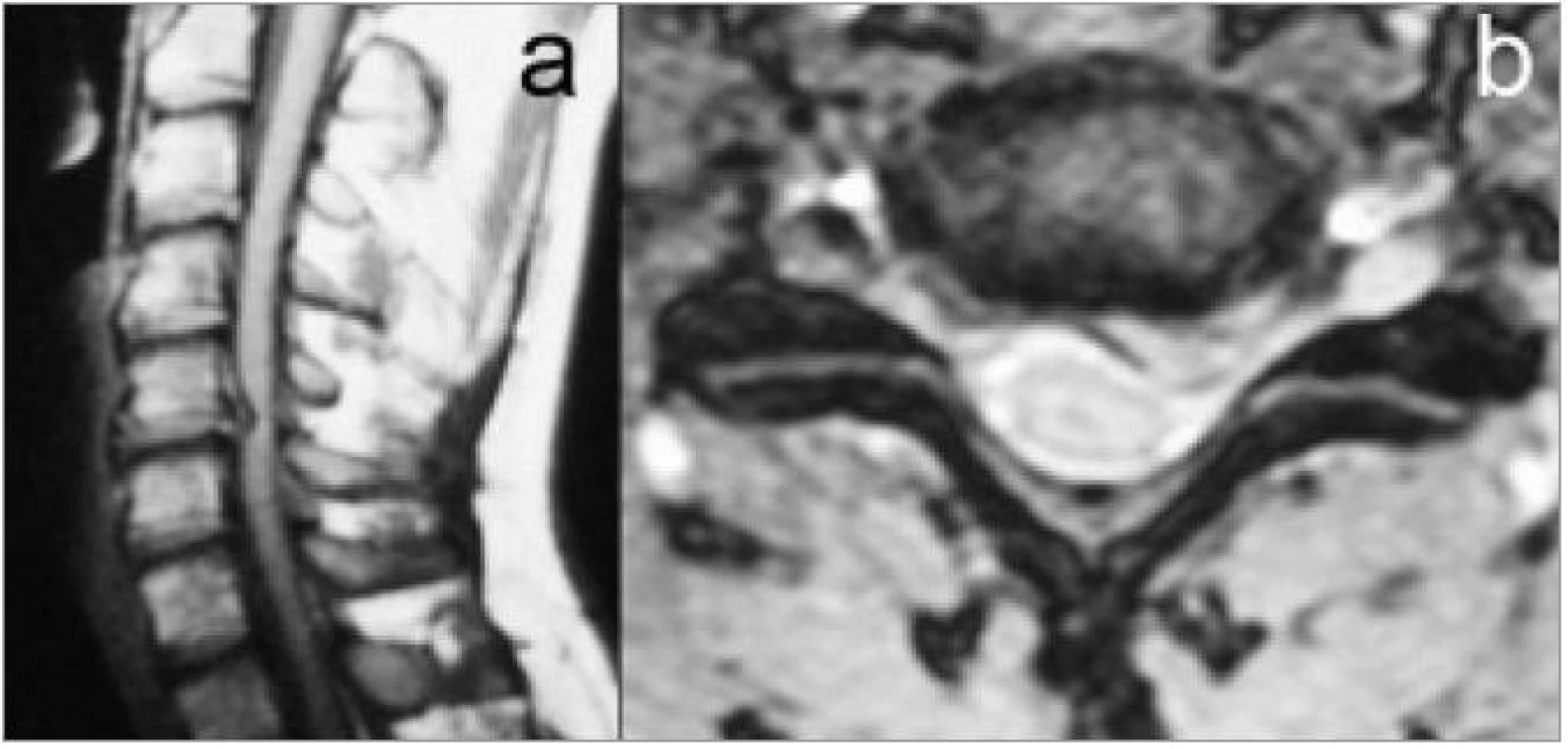
Magnetická rezonance (MRI)
Vyšetření magnetickou rezonancí má v diagnostice degenerativních onemocnění krční páteře nezastupitelnou úlohu. Je to jediné vyšetření, které přímo zobrazí útlak nervové tkáně a stav měkkých struktur ve všech rovinách (obr. 9). Je zcela neinvazivní. V současné době je z indikačního algoritmu nesmíme vynechat a je považováno za vyšetření první volby. Nelze je provést pouze ve výjimečných případech, např. u pacientů s implantovanými elektronickými zařízeními typu kardiostimulátoru. Kovové implantáty, např. endoprotézy velkých kloubů, dnes překážku nepředstavují. Vyšetření je dosud dosti časově náročné a některé pacienty trpící klaustrofobií je nezbytné farmakologicky sedovat nebo i uvést do celkové anestezie. Zcela novou dimenzí vyšetřování, zatím pro nás ale rutinně nedostupnou, je dynamické MRI zobrazení [19]. Narušený disk lze zobrazit v zátěži, flexi i extenzi, a tak je možné odhalit i postižení z klidového MRI vyšetření nerozeznatelné, například dynamickou kompresi nervových struktur nebo skrytou nestabilitu.
Kostní scintigrafie
Význam izotopového vyšetření je v diagnostice CDDD omezen na diferenciální diagnostiku oblastí s vyšším metabolickým obratem. V diagnostice nádorových lézí, zejména sekundárních, má však podstatně větší důležitost.
Diskografie
Stejně jako pro oblast bederní páteře je diskografie dosud kontroverzní metodou i pro oblast krční páteře. Diskografii na bederní páteři poprvé provedl Lindblom [20] v roce 1948 a od té doby proběhl významný názorový vývoj. V roce 1957 Smith a Nichols [21,22] metodiku použili i pro krční páteř. Obecně je diskografie považována za test velmi senzitivní, ale nespecifický. Abnormální obrazy jsou často viděny i u asymptomatických pacientů [12]. Postupně byl však k morfologickému nálezu přiřazen i výsledek klinický – aplikací kontrastní látky do nucleus pulposus může být vyvolána vyšším tlakem v disku bolest konkordantní s potížemi pacienta. Již Cloward [23,24] a Smith [21] indikovali své pacienty k prvním operacím na základě většího objemu kapaliny, který degenerovaný disk pojal, nicméně hlavním indikačním kritériem byla vyprovokovaná bolest v symptomatické ploténce.
Základním přínosem diskografie je tedy možnost odhalení zdroje chronické diskogenní bolesti, zejména v případech, ve kterých MRI zobrazuje více degenerativně změněných disků bez zřetelného tlaku na nervové struktury a chybí jasná neurologická symptomatologie.
Také diskrepance mezi klinickým a morfologickým nálezem nebo změna stavu plotének sousedících s fúzí může být indikací invazivní diskografie.
V naší klinické praxi diskografické vyšetření rutinně nepoužíváme, ale v současné době je indikujeme stále častěji v případech výše zmíněných a v souvislosti s aplikací mobilních náhrad (obr. 10).
Závěr grafických metod – doporučení pro referující lékaře
Grafický obraz patologie CDDD jistě není synonymem symptomatologie. Pozitivní nález je klinicky senzitivní, nikoli však specifický.
Všichni naši nemocní indikovaní k operaci pro CDDD mají nativní snímky krční páteře v neutrálním postavení a snímky dynamické. Dalším povinným vyšetřením je magnetická rezonance. Ostatní dříve popsané metody užíváme pouze při diferenciálně diagnostických nejasnostech.
Indikace k chirurgické intervenci
Cílem každého léčebného úsilí je zbavit nemocného obtíží a vhodnou prevencí zabránit progresi onemocnění. Ne jinak je tomu i v léčbě CDDD.
Nemocní přicházejí k lékaři zpravidla s bolestmi v oblasti krční páteře s iradiací do jedné nebo obou horních končetin. Neurologický výpad jako první projev degenerativního procesu je méně častý. Pokud není přítomen neurologický deficit, měla by konzervativní léčba a fyzioterapie vždy předcházet eventuální operační indikaci. Jejím základním cílem je farmakologicky, injekčními technikami a současným fyzioterapeutickým úsilím odstranit potíže, které nemocného k lékaři přivedly. Vybudování adekvátního svalového korzetu je důležité i z preventivního hlediska a může být časově náročné. Efektivita fyzioterapeutických postupů se tak může projevit až po dlouhodobém úsilí.
Obvykle se udává, že operační indikaci by měla předcházet intenzivní konzervativní léčba trvající 6–8 týdnů. Výjimku z těchto obecných pravidel tvoří pacienti s iniciálně významným nebo progredujícím neurologickým deficitem a nemocní, jejichž morfologický nález je natolik dramatický, že by mohl představovat významné riziko i při minimálním traumatu či extrémním pohybu. V takovém případě nebudeme váhat s časnou indikací operace.
Novou indikační skupinou s dosud omezenou klinickou zkušeností jsou nemocní, u kterých v symptomatologii dominují bolesti krční páteře a hlavy, někdy doprovázené vegetativními projevy. V těchto případech musí indikaci předcházet velmi pečlivá rozvaha doplněná vyšetřením, které potvrdí lokalizaci generátoru bolesti. Provokativní diskografie provedená ve více etážích, popř. blokáda příslušných intervertebrálních kloubů anestetikem obvykle rozhodnou, zda je pro nemocného výhodnější odstranění disku či fúze bolestivé spondylartrózy nebo zda operace není vhodná.
Ve sporných případech si ceníme i spolupráce klinického psychologa, který nám pomůže vyloučit nebo potvrdit psychosomatický původ obtíží.
Pro standardní operační indikaci je vždy zásadní soulad klinického a morfologického nálezu při současném neúspěchu konzervativních postupů. Konečným cílem našeho léčebného úsilí by měl být stav umožňující běžné životní aktivity nejen bez bolesti a neurologického deficitu, ale také bez abnormálních kineziologických, zejména muskulárních aktivit.
Nezbytnou podmínkou úspěchu operační indikace je také informovaný souhlas pacienta s příslibem minimálně 2leté spolupráce při sledování a vyhodnocování výsledku našeho chirurgického úsilí.
Metody operací degenerované krční ploténky
Historie chirurgické léčby
První fúze provedená Hadrou v roce 1889 [25] pro tuberkulózu je počátkem moderní chirurgie páteře. Do té doby byly k dispozici pouze destruktivní dekompresní techniky, které byly často příčinou následných deformit.
Teprve odhalení etiologie degenerativních onemocnění krční páteře nasměrovalo chirurgy k jejich operativnímu řešení. Walton a Paul v roce 1905 [26] operovali pacienta pro progredující kvadruparézu. Při prosté laminektomii však příčinu neodhalili. Tu objasnila až pitva. Pacient měl míchu utlačenou zpředu vyhřezlou meziobratlovou ploténkou tehdy popsanou jako chondrom. Zadní přístup, v té době obvyklý, poprvé úspěšně použil k odstranění výhřezu – „chondromu“ –Elsberg v roce 1925 [27]. Až v roce 1953 Spurling a Segerberg [28] ve své sestavě odstraněných laterálních herniací popisují již přesně, kde jsou limity dorzálního přístupu dané pozicí krční míchy.
Krční meziobratlová ploténka lokalizovaná ventrálně před míchou je logicky nejsnáze dosažitelná zpředu. Od doby, kdy byla anterolaterální cesta k přední ploše krční páteře navržena Badgleym v roce 1939 a popsána Robinsonem a Smithem v roce 1955 [29,30] a nezávisle Clowardem [31], došlo k nebývalému rozvoji prostředků používaných ke zprostředkování meziobratlové fúze. Původně nejčastěji užívané autologní kostní štěpy později z velké míry nahradily alogenní transplantáty [32–37] nebo kostní náhrady [38–41]. Kost byla do meziobratlového prostoru pouze vložena, nebo navíc ještě jištěna dlahou [42].
Dnes jsou místo kostních štěpů stále častěji užívány vložky (také koše, klece či v angl. literatuře cage, spacery) z cizorodých materiálů [43–46]. Cílem všech uvedených metod je vždy po adekvátní dekompresi a eventuální distrakci kolabovaného prostoru dosažení pevného spojení sousedních obratlů kostní fúzí.
Kostní srůst pohybového segmentu ale jistě není fyziologickým řešením. Omezení hybnosti může vést k dynamickému přetížení sousedních segmentů tzv. Adjacent Segment Degeneration (ASD) [47–49]. Odvěká touha chirurgů udržet hybnost v oblastech přírodou k tomu určených podpořená četnými pracemi popisujícími ASD vedla k vývoji totální mobilní náhrady disku krční páteře (CTDR – Cervical Total Disc Replacement). Právě v současném desetiletí zažíváme až nekritický rozkvět této moderní technologie [50–54].
Někteří autoři, aby udrželi mobilitu a zároveň odstranili útlak nervových kořenů, se dokonce vracejí k nejstarší metodice zadního přístupu foraminotomií, používají však mikrochirurgické techniky a minimálně invazivního přístupu. Jimi publikované výsledky jsou srovnatelné s výsledky operací z předního přístupu [55–57]. Na druhé straně však jsou i dnes zastánci prostého odstranění ploténky bez jakékoli následné náhrady [58–60].
Vlastní chirurgické metody – indikace, výhody a nevýhody
Základním cílem každé operace meziobratlového prostoru krční páteře je adekvátní dekomprese utlačených nervových struktur (míchy, kořenů), nebo v případě axiální bolesti odstranění generátoru bolesti (disku, fúze kloubů). Kvalitní technické vybavení operačního sálu a zkušenost chirurga jsou dnes základní podmínkou úspěšnosti operativy krční ploténky.
Do výbavy pro chirurgii krční páteře nezastupitelně patří peroperační skiaskopie, možnost peroperační elektrofyziologické monitorace, operační mikroskop, vysokoobrátková fréza a samozřejmě odpovídající variabilita dostupných páteřních implantátů.
I přesto, že v současné době neexistuje vědecky podložená studie, která by objasnila, zda je pro pacienty postižené segmentární degenerativní patologií krční páteře výhodnější prostá diskektomie, diskektomie s fúzí, instrumentovaná diskektomie s fúzí nebo totální náhrada protézou, z literárních údajů vyplývá, že odstraněnou ploténku většina autorů nahrazuje [35–37,41,43,44,46]. Udržení nebo znovuobnovení výšky meziobratlového prostoru má zásadní význam pro velikost intervertebrálního foramina, a tedy dekompresi nervového kořene. Fúze zprostředkovaná vlastní kostí je obvykle považována za „zlatý standard“ zejména v krátkodobém pooperačním sledování [32,33,35]. Z dlouhodobého hlediska se však klinické i morfologické výsledky zdají být srovnatelné, a tak stále není zřejmé, která z metod fúze pohybového segmentu je pro pacienta nejvýhodnější, nebo zda v indikovaných případech není ještě větším přínosem užití totální mobilní náhrady [46,52,54,60].
A) Prostá dekomprese
Diskektomie z předního přístupu (ACD – Anterior Cervical Discectomy)
Prosté odstranění disku z anterolaterálního přístupu překvapivě nebylo historicky první zvolenou metodou chirurgického ošetření CDDD [30,31].
Dobré zkušenosti s jednoduchým odstraněním výhřezu a hmot disku v bederní oblasti byly aplikovány v operativě CDDD až později [59]. Odstranění výhřezu ploténky v jedné etáži u nemocného s dominantní kořenovou symptomatologií přináší okamžitou úlevu od bolesti. Výkon je jednoduchý a velmi krátký. Operovaný může být okamžitě mobilizován a odpadají také nemalá rizika spojená s implantací jakékoli náhrady disku. Přestože jsou dobré výsledky dlouhodobého sledování nemocných po prosté jednoetážové diskektomii v literatuře popisovány zřídka [60], lze předpokládat, že u pacientů s primárně širokými intervertebrálními otvory po snížení meziobratlového prostoru diskektomií nedojde k jejich kritickému zúžení. V některých případech následně prostor disku zanikne a vytvoří se spontánní intervertebrální déza. Často ale vzniká analog pakloubu a přetrvává pohyb. Vývoj následných osteoproduktivních změn, stejně jako narušení sagitální dynamické rovnováhy mohou být argumentem proti této metodice. Zmíněná rizika negativního vývoje po diskektomii bez náhrady vyniknou u víceetážových dekompresí, u nichž bývá následná kyfotizace pravidlem. Transunkální mikrochirurgické odstranění laterálního výhřezu nebo osteofytu při zachování vlastní ploténky může být alternativou snižující tato rizika, neboť k snížení prostoru nedochází a také pohyb je zachován [61]. Diskutabilní a dosud nepopsané je však riziko následných recidiv.
Závěr: Prostá mikrodiskektomie z anterolaterálního přístupu představuje přijatelnou variantu ošetření jednoetážové patologie, zejména pokud adekvátně dekomprimujeme intervertebrální foramen. U více etážových výkonů je indikace sporná zejména pro vysoké riziko následné kyfotizace.
Mikroforaminotomie ze zadního přístupu
Dříve poměrně často prováděné zadní výkony – laminektomie, foraminotomie a jejich kombinace byly spojeny s destruktivní dekompresí v oblasti kloubů, rozsáhlou devastací stabilizujícího svalového aparátu a následnou kyfotizací, kterou provázely četné klinické obtíže. Dnes v souvislosti se snahou zachovat mobilitu operovaného segmentu se znovu někteří autoři k zadnímu přístupu vracejí [62]. Operace jsou ale prováděny minimálně invazivními přístupy nebo dokonce endoskopicky [57]. Indikace je obvykle limitována na laterální patologii v 1 etáži.
Závěr: Zadní mikrochirurgická nebo endoskopická foraminotomie může být s výhodou indikována u jednoetážové radikulopatie. Zejména v případě měkkého výhřezu, který tísní 1 kořen laterálně, je velmi efektivní. Riziko následných recidiv je však větší než po diskektomii
B) Dekomprese s následnou náhradou disku
Diskektomie s fúzí (ACDF – Anterior Cervical Discectomy with Fusion)
Tradičním a dříve nejvíce užívaným materiálem je autologní kostní štěp (obr. 11), u něhož lze vzhledem k jeho biologickým vlastnostem očekávat optimální morfologické výsledky [33,63].
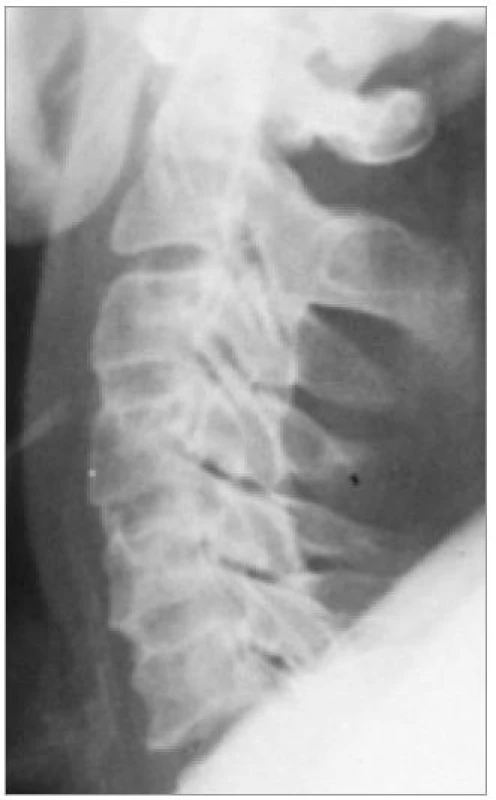
Kostní štěpy odebrané během operace pacientovi jsou přirozeně osteogenní, tzn. obsahují živé mezenchymové elementy v různém stupni osteoblastické diferenciace, takže mají samy zachovanou schopnost osteoprodukce. Jakožto přirozené kosti mají samozřejmě vlastnosti osteokonduktivní. Autogenní materiál neohrožuje operovaného přenosem infekční noxy a odpadá i problematika imunokompatibility štěpu.
Autologní štěpy obsahují podle svého anatomického původu různý poměr kortikální a spongiózní hmoty. Kortikální hmota poskytuje mechanickou oporu, zatímco spongiózní hmota je tkání bohatou na osteogenní prekurzory a nekolagenní proteiny kostní matrix, čímž vytváří dobré osteoinduktivní a osteogenní prostředí [40]. Kortikospongiózní poměr je dán především anatomickým původem štěpu. Nejčastějším místem odběru je hřeben lopaty kosti kyčelní. Trikortikální štěp tohoto původu má nejvyšší poměrné zastoupení spongiózy. Dalšími, méně využívanými místy odběru, jsou fibula, tělo přilehlých krčních obratlů, žebro a kalva [64,65,36].
Komplikace užití trikortikálního štěpu (obr. 12) bez další podpory (stand-alone) dosahují frekvence 5–25 % [31,66,67,30].

Odběr autologního kostního štěpu z lopaty kosti kyčelní je i v rukou zkušených spinálních chirurgů zatížen 10 až 19% rizikem komorbidity z oblasti odběru štěpu [66,65]. Mezi chirurgické komplikace se započítává zlomenina pánve po odběru štěpu, enterokutánní píštěl, svalová hernie a herniace břišního obsahu, raný hematom, raná infekce, iatrogenní poškození iliohypogastrického a ilioingvinálního nervu, prolongované hojení a kosmetická deformita. U podstatného procenta pacientů přetrvává po odběru chronická lokální bolest. Takto vysoké riziko komplikací se v minulosti stalo důvodem k hledání substituentů autologního štěpu. Odběrem autologního materiálu se také operace prodlužuje. V podmínkách české medicíny ale není zanedbatelný ani faktor ceny – tento typ náhrady disku je nejlevnější.
Počátek klinického užití alogenních (kadaverózních) štěpů se datuje do 50. let minulého století a je spojen se jménem jednoho z průkopníků krční páteřní chirurgie, R. B. Clowardem [31]. Od té doby byly aloštěpy užity snad ve všech spinálních lokalizacích [32,68]. Staly se oblíbené jak u dlouhých fúzí, kde je zapotřebí většího množství kostního materiálu, tak v těch případech, kdy se chirurg snaží vyhnout odběru autologního štěpu, ať už z důvodů zkrácení operačního výkonu, či výše popsané komorbidity v oblasti odběru. Morfologické výsledky jejich užití lze historicky rozdělit do 2 skupin. Menší skupina klinických prací popisuje u alograftů horší radiologické výsledky oproti autologním štěpům [33,69]. Větší část autorů však nalézá incidenci solidní kostní fúze srovnatelnou se štěpy autologními [32,34]. Výsledky prací se liší jen v oblastech incidence fúze při víceetážových výkonech, incidence fúze u kuřáků apod. Podobnou zkušenost učinilo i naše pracoviště u vzorku 79 konsekutivně operovaných pacientů [37].
Optimistické výsledky výše uvedených komparativních studií se promítly i do produkce farmaceutických společností, které přicházejí především na americké trhy s alogenními produkty, jež jsou svou velikostí a povrchovou úpravou uzpůsobeny konkrétnímu klinickému užití (alogenní spacery).
Alogenní materiály mají především osteokonduktivní vlastnosti. Jedná se o kostní tkáň, která byla v průběhu sterilizace a konzervace zbavena veškerých živých elementů, včetně vlastních mezenchymových. Primárním zdrojem osteoprogenitorových buněk jsou při předpokládané fúzi chirurgicky připravená lůžka krycích desek přilehlých obratlů a zde jsou produkovány i potřebné růstové faktory. Tím, že alomateriál podstoupuje fyzikální a chemickou úpravu, ztrácí i své imunogenní vlastnosti.
Alogenní štěpy byly v minulosti diskutovány pro nebezpečí infekce virem HIV, hepatitidy B a C a nověji i výskytu prionových nákaz. Riziko v této souvislosti jistě existuje, nicméně screening kadaverózního materiálu, z něhož jsou štěpy odebírány, společně s pokroky v oblasti konzervace a sterilizace štěpů, posunují takovou možnost spíše do roviny teoretické. Dosud byla popsána jediná kauza přenosu HIV touto cestou [70]. Stalo se tak v r. 1985 v případě kostního štěpu, který byl před implantací ošetřen pouze lyofilizací a jehož dárce, intravenózní narkoman, nebyl testován pro eventuální přenosnou chorobu. Celkem 12 příjemců přitom obdrželo kostní štěp a u 3 z nich onemocnění pokročilo do stadia AIDS. Dále je znám jediný případ pacienta, který prodělal hepatitidu C po implantaci kontaminovaného alogenního kostního štěpu, jenž byl ošetřen pouze lyofilizací [70].
Popsaným rizikům se lze zcela vyhnout, použijeme-li syntetickou náhradu kostní tkáně. Obvykle se jedná o deriváty trikalcium fosfátu nebo hydroxy-apatitu. Průmyslově tvarované vložky mají pouze osteokonduktivní vlastnosti a bývají poměrně křehké. Jejich využití je výhodné spíše u instrumentovaných operací.
Závěr: ACDF představuje jednoduchou variantu náhrady disku po dekompresi. Autologní kost se hojí nejrychleji, ale četnost dosažené fúze je finálně stejná jako při užití alograftu. Odběr autologní kosti je zatížen významnou lokální komorbiditou. Vložení auto - či alograftu bez současné instrumentace je zatíženo významným rizikem kolapsu, zlomeniny nebo dislokace. V případě alograftu či kortikálního autoštěpu není zanedbatelné riziko následného zanoření vloženého materiálu do sousedního obratle.
Instrumentovaná přední diskektomie s fúzí (i ACDF)
Z důvodů výše zmíněných komplikací souvisejících s užitím samotné (stand alone) kosti či její náhrady většina autorů preferuje užití instrumentace k zajištění štěpu [67,69,71,72].
Jednotlivé práce se různí jen typem fixujícího implantátu. K dispozici jsou zcela rigidní konstrukce, kde jsou šrouby pevně uzamčeny v dlaze, nebo zcela volné systémy, ve kterých mají šrouby možnost úhlového i podélného pohybu. V poslední době jsou užívány i tzv. dynamické dlahy, které umožňují podélný pohyb šroubů a kompresi zavedeného štěpu. Tím se údajně zlepšují podmínky pro osteointegraci [72,73]. Implantáty jsou obvykle z titanu a jeho slitin. Krom dobré biokompatibility je tak snížen i rozsah artefaktů při zobrazení magnetickou rezonancí. Do meziobratlového prostoru jsou obvykle vkládány kostní štěpy nebo jejich syntetické náhrady. Bikortikální zavedení šroubů výhodné pro pevnou rekonstrukci u traumatu v případě CDDD není nutné a většina jistících šroubů je zaváděna pouze monokortikálně [74]. I přes značné pokroky v designu a kvalitě užitých materiálů jsou popisovány komplikace (dislokace, zlomení šroubu nebo dlahy) plynoucí z užití přidaného hardware [67].
Práce na vyšší hladině průkaznosti, které by ospravedlňovaly užití té či oné metody instrumentace, však nejsou ještě k dispozici.
Závěr: ACDF je v současné době nejčastěji užívanou alternativou ošetření CDDD z předního přístupu. Klinické i morfologické výsledky jsou velmi dobré. Je však třeba počítat s určitou incidencí komplikací plynoucích z užitých implantátů.
Náhrada ploténky vložkou
Časová náročnost a komplikovanost dlahových fixací vedla chirurgy k hledání jednoduššího způsobu zprostředkování fúze meziobratlového prostoru.
V roce 1979 pozoroval zvěrolékař Grant [75], že distrakce a stabilizace pohybového segmentu krční páteře pomocí chirurgicky implantované vložky může pomoci u choroby zvané wobbler disease provázené myelopatií u dostihových koní. První úspěšné operace u koní provedl modifikovanou Clowardovou technikou a k fixaci segmentu použil válcový xenogenní kostní štěp. Později Bagby navrhl pro stejný účel ocelový válec s bočnými perforacemi. Bagby [75] v roce 1987 přednesl výsledky své práce během NASS (North American Spine Society Meeting) a navrhl tuto techniku užít v humánní medicíně. Společně s Kuslichem [76] vyvíjejí nový implantát, u kterého původní ocelový válec s bočnými perforacemi nahrazují dutým ve stěnách perforovaným šroubem velkého průměru s titanové slitiny. Do válce pak bylo možno vložit kostní tkáň za účelem osteoindukce. Současně se podobnou myšlenkou zabýval i Charles Ray [45]. Schválením Bagbyho a Kuslichovy vložky (BAK cage) FDA (Food and Drug Administration) došlo k významnému rozšíření metodiky nejprve v USA a později i v Evropě. U kovových implantátů však bylo obtížné rentgenologicky sledovat prorůstání kostní tkáně, a tak byla vyvinuta i celá řada vložek z umělých rentgen-transparentních hmot [43]. Hlavní výhodou všech typů vložek zůstává schopnost udržet výšku operovaného prostoru, a tím nepřímou distrakci intervertebrálních foramin (obr. 13).

I přes široké použití těchto náhrad, v anglické literatuře nazývaných spacer nebo cage zůstává problematika nutnosti použití kostní tkáně či její náhrady jako doplňku otevřena [41,46].
Nejčastěji popisovanou komplikací aplikace spacerů je jejich zanořování do sousedních obratlů. V námi hodnocené sestavě 198 operovaných meziobratlových prostorů se souhrnná incidence zaboření pohybovala kolem 13 % [77]. Noření bylo pozorováno vždy v časném pooperačním období a vždy se implantát bořil do dolního obratle. Jen výjimečně to bylo více než o 4 mm a v žádném případě nebyl touto komplikací ovlivněn klinický obraz. Nejčastější příčinou bylo uložení vložky příliš dorzálně. Takové komplikaci se dá zabránit využitím opory předních hran obratle s osteofyty a větší minerálovou denzitou [77].
Závěr: Vložky představují jednoduchou alternativu dlahovacích technik a lze očekávat i stejné klinické výsledky. Na druhé straně je však třeba počítat s nižší incidencí kostní fúze a se změnami operací nastoleného anatomického uspořádání, které mohou být pro páteř nevýhodné zejména z dlouhodobého hlediska.
Úplná náhrada disku protézou (CTDR)
Celé minulé století byla intersomatická fúze považována za ideální řešení segmentární degenerace krční páteře. Až příchod prospektivních studií s dlouhodobým sledováním pacientů, kteří fúzi podstoupili, odhalil neblahý vliv stabilizace meziobratlového prostoru na přilehlé segmenty [48,49,63]. Ty přebírají pohybové nároky kladené před operací na srostlý segment a dochází k jejich přetížení, hypermobilitě, nestabilitě a následně k akceleraci degenerativního procesu, jež se obvykle projeví osteoproduktivními změnami nebo výhřezem disku. Pokud jsou přítomny pouze známky radiologické (obr. 14), hovoříme o Adjacent Segment Degeneration (ASD). V případě souvisejících klinických symptomů situaci označujeme jako Adjacent Segment Disease [78]. I přesto, že teorie přetížení byla podpořena mnoha biomechanickými pracemi, které popisují hypermobilitu [79–81] nebo zvýšený intradiskální tlak ve fúzi sousedícím segmentu [82], sám Hilibrand jako jeden z jejích hlavních propagátorů uvádí, že stále není jisté, zda radiografické a klinické projevy ASD nejsou pouze přirozenou progresí dříve přítomné a pravděpodobně geneticky determinované degenerace sledovaného disku [49]. Citované studie tak netvoří důkazní oporu, ale spíše potencují odvěkou touhu chirurgů zachovat naturální stav, tedy pohyb. První laboratorní pokusy s pohyblivou náhradou ploténky se připisují Nachemsonovi, ale první klinické aplikace jsou dokumentovány pro Fernströmův kulový implantát [83]. Dislokace, zanořování a fúze kulového implantátu zbrzdily počáteční nadšení. Krční oblast představovala také větší nebezpečí pro případné komplikace než páteř bederní, kde byl následný rozvoj aplikace protéz mnohem rychlejší. První praktické implantace totální náhrady cervikálního disku (CTDR) byly prováděny až mnohem později [84,85]. Další výzkumy a hlavně vývoj nových materiálů a tvarů protéz [86] postupně vedly k většímu rozšíření CTDR. Skutečná éra CTDR však začala až v roce 2000, kdy Vincent Bryan zavedl sofistikovaný mobilní implantát do klinického užití na krční páteři [47,87]. Od té doby se tendence použít mobilní náhradu namísto fúze prohlubuje a mnohdy je provázena až nekritickým nadšením mohutně podporovaným výrobci protéz [50,53,88]. V současnosti je komerčně k dispozici již třetí generace totálních náhrad cervikálního disku (obr. 15). S touto problematikou je však vázána celá řada jiných postojů nejen k indikacím, ale i k následné rehabilitační péči [89–91].
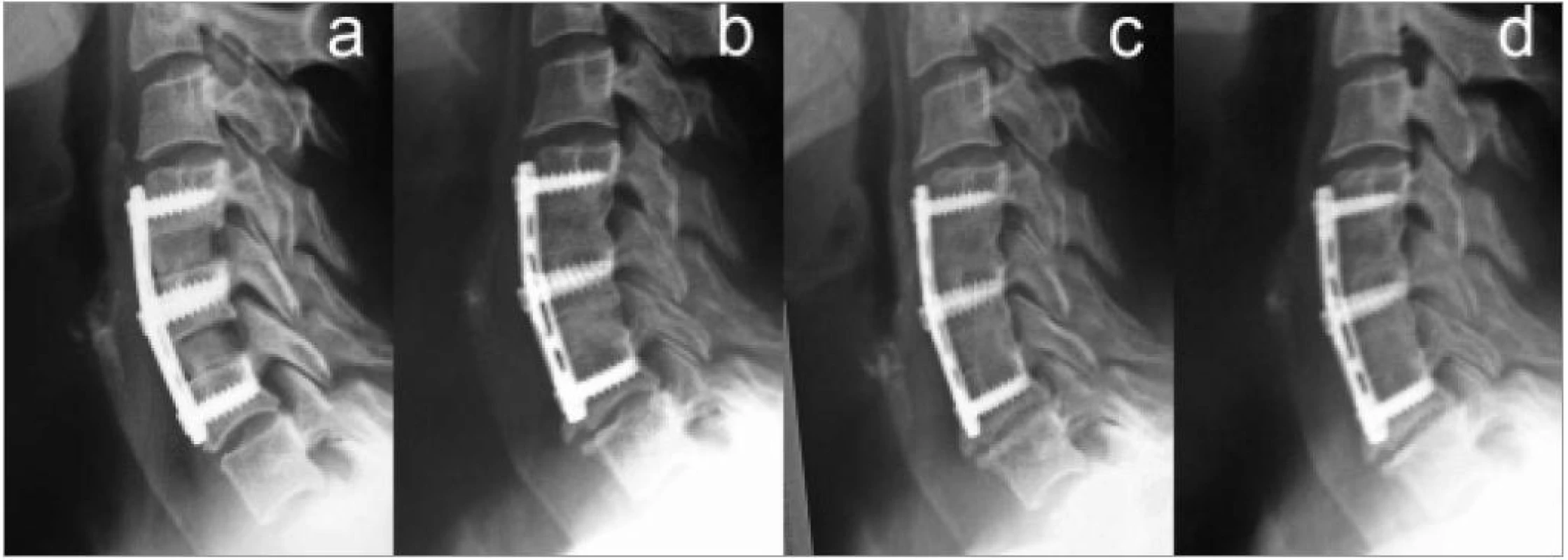

K indikačnímu rozhodnutí je vždy nutné vyšetření MRI a dynamické snímky v maximální aktivní flexi a extenzi. K operaci indikujeme zásadně jedince s ukončeným kostním růstem (starší 20 let).
Jednoznačně nejvíce z CTDR profitují nemocní s měkkým výhřezem krčního disku, s minimem osteoproduktivních změn (osteofyty), bez známek poškození intervertebrálních kloubů, jejichž segmentární pohyb je v dostatečné míře zachován (obr. 16). Podmínkou přihojení pohyblivých částí protézy je také kvalitní kostní lože bez deformací způsobených degenerací.
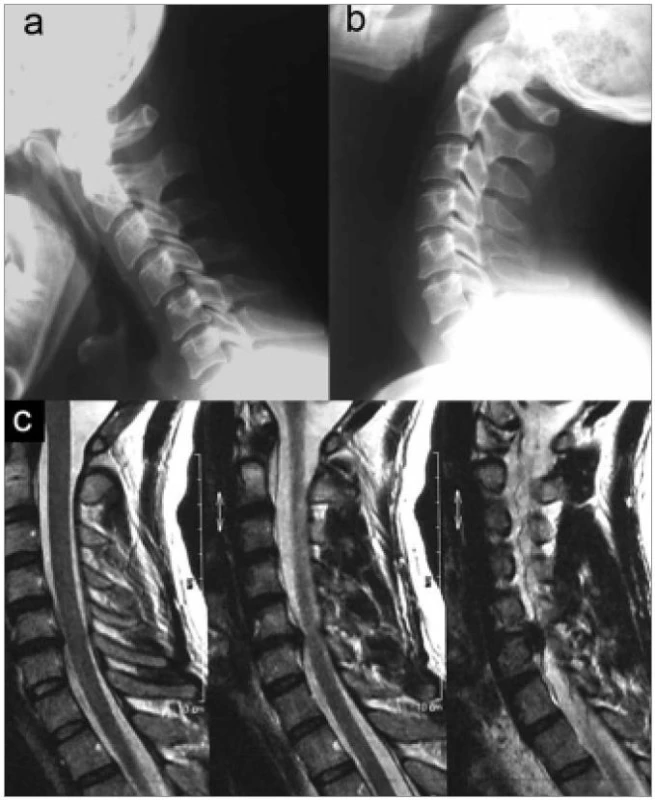
Krom obvyklých kontraindikací platných i pro ostatní implantace (alergie, zánět, osteoporóza apod) nepovažujeme za vhodné užití CTDR u nízkých meziobratlových prostorů, významných osteochondróz, kalcifikací předního nebo zadního podélného vazu, spondylartrózy, nebo segmentů apriori nepohyblivých [90]. Aplikací protézy nelze také obvykle napravit kyfózu segmentu, naopak často je možné vidět její pooperační zhoršení [89,92]. Dokonalá dekomprese nervových struktur je vždy podmínkou úspěchu, což platí pro CTDR ještě důrazněji než pro fúzní techniky.
Chybná indikace, ale i nekvalitní technické provedení, může vést k podstatně horším výsledkům než kterákoli z dříve citovaných metod. Jsou popsány i komplikace spojené s technicky náročnou implantací [93,94]. U prostorů s vyšším stupněm degenerace (hard disc) lze také očekávat vyšší frekvenci následné pooperační fúze, což jistě není cílem aplikace CTDR [90,95–97]. Publikované studie zatím nepotvrdily jednoznačně efektivitu mobilní náhrady v prevenci ASD [98].
Na druhé straně je ze zveřejněných prací zřejmé, že pacienty lze po CTDR mobilizovat rychleji a celkové klinické výsledky jistě nejsou horší než u ostatních metod [99–101].
Závěr: CTDR je nejmodernější alternativou ošetření meziobratlového prostoru po přední diskektomii. Aplikace protézy je však indikována pouze u poměrně úzce selektované skupiny pacientů s měkkým výhřezem krční ploténky, zachovanou hybností cílového segmentu, nepoškozenými klouby a dostatečně vysokým meziobratlovým prostorem.
Technicky je užití CTDR nejnáročnější metodou a mělo by být prováděno pouze ve spondylochirurgických centrech s dostatečnou zkušeností.
Sledování nemocných po operaci
Důvěryhodná interpretace výsledků spondylochirurgie je dnes podmínkou nutnou nejen pro publikační činnost, ale i pro vlastní audit a vývoj na každém pracovišti. Detekce a analýza vlastních komplikací (obr. 17) je jedinou cestou k jejich omezení v budoucnu.
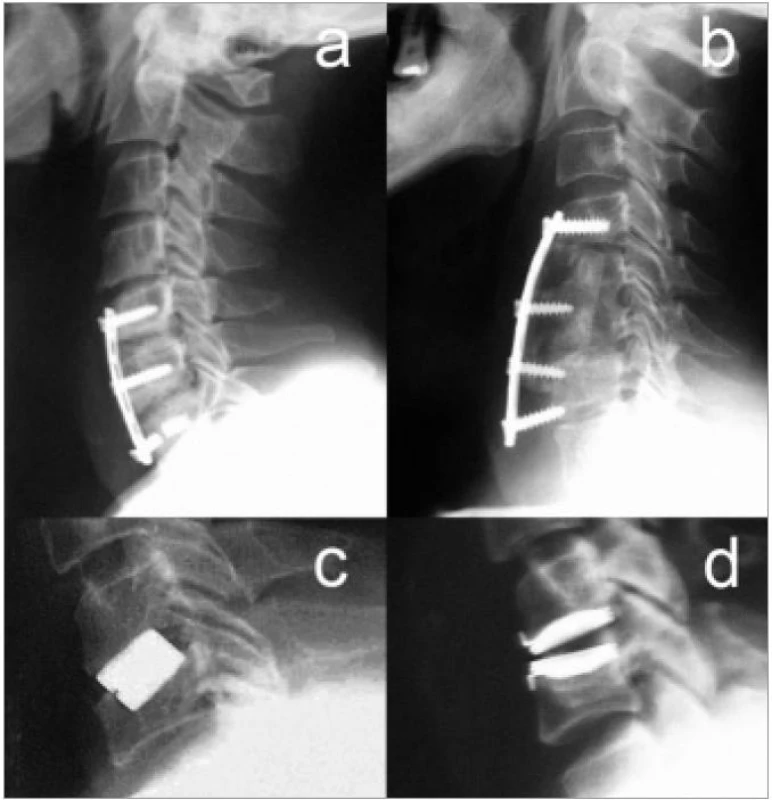
V chirurgii páteře je obvykle doporučeno prospektivní sledování klinických a morfologických výsledků v perioperačním období, po 1., 2. a 3. měsíci. Další kontroly jsou pak prováděny po 6 měsících, 1 roce a 2 letech [37,99,101].
Hodnocení výsledků chirurgického úsilí
U nemocných operovaných pro CDDD je za standardní považováno sledování vývoje neurologického nálezu, indexu krčního diskomfortu [102] dle Vernona (NDI – Neck Disability Index) a vizuálních analogových škál (VAS) vyjadřujících subjektivní hodnocení pacienta. Obvyklé je hodnoceni VAS pro intenzitu a frekvenci bolestí paže a krční oblasti. Stejně se hodnotí i spokojenost nemocného s výsledkem operace. Dalšími klinickými parametry mohou být odpovědi na otázky, zda by nemocný podstoupil operaci znovu, návrat do zaměstnání nebo dotazníky sledující dopad operace na kvalitu života nemocného. Morfologické výsledky jsou kontrolovány zobrazovacími metodami. Jejich frekvence je však nižší, abychom snížili přílišnou radiační zátěž.
Závěry: Chirurgie segmentárního degenerativního onemocnění krční páteře patří mezi nejefektivnější metody spondylochirurgie. Základní podmínkou úspěchu je přesná indikace a kvalitní technické provedení operace. Dobrých výsledků lze dosáhnout řadou metod ošetření meziobratlového prostoru. Pro žádnou z citovaných možností však není v literatuře dostatečná důkazní opora, a tak je dosud možné použít všechny s očekáváním podobných klinických výsledků.
Lékař odesílající nemocného k operaci by měl vždy znát výsledky operujícího týmu a být s ním v trvalém kontaktu. Zkušenost s prováděním podobných výkonů, stejně jako adekvátní technické vybavení pracoviště, by měly být dalším kritériem úspěšné spolupráce. Česká spondylochirurgická společnost JEP dlouhodobě sleduje parametry jednotlivých spondylochirurgických pracovišť a jejich výkonnost kategorizuje.
K orientaci mezi spondylochirurgickými pracovišti může referující neurolog, ortoped či rehabilitační specialista užít databáze společností garantovaných pracovišť, jež je každoročně aktualizována a zveřejňována na www.spine.cz.
Vznik předkládané práce nebyl podpořen žádným grantem ani jinými zdroji.
Poděkování
Autor děkuje všem svým spolupracovníkům z neurochirurgického oddělení, bez jejichž soustavné podpory by práce nemohla vzniknout.
doc. MUDr. Petr Suchomel, Ph.D.
Neurochirurgické oddělení
Neurocentrum
Krajská nemocnice Liberec a.s.
Husova 10
460 63 Liberec
e-mail: petr.suchomel@nemlib.cz
Přijato k recenzi: 2. 4. 2008
Přijato do tisku: 20. 5. 2008
Recenzenti:
prof. MUDr. Zdeněk Kadaňka, CSc.
doc. MUDr. Martin Krbec, CSc.
MUDr. Petr Vaněk, Ph.D.
doc. MUDr. Petr Suchomel, Ph.D. (1958)
Petr Suchomel vystudoval Fakultu všeobecného lékařství UK v Praze v r. 1983. Do r. 1992 pracoval v Ústí nad Labem – nejprve na chirurgické klinice, poté na neurochirurgickém oddělení, zde od roku 1987 jako vedoucí lékař JIP. Složil 2 atestace – první z chirurgie (1986), druhou z neurochirurgie (1991). Od r. 1992 působí jako primář Neurochirurgického oddělení nemocnice v Liberci a od r. 1994 jako přednosta Neurocentra Krajské nemocnice v Liberci. V r. 2005 dokončil doktorandské studium, v loňském roce se habilitoval na 1. LF UK v Praze. Doc. Suchomel působí rovněž jako učitel a garant oboru na Ústavu zdravotnických studií Technické univerzity v Liberci a jako docent na Neurochirurgické klinice 1. LF UK v Praze. Petr Suchomel se ve své práci zabývá zejména neurochirurgickou operativou se zaměřením na problematiku cévní neurochirurgie, chirurgie nádoru mozku, obalů, lbi a lební báze. Specializuje se na chirurgie páteře a míchy. Aktivně se podílel na více než 4 000 operacích, mimo ČR také v Thajsku, Malajsii, Spojených arabských emirátech, Brazílii, Slovensku, Libyi aj. Po celé své působení se věnuje výzkumné, pedagogické a školitelské činnosti.
Je členem výboru České neurochirurgické společnosti JEP, místopředsedou a členem výboru České spondylochirurgické společnosti JEP, členem České neurologické společnosti JEP, Společnosti pro neurovědy JEP a členem společnosti Central European Neurosurgical Society. Organizuje celostátní i mezinárodní kongresy, získal mnohá významná ocenění (čestný člen společností, Osobnost Liberecka, Pocta hejtmana aj). Doc. Suchomel je autorem a spoluautorem padesátky článků a kapitol v monografiích. Napsal odbornou publikaci Spondylolistéza.
Vědomostní test
1. Nejčastější příčinou bolestí v krční páteři je:
- a) nádorové onemocnění
- b) vadné držení
- c) degenerativní onemocnění
2. Axiální bolest krční páteře souvisí s:
- a) kostní přestavbou
- b) kompresí nervových kořenů
- c) iritací nervových zakončení v oblasti disku či kloubů
3. Radikulopatie je obvykle způsobena:
- a) útlakem nervového kořene v oblasti foramen intervertebrale
- b) poškozením předních míšních rohů
- c) zánětem nervového kořene
4. Nejčastější příčinou myelopatie je:
- a) ateroskleróza
- b) degenerativní onemocnění krční páteře
- c) zánět míšní tkáně
5. Prvním grafickým vyšetřením pacienta s “Cervical Degenerative Disc Disease” (CDDD) by mělo být:
- a) zobrazení magnetickou rezonancí (MRI)
- b) šikmý nativní snímek
- c) nativní snímek v bočné a předozadní projekci
6. Do základní sestavy grafických vyšetření pacienta s CDDD nepatří:
- a) MRI
- b) CT
- c) nativní snímek
7. CT u CDDD je vhodné k zobrazení:
- a) útlaku nervové tkáně vyhřezlou ploténkou
- b) kostních změn a osifikací v zadním podélném vazu
- c) stavu degenerace meziobratlové ploténky
8. Grafickým základem pro operační indikaci CDDD je:
- a) nativní snímek krční páteře, dynamický snímek a MRI
- b) nativní snímek krční páteře a CT
- c) nativní snímek, dynamické a šikmé snímky
9. Diskografie je výhodná zejména, neboť:
- a) přímo zobrazí morfologické změny disku
- b) může vyvolat konkordantní obtíže
- c) je snadno proveditelná
10. K chirurgické intervenci pro CDDD jsou indikováni nemocní:
- a) s významným neurologickým deficitem
- b) s výrazným grafickým nálezem
- c) s harmonickým klinickým a grafickým obrazem po neúspěchu konzervativní terapie
11. Konzervativní léčba by měla předcházet chirurgický výkon:
- a) vždy
- b) v případě nevýznamného morfologického nálezu
- c) pokud není neurologický deficit významný či neprogreduje
12. Nejvýhodnějším operačním řešením CDDD je:
- a) prosté odstranění nemocné ploténky
- b) odstranění a nahrazení ploténky štěpem nebo klecí
- c) dosud není jasné, která z metod je nejvýhodnější
13. Nejvýznamnější nevýhodou zadní mikroforaminotomie pro výhřez krční ploténky je:
- a) možnost poškození nervového kořene
- b) krvácení z oblasti foramen intervertebrale
- c) možnost recidivy výhřezu
14. Největší nevýhodou užití autologních kostních štěpů je:
- a) možnost hojení v chybném postavení
- b) komplikace a bolesti v místě odběru štěpu
- c) nutnost další operační rány
15. Použití kovových dlah a šroubů je spojeno s rizikem:
- a) imunitní reakce
- b) zlomení a dislokace implantátu
- c) obtížně možné revizní operace
16. Při “Anterior Cervical Discectomy with Fusion” (ACDF) se nejrychleji vhojují:
- a) autologní kostní štěpy
- b) alogenní kostní štěpy
- c) klece z kovu
17. Klinické výsledky ACDF jsou dle literatury nejlepší při užití:
- a) spacerů
- b) dlahových konstrukcí
- c) jsou stejné pro všechny metody
18. Totální náhrada cervikálního disku (CTDR) je vhodná u:
- a) víceetážového postižení
- b) u mladých nemocných
- c) v případě měkkého výhřezu se zachovalou hybností segmentu
19. O “Adjacent Segment Disease” (ASD) hovoříme:
- a) pokud dojde k degeneraci v segmentu přilehlém předchozí fúzi
- b) pokud dojde k symptomatické degeneraci segmentu přilehlého předchozí fúzi
- c) pokud dojde k symptomatické degeneraci přilehlého segmentu, jež nebyla dříve patrna
20. Výpovědní hodnotu mají výsledky operačního řešení CDDD při sledování:
- a) 6 měsíců
- b) 1 rok
- c) minimálně 2 roky
Správná je jedna nebo více odpovědí
Za správné vyřešení testu získá řešitel 5 kreditů ČLK.
Test můžete vyplnit na: WWW.CSNN.EU
Zdroje
1. Boos N, Weissbach S, Rohrbach M, Weiler C, Spratt KF, Nerlich AG. Classification of age related changes in lumbar intervertebral discs. Spine 2002; 27(23): 2631–2644.
2. Benoist M. Natural history of the aging spine. Eur Spine J 2003; 12(Suppl 2): S86–S89.
3. Urban J. The physiology of the intervertebral disc. In: Gunzburg R, Szpalski M (Eds). Lumbar disc herniation. Philadelphia: Lippincot Williams and Wilkins 2001 : 22–31.
4. Holm SH. Nutritional and pathophysiologic aspects of the lumbar intervertebral disc. In: Wiesel SW, Weinstein JN, Herkowitz H et al (Eds). The lumbar spine. Philadelphia: WB Saunders 1996 : 285–310.
5. Bogduk N, Windsor M, Inglis A. The inervation of the cervical intervertebral discs. Spine 1988; 13(1): 2–8.
6. Lukáš R, Barsa P, Suchomel P. Diskogenní bolest a její chirurgická léčba arthroplastikou. Acta Spondylologica 2004; 3(1): 9–17.
7. Kadaňka Z, Mareš M, Bednařík J, Smrčka V, Krbec M, Stejskal L et al. Approaches to spondylotic cervical myelopathy: conservative versus surgical results in a 3-year follow-up study. Spine 2002; 27(20): 2205–2210.
8. Lohnert J, Látal J. Cervikálna spondylotická myelopatia. Bratislavské Lek Listy 1999; 96 : 395–400.
9. Benzel EC, Lancon J, Kesterson L, Hadden T. Cervical laminectomy and dentate ligament section for cervical spondylotic myelopathy. J Spinal Disord 1991; 4(3): 286–295.
10. Herdmann J, Linzbach M, Krzan M, Dvorak J, Bock WJ. The European myelopathy score. Advances in Neurosurgery 1994; 22 : 266–268.
11. Rogers C, Joshi A, Dreyfuss P. Cervical instrinsic disc pain and radiculopathy. In: Malanga GA (Ed). Cervical Flexion-Extension Injuries. 2nd ed. Hanley and Belfus (State of the art reviews 1998): 323–356.
12. Schellhas KP, Smith MD, Cooper RG, Pollei SR. Cervical discogenic pain. Prospective correlation of magnetic resonance imaging and discography in asymptomatic subjects and pain sufferers. Spine 1996; (21)3 : 300–312.
13. Pracyk JB, Traynelis VC. Treatment of the painful motion segment: cervical arthroplasty. Spine 2005; 30(Suppl 16): S23–S32.
14. Schofferman J, Garges K, Goldwaithe N, Koestler M, Libby E. Upper cervical anterior discectomy and fusion improves discogenic cervical headaches. Spine 2002; 27(20): 2240–2244.
15. Wachli B, Dvorak J, Grob D. Cervical spine disorders and headaches. 21st Meeting of CSRS, New York 1993.
16. MacNab I. Symptoms in cervical disc degeneration. In: Cervical Spine research Society Editorial Committee (Ed). The Cervical Spine. 2nd ed. Philadelphia: JB Lippincott 1989 : 599–606.
17. Abumi K, Manabu I, Kaneda K. Surgical treatment of cervical destructive spondylarthropathy (DSA). Spine 2000; 25(22): 2899–2905.
18. Friedenberg ZB, Miller VT. Degenerative disc disease in cervical spine. J Bone Joint Surg Am 1963; 45 : 1171–1178.
19. Schlamann M, Reischke L, Klassen D, Maderwald S, Böhner V, Kollia K et al. Dynamic magnetic resonance imaging of the cervical spine using the NeuroSwing System. Spine 2007; 32(21): 2398–2401.
20. Lindblom K. Diagnostic puncture of intervertebral disks in sciatica. Acta Orthop Scand 1948; 17 : 231–239.
21. Smith G. The normal cervical diskogram; with clinical observations. Am J Roentgenol Radium Ther Nucl Med 1959; 81(6): 1006–1010.
22. Smith G, Nichols PJ. The technique of cervical discography. Radiology 1957; 68 : 718–720.
23. Cloward RB. Cervical discography: technique, indications and use in the diagnosis of cervical ruptured disks. Am J Roentgenol 1958; 79(4): 563–564.
24. Cloward RB. Cervical discography: a contribution to the aethiology and mechanism of neck, shoulder and arm pain. Ann Surg 1959; 150 : 1052-1064.
25. Hadra BE. Wiring of the spinous process in injury and Pot´s disease. Trans Am Orthop Assoc 1981; 4 : 206.
26. Walton GL, Paul WE. Contribution to the study of spinal surgery: One successful and one unsuccessful operation for the removal of the tumor. Boston Med Surg J 1905; 153 : 114–117.
27. Elsberg CA. The extradural ventral chondromas, their favorite sites, the spinal cord and root symptoms they produce, and their surgical treatment. Bull Neurol Inst NY 1931; 1 : 350–388.
28. Spurling RG, Segerberg LH. Lateral intervertebral disc lesionsin the lower cervical region. J Am Med Assoc 1953; 151(5): 354–359.
29. Bailey RW, Badgley CE. Stabilization of the cervical spine by anterior fusion. J Bone Joint Surg Am 1960; 42-A: 565–594.
30. Robinson RA, Smith GW. Anterolateral cervical disc removal and interbody fusion for cervical disc syndrome. Bull Johns Hopkins Hosp 1955; 96 : 223–224.
31. Cloward RB. The treatment of ruptured intervertebral discs by vertebral body fusion. Indications, operative technique, aftercare. J Neurosurg 1953; 10(2): 154–168.
32. Ann HS, Simpson JM, Glover JM, Stephan J. Comparison between allografts plus demineralised bone matrix versus autograft. Spine 1995; 20(20): 2211–2216.
33. Bishop RC, Moore KA, Hadley MN. Anterior cervical interbody fusion using autogenic and allogenic bone graft substrate: a prospective comparative analysis. J Neurosurg 1996; 85 : 206–210.
34. Brown CW, Orme TJ, Richardson HD. The rate of pseudoartrosis in patients who are smokers and patients who are not smokers: a comparison study. Spine 1986; 11 : 942–943.
35. Floyd T, Ohnmeiss D. A meta-analysis of autograft versus allograft in anterior cervical spine fusion. Eur Spine J 2000; 9(5): 398–403.
36. Martin GJ jr, Haid RW jr, MacMillan M, Rodts GE jr, Berkman R. Anterior cervical discectomy with freeze-dried fibula allograft. Overview of 317 cases and literature review. Spine 1999; 24(9): 852–858.
37. Suchomel P, Barsa P, Buchvald P, Svobodník A, Vaničková E. Autologous versus allogenic bone grafts in instrumented anterior cervical discectomy and fusion: a prospective study with respect to a bone union pattern. Eur Spine J 2004; 13(6): 510–515.
38. Erbe EM, Marx JG, Clineff TD, Bellincampi LD. Potential of an ultraporous beta-tricalcium phosphate synthetis cancelous bone void filler and bone marrow aspirate composite graft. Eur Spine J 2001; 10(Suppl 2): S141–S146.
39. Khan SN, Sandhu HS, Parvataneni HK, Girardi FP, Cammisa FP jr. Bone graft substitutes in spine surgery. Bull Hosp Jt Dis 2000; 59(1): 5–10.
40. Marchesi DG. Spinal fusions: bone and bone substitutes. Eur Spine J 2000; 9(5): 372–378.
41. Rudinský B, Hill R, Koleják K. Anterior cervical interbody fusion with bioceramic cages: initial experience. In: Kaech DL, Jinkins JR (Eds). Spinal restabilisation procedures. Elsevier 2002 : 249–256.
42. Orozco Delcios R, Llovet Tapies J. Osteosyntesis en lac fractures de raquis cervical. Revista Otop Traumatol 1977; 14 : 285–288.
43. Brantigan JW, Steffee AD, Geiger JM. A carbon fiber implant to aid interbody lumbar fusion: mechanical testing. Spine 1991; 16(Suppl 6): S227–S282.
44. Matgé G, Leclercq TA. Rationale for interbody fusion with threaded titanium cages at cervical and lumbar levels. Results of 357 cases. Acta Neurochir (Wien) 2000; 142(4): 425–434.
45. Ray CD. Spinal interbody fusion: a review featuring new generation technigues. Neurosurg Q 1997; 7(2): 135–156.
46. Suchomel P, Barsa P. Náhrada krční meziobratlové ploténky vložkou Cespace bez použití kosti či její náhrady. Prospektivní studie. Acta Spondylologica 2004; 3(1): 5–9.
47. Goffin J, Casey A, Ker P, Liebig K, Lind B, Logroscino C et al. Preliminary Clinical Experience with the Bryan Cervical Disc Prosthesis. Neurosurgery 2002; 51(3): 840–847.
48. Kulkarni V, Rajshekhar V, Raghuram L. Accelerated spondylotic changes adjacent to the fused segment following central cervical corpectomy: magnetic resonance imaging study evidence. J Neurosurg Spine 2004; 100 : 2–6.
49. Hilibrand AS, Robbins M. Adjacent segment degeneration and adjacent segment disease: the consequences of spinal fusion? Spine J 2004; 4(Suppl 6): 190S–194S.
50. Bertagnoli R, Duggal N, Pickett GE, Wigfield CC, Gill SS, Karg A et al. Cervical Total Disc Replacement. Part Two. Clinical Results. Orthop Clin North Am 2005; 36(3): 355–362.
51. Bertagnoli R, Yue JJ, Pfeiffer F, Fenk-Mayer A, Lawrence JP, Kershaw T et al. Early results after ProDisc-C cervical disc replacement. J Neurosurg Spine 2005; 2(4): 403–410.
52. Coric D, Finger F, Boltes P. Prospective randomized controlled study of the Bryan Cervical Disc: early clinical results from a single investigational site. J Neurosurg Spine 2006; 4(1): 31–35.
53. Pimenta L, McAfee P, Cappuccino A, Kellera FP, Link HD. Clinical experience with the new artificial cervical PCM (Cervitech) Disc Spine J 2004; 4(Suppl 6): 315S–321S.
54. Singh K, Vaccaro AR, Albert TJ. Assessing the potential impact of total disc arthroplasty on surgeon practice patterns in North America. Spine J 2004; 4(Suppl 6): 195S–201S.
55. Clarke MJ, Ecker RD, Krauss WE, McClelland RL, Dekutoski MB. Same-segment and adjacent-segment disease following posterior cervical foraminotomy. J Neurosurg Spine 2007; 6(1): 5–9.
56. Gala VC, O'Toole JE, Voyadzis JM, Fessler RG. Posterior minimally invasive approaches for the cervical spine. Orthop Clin North Am 2007; 38(3): 339–349.
57. Ruetten S, Komp M, Merk H, Godolias G. A new full-endoscopic technique for cervical posterior foraminotomy in the treatment of lateral disc herniations using 6.9-mm endoscopes: prospective 2-year results of 87 patients. Minim Invasive Neurosurg 2007; 50(4): 219–226.
58. Dowd GC, Wirth FP. Anterior cervical discectomy: is fusion necessary? J Neurosurg 1999; 90(Suppl 1): 8–12.
59. Hirsch C. Cervical disc rupture: diagnosis and therapy. Acta Orthop Scan 1960; 30 : 172–186.
60. Savolainen S, Rinne J, Hernesniemi J. A prospective randomised study of anterior single level cervical disc operations with long-term follow-up: Surgical fusion is unnecessary. Neurosurgery 1998; 43(1): 51–55.
61. Lee JY, Löhr M, Impekoven P, Koebke J, Ernestus RI, Ebel H et al. Small keyhole transuncal foraminotomy for unilateral cervical radiculopathy. Acta Neurochir (Wien) 2006; 148(9): 951–958.
62. Cağlar YS, Bozkurt M, Kahilogullari G, Tuna H, Bakir A, Torun F et al. Keyhole approach for posterior cervical discectomy: experience on 84 patients. Minim Invasive Neurosurg 2007; 50(1): 7–11.
63. Bohlman HH, Emerz SE, Goodfellow DB, Jones PK. Robinson Anterior Cervical Discectomy and Arthrodesis for Cervical Radiculopathy. J Bone Joint Surg Am 1993; 75(9): 1298–1307.
64. Gore DR. The arthrodesis rate in multilevel anterior cervical fusions using autogenous fibula. Spine 2001; 26(11): 1259–1263.
65. Whitecloud 3rd TS, La Rocca H. Fibular strut graft in reconstructive surgery of the cervical spine. Spine 1976; 1 : 33–43.
66. Gore DR. Technique of cervical interbody fusion. Clin Orthop 1984; 188 : 191–195.
67. Graham JJ. Complications of cervical spine surgery.A five-year report on a survey of the membership of the cervical spine research society by the morbidity and mortality committee. Spine 1989; 14 : 1046–1050.
68. Barsa P, Suchomel P. Organické materiály v přední krční diskektomii a fúzi. Acta Spondylologica 2002; 1(2): 123–129.
69. Zdeblick TA, Ducker TB. The use of freeze-dried allograft bone for anterior cervical fusions. Spine 1991; 16(7): 726–729.
70. Tomford WW. Transmission of disease through transplantation of musculoskeletal allografts. J Bone Joint Surg Am 1995; 77(11): 1742–1754.
71. Barsa P, Suchomel P, Buchvald P, Kolářová E, Svobodník A. Je víceetážová instrumentovaná přední krční fúze rizikovým faktorem vzniku kostního spojení? (prospektivní studie s minimální délkou sledování 3 roky). Acta Chir Orthop Traumatol Cech 2004; 71(3): 137–141.
72. Epstein NE. Dynamic anterior cervical plates for multilevel anterior corpectomy and fusion with simultaneous posterior wiring and fusion: efficacy and outcomes. Spinal Cord 2006; 44(7): 432–439.
73. Stulik J, Pitzen TR, Chrobok J, Ruffing S, Drumm J, Sova L et al. Fusion and failure following anterior cervical plating with dynamic or rigid plates: 6-months results of a multi-centric, prospective, randomized, controlled study. Eur Spine J 2007; 16(10): 1689–1694.
74. Barsa P, Suchomel P, Buchvald P, Lukáš R, Vaníčková E. Jsou šrouby při přední krční fúzi s bikortikální fixací skutečně bikortikálně zavedeny? Retrospektivní studie. Acta Chir Orthop Traumatol Cech 2002; 69 : 35–38.
75. Bagby GW. Arthrodesis by the distraction-compression using a stainless steel implant. Orthopedics 1988; 11(9): 931–934.
76. Kuslich SD. The treatment of chronic discogenic low back pain by the Bagby and Kuslich method of interbody fusion. In: Szpalski M, Gunzburg R, Spengler DM et al (Eds). Instrumented fusion of the degenerative lumbar spine: State of the art, questions and controversies. Philadelphia: Lippincott-Raven 1996 : 233–248.
77. Barsa P, Suchomel P. Factors affecting sagittal malalignment due to cage subsidence in standalone cage assisted anterior cervical fusion. Eur Spine J 2007; 16(9): 1395–1400.
78. Hilibrand AS, Carlson GD, Palumbo MA, Jones PK, Bohlman HH. Radiculopathy and myelopathy at segments adjacent to the site of a previous anterior cervical arthrodesis. J Bone Joint Surg Am 1999; 81(4): 519–528.
79. DiAngelo DJ, Foley KT. An improved biomechanical testing protocol for evaluating spinal arthroplasty and motion preservation devices in a multilevel human cadaveric cervical model. Neurosurg Focus 2004; 17(3): E4.
80. DiAngelo DJ, Foley KT, Morrow BR, Schwab JS, Song J, German JW et al. In vitro biomechanics of cervical disc arthroplasty with the Prodisc-C total disc implant. Neurosurg Focus 2004; 17(3): E7.
81. Maiman DJ, Kumaresan S, Yoganandan N, Pintar FA. Biomechanical effect of anterior cervical spine fusion on adjacent segments. Biomed Mater Eng 1999; 9(1): 27–38.
82. Dmitriev AE, Cunningham BW, Hu N, Sell G, Vigna F, McAfee PC. Adjacent level intradiscal pressure and segmental kinematics following a cervical total disc arthroplasty: an in vitro human cadaveric model. Spine 2005; 30(10): 1165–1172.
83. Le H, Thongtrangan I, Kim DH. Historical review of cervical arthroplasty. Neurosurg Focus 2004; 17(3): E1.
84. Cummins BH, Robertson JT, Gill SS. Surgical experience with an implanted artificial cervical joint. J Neurosurg 1998; 88(6): 943–948.
85. Wigfield CC, Gill SS, Nelson RJ, Metcalf NH, Robertson JT. The New Frenchay Artificial Cervical Join. Spine 2002; 27(22): 2446–2452.
86. Smith HE, Wimberley DW, Vaccaro AR. Cervical arthroplasty: material properties. Neurosurg Focus 2004; 17(3): E3.
87. Goffin J, Van Calenbergh F, van Loon J, Casey A, Kehr P, Liebig K et al. Intermediate follow-up after treatment of degenerative disc disease with the Bryan Cervical Disc Prosthesis: single-level and bi-level.. Spine 2003; 28(24): 2673–2678.
88. McAfee PC, Cunningham B, Dmitriev A, Hu N, Woo Kim S, Cappuccino A et al. Cervical disc replacement-porous coated motion prosthesis: a comparative biomechanical analysis showing the key role of the posterior longitudinal ligament. Spine 2003; 28(20): S176–S185.
89. Pickett GE, Mitsis DK, Sekhon LH, Sears WR, Duggal N. Effects of a cervical disc prosthesis on segmental and cervical spine alignment. Neurosurg Focus 2004; 17(3): E5.
90. Mehren C, Suchomel P, Grochulla F, Barsa P, Sourkova P, Hradil J et al. Heterotopic ossification in total cervical artificial disc replacement. Spine 2006; 31(24): 2802–2806.
91. Barsa P, Pešánová H, Suchomel P. Rehabilitační a režimové vedení pacientů po náhradě krční meziobratlové ploténky a intervertebrální déze. Rehabilitace a fyzikální lékařství 2004; 11(3): 122–127.
92. Pickett GE, Rouleau JP, Duggal N. Kinematic analysis of the cervical spine following implantation of an artificial cervical disc. Spine 2005; 30(17): 1949–1954.
93. Pickett GE, Sekhon LH, Sears WR, Duggal N. Complications with cervical arthroplasty. J Neurosurg Spine 2006; 4(2): 98–105.
94. Shim ChS, Shin HD, Lee SH. Posterior avulsion fracture at adjacent vertebral body during cervical disc replacement with ProDisc-C: a case report.. J Spinal Disord Tech 2007; 20(6): 468–472.
95. McAfee PC, Cunningham BW, Devine J, Williams E, Yu-Yahiro J. Classification of heterotopic ossification (HO) in artificial disc replacement. J Spinal Disord Tech 2003; 16(4): 384–389.
96. Leung C, Casey AT, Goffin J, Kehr P, Liebig K, Lind B et al. Clinical significance of heterotopic ossification in cervical disc replacement: a prospective multicenter clinical trial. Neurosurgery 2005; 57(4): 759–763.
97. Parkinson JF, Sekhon LHS. Cervical arthroplasty complicated by delayed spontaneous vision. J Neurosurg Spine 2005; 2(3): 377–380.
98. Robertson JT, Papadopoulos SM, Traynelis VC. Assessment of adjacent-segment disease in patients treated with cervical fusion or arthroplasty: a prospective 2-year study. J Neurosurg Spine 2005; 3(6): 417–423.
99. Mummaneni PV, Haid RW. The future in the care of the cervical spine: interbody vision and arthroplasty. J Neurosurg Spine 2004; 1(2): 155–159.
100. Porchet F, Metcalf NH. Clinical outcomes with the Prestige II cervical disc: preliminary results from a prospective randomized clinical trial. Neurosurg Focus 2004; 17(3): E6.
101. Sasso RC, Smucker JD, Hacker RJ, Heller JG. Clinical outcomes of BRYAN cervical disc arthroplasty: a prospective, randomized, controlled, multicenter trial with 24-month follow-up. J Spinal Disord Tech 2007; 20(7): 481–491.
102. Vernon H, Mior S. The Neck Disability Index: a study of reliability and validity. J Manipulative Physiol Ther 1991; 14(7): 409–415.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2008 Číslo 3
-
Všechny články tohoto čísla
- Degenerace krční meziobratlové ploténky – indikace a možnosti chirurgické léčby
- Depersonalizace a derealizace – současné nálezy
- Sexuální dysfunkce u žen s epilepsií a jejich příčiny
- Pohybové aktivity pacientů trpících dědičnou polyneuropatií
- Asociace vybraných rizikových faktorů s tíží aterosklerotického postižení v karotické bifurkaci
- Funkce pravé komory srdeční a výskyt plicní hypertenze u pacientů se syndromem obstrukční spánkové apnoe
- Přínos vyšetření čichu v časné diagnostice demencí neurodegenerativní etiologie
- Analýza pulzové vlny v objektivizaci bolesti – předběžné sdělení
- Kvalita života u pacientů po subarchnoidálním krvácení – roční katamnéza
- Retrospektivní analýza nálezů zrakových evokovaných potenciálů při akutním zánětu zrakového nervu
- Laboratorní ukazatele neurodegenerace v likvoru a míra motorického postižení u Parkinsonovy nemoci: korelační studie
- Tau-protein, fosforylovaný tau-protein a beta-amyloid42 v likvoru u demencí a roztroušené sklerózy
- Migréna v těhotenství
- Sporadický „guamský parkinsonský komplex“ nebo koincidence více neurodegenerativních onmocnění?
- Použití DTI traktografie v neuronavigaci při operacích mozkových nádorů: kazuistiky
- Webové okénko
-
Analýza dat v neurologii
IX. Poissonovo rozdělení - Gerhard Waberžinek
- Management ischemické cévní mozkové příhody a tranzitorní ischemické ataky – doporučení European Stroke Organisation (ESO) 2008 – zestručněná česká verze
- Doporučený postup sekundární prevence recidivy po akutní cévní mozkové příhodě: mozkovém infarktu/tranzitorní ischemické atace a hemoragické cévní mozkové příhodě
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Depersonalizace a derealizace – současné nálezy
- Degenerace krční meziobratlové ploténky – indikace a možnosti chirurgické léčby
- Migréna v těhotenství
- Pohybové aktivity pacientů trpících dědičnou polyneuropatií

