Supracerebellární transtentoriální přístup
Supracerebellar transtentorial approach
Aim: The aim of this work was a retrospective evaluation of the safety of the supracerebellar transtentorial approach in our patient series. It represents a technically challenging approach, which we used during surgeries of the posterior and medial mediotemporal area, lateral mesencephalon and posteromedial thalamus. Materials and methods: We evaluate the series of our 8 patients, which we operated on using the supracerebellar transtentorial approach during 2013–2021. In one case, we dealt with anaplastic astrocytoma, 3× with glioblastoma multiforme primary surgery, 1× with diffuse midline H3K27M glioma, 1× with glioblastoma multiforme recurrence surgery, 1× with low-grade glioma surgery and once we operated using this approach an acutely bleeding cavernoma of the lemniscal trigone of the mesencephalon. All our patients were operated on in a semisitting position. Results: The thirty-day mortality rate of our series is zero. In case of a patient with diffuse midline H3K27M glioma which was primarily operated on in a bad neurological condition, we had to perform early revision surgery using the same approach due to residual tumor hemorrhage. In case of our first patient with extensive mediotemporal anaplastic astrocytoma, we had to add the suboccipital approach for resection radicality increase early after the first phase of surgery; after the surgery, he had superior quadrantanopsia. In one patient’s case, ischemia of the occipital lobe occurred due to an intraoperatively visible lesion of the posterior cerebral artery inside the glioblastoma. After surgery, hemianopsia was present. Conclusion: The approach poses a technically challenging, but concurrently safe surgical trajectory. In case of the lesions affecting the mediotemporal area, it is advantageous for its medial and posterior part, but during the resection it is possible to reach as far as the uncus and amygdala. The prerequisite condition is accurate anatomical knowledge; in our department, we prefer the semisitting position for this approach. It is important to have a sufficient cerebrospinal fluid decompression by releasing the fluid from the cisterna magna from a separate dural incision and a gentle manipulation of the vascular structures of the tentorial incisura.
Keywords:
Hippocampus – Amygdala – brain glioma – cavernoma – supracerebellar approach
Autoři:
R. Bartoš 1,2; M. Sameš 1; A. Malucelli 1; A. Hejčl 1; D. Ospalík 3; D. Bejšovec 4; V. Němcová 2
Působiště autorů:
Neurochirurgická klinika Univerzity, J. E. Purkyně, Masarykova nemocnice, KZ a. s., Ústí nad Labem
1; Anatomický ústav 1. LF UK, Praha
2; Neurologické oddělení, Masarykova, nemocnice, KZ a. s., Ústí nad Labem
3; Klinika anesteziologie, perioperační, a intenzivní medicíny Univerzity, J. E. Purkyně, Masarykova nemocnice, KZ a. s., Ústí nad Labem
4
Vyšlo v časopise:
Cesk Slov Neurol N 2022; 85(5): 399-404
Kategorie:
Krátké sdělení
doi:
https://doi.org/10.48095/cccsnn2022399
Souhrn
Cíl: Cílem této práce bylo vyhodnocení bezpečnosti supracerebellárního transtentoriálního přístupu na našem souboru pacientů. Jedná se o technicky náročný přístup, který jsme využili při operacích zadní a střední mediotemporální oblasti, laterálního mezencefala a posteromediálního talamu. Soubor a metodika: Jedná se vyhodnocení souboru našich 8 pacientů operovaných supracerebellárním transtentoriálním přístupem v letech 2013–2021. V jednom případě se jednalo o anaplastický astrocytom, 3× o primooperaci glioblastoma multiforme, 1× difuzního středočárového H3K27M gliomu, 1× o operaci recidivy glioblastoma multiforme, 1× o operaci nízkostupňového gliomu a jednou jsme tímto přístupem operovali akutně prokrvácený kavernom lemniskálního trigona mesencefali. Všichni naši pacienti byli operováni v poloze v polosedě. Výsledky: 30denní mortalita v našem souboru je nulová. U pacientky s difuzním středočárovým H3K27M gliomem primárně operované v neurologicky těžkém stavu jsme museli provést časnou reoperaci stejným přístupem z důvodu prokrvácení rezidua tumoru. U našeho prvního pacienta s rozsáhlým mediotemporálním anaplastickým astrocytomem jsme museli po první době časně doplnit subokcipitální přístup ke zvýšení radikality resekce, po operaci měl horní kvadrantanopsii. U jednoho pacienta došlo k ischemii okcipitálního laloku z důvodu peroperačně pozorovatelné léze arteria cerebri posterior obklopené glioblastomem. Klinicky byla po operaci přítomna hemianopsie. Závěr: Jedná se o technicky náročný, přitom ale o bezpečný přístup. U lézí postihujících mediotemporální oblast je výhodný pro její střední a zadní část, ale při resekci lze dosáhnout anteriorně až k uncu a amygdale. Předpokládanou podmínkou je precizní znalost anatomie, na našem pracovišti pro tento přístup preferujeme polohu v polosedě. Důležitá je dostatečná likvorová dekomprese vypuštěním moku z cisterna magna ze separátní durální incize a šetrná manipulace s cévními strukturami tentoriální incisury.
Klíčová slova:
Amygdala – mozkový gliom – kavernom – hipokampus – supracerebellární přístup
Úvod
Supracerebellární transtentoriální přístup představuje alternativní možnost pro operaci mozkové léze v oblasti zadní a střední mediotemporální oblasti (hipokampu). Rozšíření operačního pole transcizí tentoria může být výhodné i pro dosažení laterálního mezencefala a posteromediálního talamu. Jedná se o technicky náročný přístup, jehož výhodou v případě resekce mediotemporálních (archikortikálních) struktur je šetření neokortexu. V našem krátkém sdělení hodnotíme naše zkušenosti s tímto přístupem.
Materiál a metodika
Na neurochirurgické klinice v Ústí nad Labem jsme v letech 2013–2021 operovali 8 pacientů supracerebellárním transtentoriálním přístupem. V jednom případě se jednalo o anaplastický astrocytom, 3× o primooperaci glioblastoma multiforme (GBM) (obr. 1), 1× o operaci recidivy GBM (obr. 2A), 1× difuzního středočárového H3K27M gliomu (obr. 2B), 1× o operaci nízkostupňového gliomu (low-grade glioma; LGG) u pacientky vysoce preferující aktivní chirurgický postup (obr. 3) a jednou jsme tímto přístupem operovali akutně prokrvácený kavernom lemniskálního trigona mesencefali (obr. 4). Všichni naši pacienti byli operováni v poloze v polosedě. Technika operace byla popsána v naší předchozí práci [1].
Fig. 1 Transtentorially-resected glioblastoma multiforme of the hippocampus in a 60-year-old male.
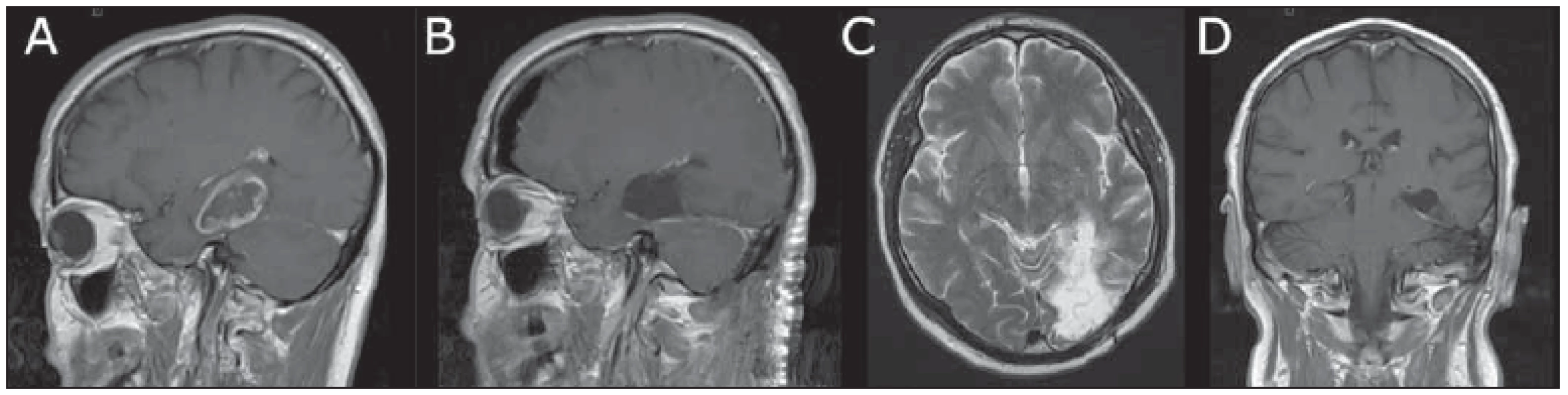
(A) Postcontrast T1WI sagittal MRI
before surgery; (B) postcontrast T1WI sagittal MRI early after surgery; (C) T2WI axial MRI one year after surgery showing an ischemic lesion in
the left basal occipital region due to injury of a small posterior cerebral artery branch; (D) postcontrast T1WI coronal MRI 1 year after surgery
showing a stable disease condition.
Fig. 2 Postoperative images of two
patients operated on by the transtentorial
approach.

(A) CT of a 39-year-old male after
glio blastoma multiforme recurrence surgery;
(B) T2WI MRI of a female with diff use midline
glioma H3K27M WHO IV located in the posteromedial
thalamus and mesencephalon after
two-stage resection and oncological
treatment.
Fig. 3 Images showing the course of treatment of a 34-year-old female with mesiotemporal low-grade glioma.
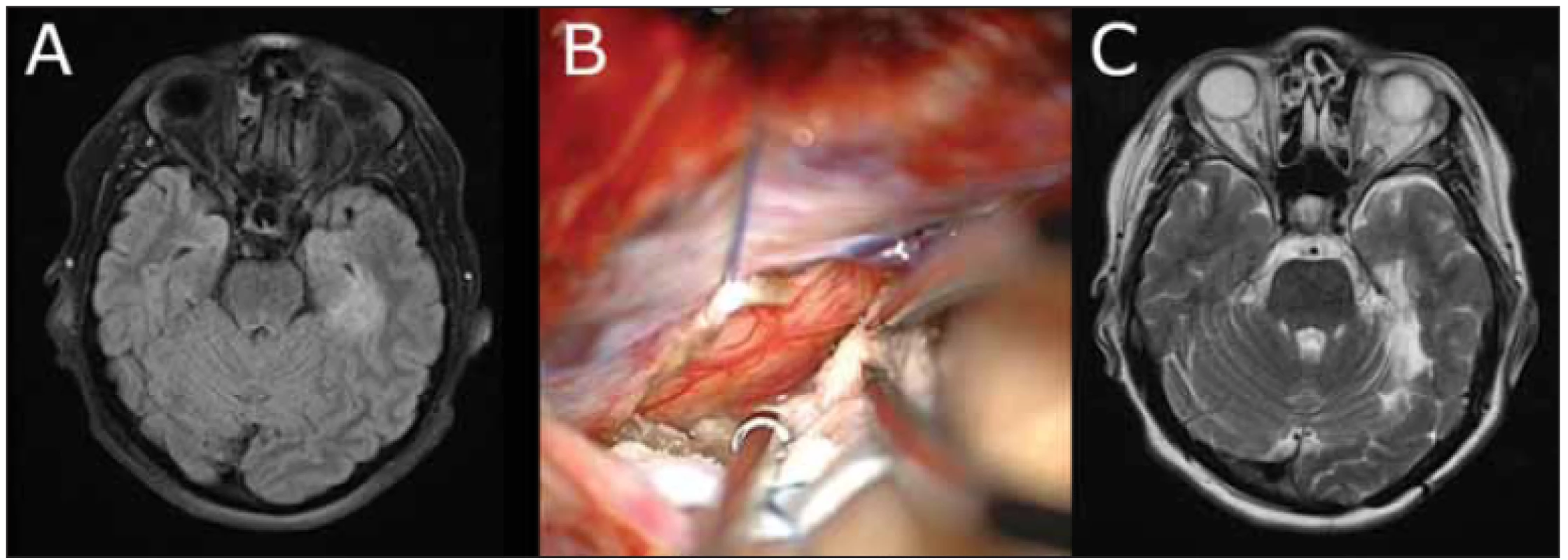
(A) FLAIR axial MRI
showing infi ltration of the middle third of the parahippocampal gyrus on the left; (B) transtentorial approach, lifting of the medial leaf of the
transected tentoria; (C) T2WI axial MRI 7 years after surgery showing radical resection; the patient did not undergo any oncological treatment.
FLAIR – fluid attenuated inversion recovery
Fig. 4 Images showing the course of treatment of a 48-year-old male with a cavernoma of the lemniscal trigone of the mesencephalon
and thalamus on the left after bleeding.
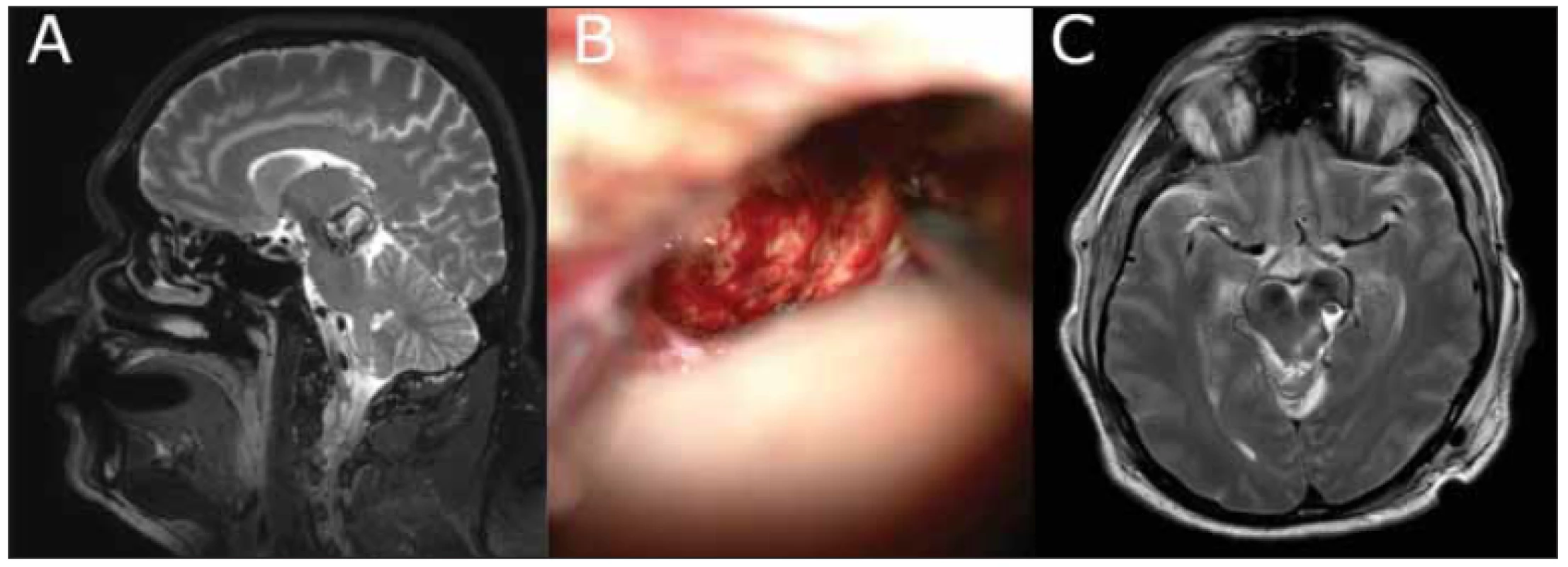
(A) T2WI sagittal MRI; (B) cavity after cavernous extirpation; via transtentorial approach, it was
possible to achieve the cranial aspect of the cavernoma; (C) T2WI axial MRI on day 2 after surgery showing the original localization of the cavernoma
behind the pyramidal tract and lateral to the nucleus ruber; the patient has no vision loss or motor deficits; he presents only with
residual contralateral tactile limb hypoesthesia.
Výsledky
Třicetidenní mortalita v našem souboru je nulová. U 18leté pacientky s difuzním středočárovým gliomem H3K27M v oblasti mezencefala a pulvinaru talamu, primárně operované v akutně těžkém neurologickém stavu, jsme museli provést časnou reoperaci stejným přístupem z důvodu prokrvácení rezidua tumoru několik hodin po zavedení ventrikuloperitoneálního shuntu 4. den po první operaci, a tím signifikantně zvýšit radikalitu resekce. Po operaci došlo ke zlepšení stavu, pacientka podstoupila onkologickou léčbu a byla schopna chůze s oporou. U dalšího mladého 39letého pacienta s recidivou GBM po 8 měsících byl prvním přístupem přední přístup – transsylvijský. Pooperační výsledek zobrazený na obr. 2A je výsledkem kombinace obou přístupů. Z transtentoriálního přístupu bylo možné dosáhnout až odstupu nervus oculomotorius. U našeho prvního operovaného v roce 2013, pacienta s rozsáhlým mediotemporálním anaplastickým astrocytomem, jsme museli po první době časně doplnit subokcipitální přístup ke zvýšení radikality resekce. Po operaci měl horní kvadrantanopsii, danou lézí Meyerovy kličky [1]. U jednoho pacienta s GBM došlo k ischemii okcipitálního laloku z důvodu peroperačně pozorovatelné léze arteria cerebri posterior (posterior cerebral artery; PCA) obklopené GBM, respektive jsme arterii museli cíleně obětovat, aby resekce byla radikální. Její pahýl jsme ošetřili hemoklipem. Klinicky byla po operaci přítomna hemianopsie (obr. 1). Tento pacient byl 1 rok po operaci po onkologické léčbě Stuppovým protokolem bez recidivy tumoru a plně funkční. U 3 pacientů byly na pooperační MR T2 difuzí vážených obrazech pozorovatelné změny mozečku (37,5 %), u všech však byly asymptomatické. U jedné pacientky jsme pozorovali drobný asymptomatický epidurální hematom v oblasti zadní jámy lební. U žádného z pacientů jsme nepozorovali ani přechodnou poruchu některého z okohybných nervů. Celková morbidita výkonu u našich pacientů je tedy dána poruchou zorného pole u 2 pacientů (25 %). Tři z 6 našich pacientů s vysokostupňovým gliomem, kteří byli operování tímto přístupem, přežili déle než 1 rok. U 3 pacientů s dobou přežití kratší jednoho roku byla průměrná doba přežití 8 měsíců (7–9 měsíců). Přístup umožnil u 6 pacientů radikální resekci léze (75 %) a u 2 pacientů jsme operaci hodnotili jako subtotální (25 %). Dále jsme se v naší praxi nesetkali se situací, kdy bychom u jiného pacienta transtentoriální přístup pro nemožnost manipulace s cílovými strukturami či obtíže spojené s kardiovaskulární nestabilitou nedokončili. Během operací jsme ani u jednoho pacienta nezaznamenali vzduchovou embolii.
Diskuze
Anatomicko-technické aspekty přístupu jsou zaznamenány srovnáním kadaverozní disekce přístupu s realitou na operačním sále (obr. 5A, B). Z paramediální incize provedeme standardní kraniotomii nad oblastí zadní jámy, přičemž tato kraniotomie kraniálně musí přesahovat zhruba 2 cm nad transverzální splav, ale kaudomediálně musí dosahovat na bazi mozečku k dosažení cisterna magna. Poté nejprve provedeme krátkou durotomii v kaudomediální části kraniotomie, vatičkou elevujeme mozeček a vypustíme likvor nástřihem arachnoidey cisterna magna. Tímto mozeček klesá bazálně a uvolňuje se tentoriální plocha mozečku. Pokud se prostor nad mozečkem v průběhu operace uzavírá, či máme pocit tenze mozečku, opakovaně zde likvor odsáváme. Alternativně můžeme do cisterny zavést krátkou drenážní hadičku a tu fixovat stehem (obr. 6A). Poté provádíme vlastní přístupovou durotomii, a to obloučkem pod transverzálním splavem (sinus transversus), s malou extenzí kaudálně. Subokcipitální plocha mozečku tedy zůstává chráněna, durální lalok vyvěšujeme kraniálně. Možné je i založení vyvěšujícího stehu přímo na zadní tentorium před transverzální splav (obr. 6B), jak to doporučuje Aaron Gadol [2]. Pokud operujeme na straně dominantního transverzálního splavu (častěji vpravo), můžeme jeho patenci po vyvěšení tvrdé pleny zkontrolovat pomocí intraoperační transkraniální dopplerometrie (iOP TCD) nebo fluorescenční venografie (ICG). Poté je důležitá snaha o zachování drénujících žil směřujících z horní plochy mozečku do tentoria, a proto je výhodný jednostranný paramediální přístup i možnost přítomné žíly dlouze uvolnit, a to i vytvořením durálního žilního rukávce (obr. 6B). Tím minimalizujeme riziko hemoragické infarzace mozečkové hemisféry. Horní plochu mozečku pak kryjeme chirurgickou vatou či gumou. Transcizi tentoria započínáme ideálně co nejblíže ke splavu, vstup přizpůsobujeme přítomnosti žil a eventuálních žilních lakun, bezpečně identifikujeme spodní plochu okcipitálního laloku, řez směřujeme anteromediálně a poté postupně transcidujeme celé tentorium až do incisury za eventuální koagulace či stázy hemoklipy. Cíp tentoria můžeme fixovat a retrahovat stehem nebo, jak navrhuje Michael Lawton, fixovat aneuryzmatickým klipem [3]. Tuto možnost a lokaci případného klipu v místě přišití laloku tentoria kraniálně naznačuje náš kadaverozní preparát (obr. 5A), v klinické praxi jsme používali vyvěšovací steh nebo retrakci tentoria koagulací, případně jeho širší vystřižení v celém přístupu do písmena „V“ se špičkou v incisuře. Při námi používaném ipsilaterálním transtentoriálním přístupu je výhodou, že laterální část tentoria tvoří přirozenou ochranu horní plochy mozečku a mediální část lze vyvěsit stehem nahoru (obr. 3B). Při použití hemoklipů lze okraj tentoria také i s nimi evertovat a tak udržet v otevřené poloze. Poté transcidujeme arachnoideu, identifikujeme a mobilizujeme nervus trochlearis a preparujeme PCA v jejím quadrigeminálním segmentu P3 (obr. 6C). Poté postupujeme preparací dále ventrálně na ambientní segment PCA. Takto se nám naskytne pohled na quadrigeminální a ambientní cisterny a posteriorní mediobazální oblast v rozsahu parahipokampálního (linguálního) a okcipitotemporálního gyru (fusiformního), mezi nimiž je sulcus collateralis (obr. 5A). Dosažitelné jsou též laterální tegmentální aspekt mezencefala a posteroinferiorní pulvinar talamu. Během resekce se dostáváme zespodu do temporálního rohu postranní komory za použití dlouhých bipolárních koagulačních pinzet či ultrasonického aspirátoru (CUSA). Naskýtá se nám tedy nezvyklý pohled na strop temporálního rohu postranní komory. Pozvolnou resekcí nádoru a koagulací hipokampálních a parahipokampálních tepének, kterou můžeme provádět i bezpečně subpiálně, poté postupujeme nejprve k inferiornímu choroidálnímu bodu. Někdy můžeme resekci zakončit po identifikaci arteria cerebri media (middle cerebral artery; MCA) a/nebo nervus oculomotorius [1] (obr. 6D). Tato vzdálenost je již extrémní a nepohodlná, např. Uğur Türe ale popisuje možnost nadzvednutí předního parahipokampálního gyru vatičkou, a to v případě jeho zastínění pyramidou [4]. V další práci se tým profesora Türeho zabývá MR morfometrickou studií vlivu tentoriálního úhlu na možnost dosažení přední části mediotemporální oblasti. Konstatují, že čím je tento úhel „strmější“, tím je transtentoriální přístup komplikovanější a v zákrytu za apexem pyramidy zůstává větší objem mozkové tkáně [5]. V další práci Türe využívá tento přístup pro resekce talamických lézí a uvádí jej jako jedinou možnost, pokud je cisterální povrch pulvinaru skryt pod spleniem corporis callosi – v tomto případě není možno využít posteriorní interhemisferický transtentoriální subspleniální přístup. Jako nevýhodu polohy v polosedě ale konstatuje nemožnost provedení intraoperační MR [6]. Během operování talamické léze je nutná bezpečná identifikace hlubokého žilního systému vč. průběhu vena basalis Rosenthali.
Fig. 5 Images comparing the cadaveric model of the supracerebellar transtentorial approach
on the left with a realistic setting in the operating room (also on the left).
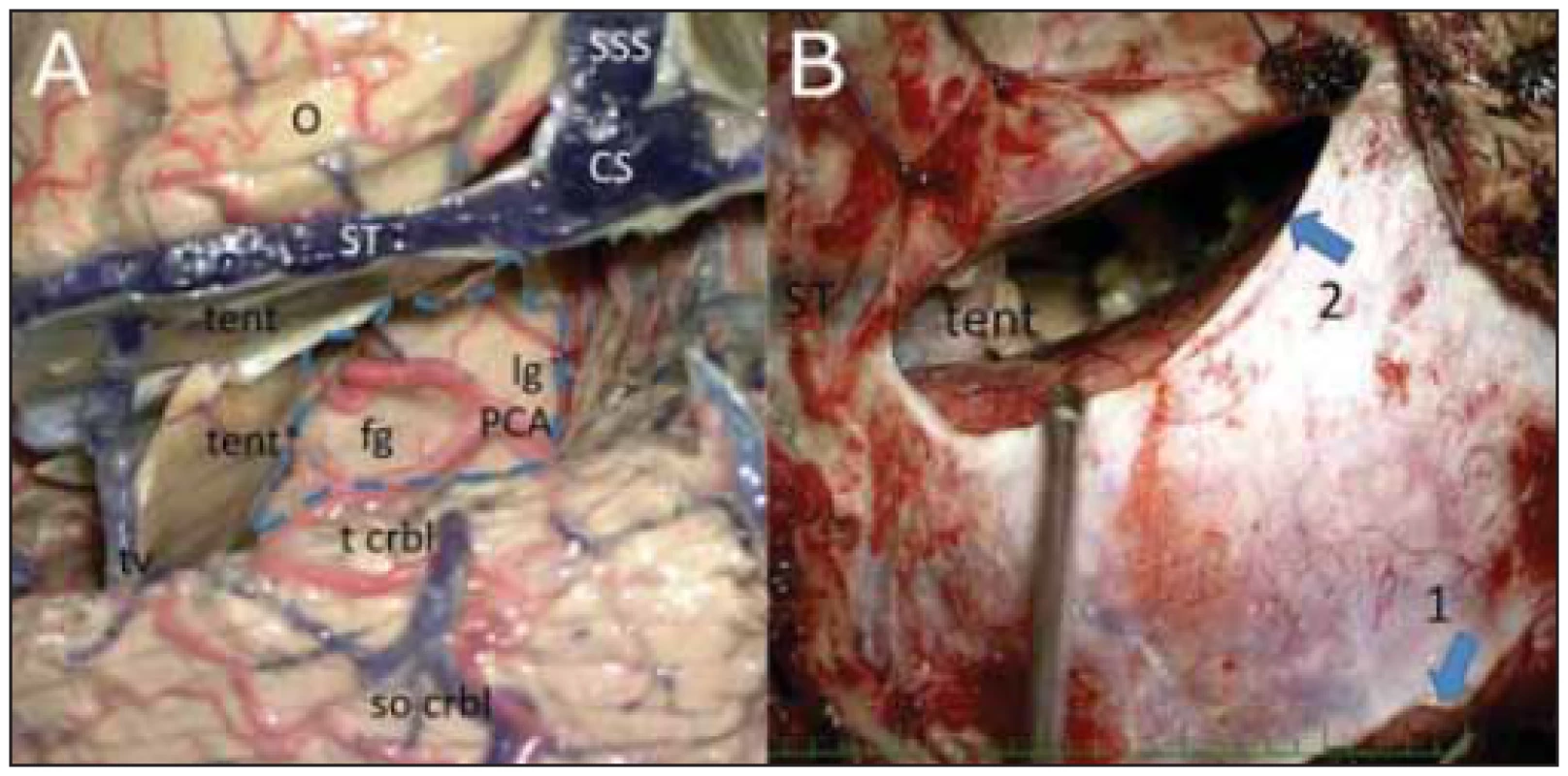
(A) Cadaveric
model; arteries were injected with the red silicone and the venous system with the
blue silicone. (B) Realistic setting in the operating room; the lower arrow (1) shows the drainage
approach to the cisterna magna; the upper arrow (2) shows the access durotomy; the
suboccipital surface of the cerebellum remains completely protected. The tent shows the
rest of the tentoria laterally; here the tentorium was cut into a „V“ and coagulated.
CS – confl uens sinuum; fg – gyrus fusiformis (occipitotemporalis); lg – gyrus lingualis (parahippocampus);
O – lobus occipitalis; PCA – posterior cerebral artery; SSS – sinus sagittalis superior;
ST – sinus transversus; so crbl – suboccipital surface of the cerebellum; t crbl – tentorial
surface of the cerebellum; tent – tentorium; tent * – tentorial fl ap lifted cranially by
a stitch (an alternative may be Lawton‘s aneurysmatic clip); tv – tentorial vein from the lateral
„upper“ surface of the cerebellum.
Fig. 6 Technical details of a glioblastoma multiforme recurrence resection by a left transtentorial approach.
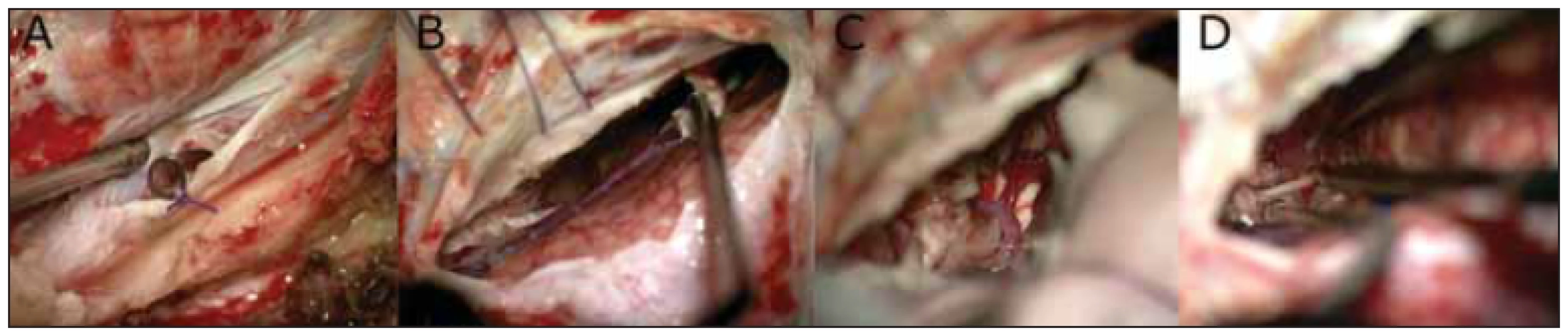
(A) Basal durotomy and positioning
of a drainage tube fixed by suture, enabling continuous outfl ow of cerebrospinal fl uid; (B) wide mobilization of the tentorial vein
with a dural sleeve cutout; a stitch lifting the dura anteriorly to the transverse sinus according to Aaron Gadol, which widens the field of view;
(C) view of the lateral mesencephalon, posterior cerebral artery and vena basalis Rosenthali after the transection of the tentoria; (D) reaching
the level of the oculomotor nerve; manipulation beyond this point gets more dangerous.
Tento přístup od Türeho přejal Niklaus Krayenbűhl z pracoviště v Zürichu, kde byl transtentoriální přístup do klinické praxe poprvé uveden (Yaşargil, Yonekava). Na souboru 17 selektivních amagdalohipokampektomií zjišťuje zejména riziko pooperačního výpadu perimetru, které hodnotí ve srovnání se sériemi standardních předních přístupů jako nízké, kdy u žádného z jeho pacientů k poruše perimetru nedošlo. Naopak 4 jeho pacienti (24 %) měli přechodnou okohybnou poruchu danou částečnou lézí nervus trochlearis (3×) a nervus oculomotorius (1×) [7]. Yonekava ve své původní práci z roku 2001 upozorňuje na možnost arytmií a bradykardie během tentoriální transcize, jejichž pravděpodobnou příčinu vzniku přičítá iritaci nervus trigeminus [8]. V našem souboru jsme se s tímto jevem nesetkali, ale doporučujeme o této možnosti informovat anesteziologa. Samozřejmou nutností je myslet na možnost vzduchové embolie v poloze v polosedě. Tato poloha je však pro daný transtentoriální přístup velice výhodná. Důkazem je fakt, že všichni autoři – kromě Aarona Gadola, který jako jediný preferuje „park-bench“ pozici [2] – provádějí tuto operaci v poloze v polosedě. Důležité jsou dostatečná likvorová dekomprese vypuštěním moku z cisterna magna ze separátní incize a šetrná manipulace s cévními strukturami tentoriální incisury. Tak lze předejít zejména poškození PCA.
Závěr
Supracerebellární transtentoriální přístup představuje miniinvazivní koridor pro dosažení mediobazálního temporálního komplexu nepoškozující přilehlé neokortikální struktury. Jedná se o technicky náročný, ale přitom o bezpečný přístup. U lézí postihujících mediotemporální oblast je velice výhodný pro její střední a zadní část, ale při resekci lze dosáhnout anteriorně až k oblasti uncu a amygdaly. Resekce v oblasti temporálního pólu, byť trajektorií možná, je již v našich rukách na hranici bezpečnosti a je lépe přístupy zkombinovat. Rozšíření operačního pole transcizí tentoria může být výhodné i pro dosažení laterálního mezencefala a posteromediálního talamu.
Etické aspekty
Studie nepodléhá schválení etickou komisí.
Grantová podpora
Tato práce byla částečně podpořena vnitřním granty KZ. a. s. IGA-KZ-2020-1-20 a IG8 – 217112009.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
MUDr. Robert Bartoš, Ph.D.
Neurochirurgická klinika
Univerzity J. E. Purkyně
Masarykova nemocnice, KZ a.s.
Sociální péče 3316/12A
400 11 Ústí nad Labem
e-mail: robert.bartos@kzcr.eu
Přijato k recenzi: 1. 7. 2022
Přijato do tisku: 5. 10. 2022
Zdroje
1. Bartoš R, Radovnický T, Orlický M et al. Kombinovaný paramediánní supracerebellární-transtentoriální a miniinvazivní suboccipitální přístup při resekci gliomu celé délky mediobazální temporální oblasti: anatomická studie, technické poznámky a kazuistika. Cesk Slov Neurol N 2014; 77/110 (3): 353–358.
2. Teton ZE, Hendricks BK, Marotta DA et al. Transtentorial approach to parahippocampal lesions: a technically challenging approach for preserving temporal lobe structures. World Neurosurg 2020; 142 : 626–635. doi: 10.1016/j.wneu.2020.07.092.
3. Baranoski JF, Bajaj A, Przybylowski CJ et al. Clip retraction of the tentorium: application of a novel technique for tentorial retraction during supracerebellar transtentorial approaches. J Neurosurg. 2020; 134 (3): 1198–1202. doi: 10.3171/2020.2.JNS192952.
4. Türe U, Harput MV, Kaya AH et al. The paramedian supracerebellar-transtentorial approach to the entire length of the mediobasal temporal region: an anatomical and clinical study. Laboratory investigation. J Neurosurg 2012; 116 (4): 773–791. doi: 10.3171/2011.12.JNS11791.
5. Lafazanos S, Türe U, Harput MV et al. Evaluating the importance of the tentorial angle in the paramedian supracerebellar-transtentorial approach for selective amygdalohippocampectomy. World Neurosurg 2015; 83 (5): 836–841. doi: 10.1016/j.wneu.2014.12. 042.
6. Serra C, Türe H, Yaltırık CK et al. Microneurosurgical removal of thalamic lesions: surgical results and considerations from a large, single-surgeon consecutive series. J Neurosurg 2020; 1–11. doi: 10.3171/2020.6.JNS20 524.
7. Serra C, Akeret K, Staartjes VE et al. Safety of the paramedian supracerebellar-transtentorial approach for selective amygdalohippocampectomy. Neurosurg Focus 2020; 48 (4): E4. doi: 10.3171/2020.1.FOCUS19 909.
8. Yonekawa Y, Imhof HG, Taub E et al. Supracerebellar transtentorial approach to posterior temporomedial structures. J Neurosurg 2001; 94 (2): 339–345. doi: 10.3171/jns.2001.94.2.0339.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2022 Číslo 5
-
Všechny články tohoto čísla
- Onemocnění bederní páteře – nová neurologická nemoc z povolání
- Karotický web
- Vývoj elektronického testu paměti pro starší osoby (ALBAV)
- Vlastnosti mikroflóry a rizikové faktory infekcí dolních cest dýchacích u pacientů se závažným kraniocerebrálním poraněním na jednotce intenzivní péče
- Výsledky rekonstrukčních operací lícního nervu
- Účinek sumatriptanu po simulovaném traumatickém poranění mozku u potkanů
- Supracerebellární transtentoriální přístup
- Gyrus dentatus – anatomie, cévní zásobení, funkce a neuropatologie
- Počítačově modelovaná kranioplastika z porózního polyethylenu v rizikovém terénu
- Kombinace Bickerstaffovy kmenové encefalitis se syndromem Guillain-Barrého
- Cenobamát
- Zemřel MUDr. Jan Pařízek
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Onemocnění bederní páteře – nová neurologická nemoc z povolání
- Cenobamát
- Karotický web
- Výsledky rekonstrukčních operací lícního nervu
