Detekce pravolevých zkratů u mladých pacientů po ischemické cévní mozkové příhodě – pilotní studie
Detection of Right-to-left Shunt in Young Patients after Ischemic Stroke – a Pilot Study
Aim:
The aim of the pilot study was to assess correlation between three diagnostic methods – contrast transesophageal echocardiography (cTEE), contrast transcranial Doppler (cTCD) and Flow detection system AnazenTM (FDS) – in detecting right-to-left shunts in young patients aged under 55 years with ischemic stroke or transient ischemic attack (TIA).
Patients and methods:
All consecutive patients presenting with acute ischemic stroke or TIA aged 18–55 years and able to perform sufficient Valsalva maneuver who signed informed consent were enrolled to the study from 8/2014 to 4/2015. Brain-computed tomography or magnetic resonance imaging as well as detection of right-to-left shunt using the cTEE, cTCD and FDS were performed in all patients after an onset of stroke/TIA. Correlations of the results between the methods and sensitivity, specificity, positive and negative predictive values of cTCD and FDS compared to cTEE as a gold standard were statistically evaluated.
Results:
In total, 30 patients (21 males, mean age 46.2 ± 8.5 years) were included in the study. Right-to-left shunt was detected in the same eight (26.7%) patients using the cTEE and cTCD, and in one additional patient (totally nine, 30.0%) using FDS. Spearman`s coefficient for cTEE and FDS was 0.92 and for cTEE and cTCD 1.00. Interclass correlation coefficient was 0.975. Sensitivity, specificity, positive and negative predictive values were 100%, 100%, 100%, 100%, respectively, for cTCD and 100%, 95.5%, 88.9%, 100%, respectively, for FDS.
Conclusion:
Correlation between cTCD and FDS as a new method with cTEE as a gold standard in right-to-left shunt detection appear to be high. Considering the ease of their use, both cTCD and FDS appear as suitable screening methods.
Key words:
stroke – right-to-left shunt – patent foramen ovale
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
M. Kuliha 1,2; M. Roubec 1; A. Goldírová 1,3; E. Hurtíková 1; J. Krajča 4; V. Procházka 4
; M. Kolek 5; R. Herzig 6; D. Školoudík 1–3
Působiště autorů:
Neurologická klinika LF OU a FN Ostrava
1; Neurologická klinika 1. LF UK a VFN v Praze
2; Ústav ošetřovatelství, FZV UP v Olomouci
3; Radiologický ústav, FN Ostrava
4; Kardiochirurgické centrum, FN Ostrava
5; Komplexní cerebrovaskulární centrum, Neurologická klinika LF UK a FN Hradec Králové
6
Vyšlo v časopise:
Cesk Slov Neurol N 2016; 79/112(5): 541-545
Kategorie:
Původní práce
doi:
https://doi.org/10.14735/amcsnn2016541
Souhrn
Cíl:
Cílem této pilotní studie bylo zhodnotit korelaci tří dostupných diagnostických metod v detekci pravolevých zkratů u mladých pacientů s ischemickou cévní mozkovou příhodou nebo tranzitorní ischemickou atakou (TIA) do 55 let věku, a to jícnovou echokardiografií s kontrastní látkou (cTEE), transkraniální dopplerovskou monitorací s kontrastní látkou (cTCD) a pomocí Flow Detection System – AnazenTM (FDS).
Materiál a metodika:
Všichni pacienti po proběhlé ischemické cévní mozkové příhodě nebo TIA ve věku 18–55 let schopní provést dostatečný Valsalvův manévr, kteří podepsali informovaný souhlas, byli zařazeni do studie od 8/2014 do 4/2015. U všech pacientů byla provedena výpočetní tomografie nebo magnetická rezonance mozku po iktu/TIA a vyšetření pravolevého zkratu pomocí cTEE, cTCD a FDS. Statisticky byly zhodnoceny korelace výsledků mezi metodami a senzitivita, specificita, pozitivní a negativní prediktivní hodnota cTCD a FDS oproti cTEE jako zlatému standardu.
Výsledky:
Do studie bylo celkem zařazeno 30 pacientů (21 mužů, průměrný věk 46,2 ± 8,5 let). Pravolevý zkrat byl detekován u osmi (26,7 %) stejných pacientů pomocí cTEE a cTCD, a u jednoho dalšího pacienta (celkem devět, 30,0 %) pomocí FDS. Spearmanův koeficient shody mezi cTEE a FDS byl 0,92, mezi cTEE a cTCD 1,00. Interclass correlation coefficient byl 0,975. Senzitivita, specificita, pozitivní a negativní prediktivní hodnota byly 100 %, 100 %, 100 %, 100 % pro cTCD a 100 %, 95,5 %, 88,9 %, 100 % pro FDS.
Závěr:
Korelace cTCD a FDS jako nové metody se zlatým standardem cTEE v detekci pravolevých zkratů se jeví vysoká. Obě metody, cTCD a FDS, se vzhledem k jednoduchosti provedení ukazují jako ideální skríningové metody.
Klíčová slova:
cévní mozková příhoda – pravolevý zkrat – foramen ovale patens
Úvod
Cévní mozkové příhody (CMP) patří k nejčastějším příčinám mortality, morbidity a invalidizace populace ve vyspělých zemích [1,2]. Nejběžnějším typem CMP jsou ischemické CMP (iCMP), které tvoří okolo 80–90 % všech mozkových příhod. Nejčastěji příčinou iCMP je akutní okluze mozkové tepny, kterou lze prokázat v prvních 3–6 hod od vzniku příznaků u více než 80 % pacientů. Závažnost prognózy iCMP dokumentuje 30denní mortalita, která se pohybuje mezi 10 a 17 %, u pacientů s rozsáhlou ischemií až 75 % [2]. Plně soběstačných po třech měsících je pak pouze asi 30 % pacientů [2]. Dle literatury je 20–50 % všech iCMP kardioembolické etiologie [1], kdy k embolizaci dochází buď z levého srdce (zde etiologicky převažuje fibrilace síní) nebo tzv. paradoxní embolizací při pravolevých zkratech, a to nejčastěji na podkladě foramen ovale patens (PFO), vzácněji při defektu septa síní. Výjimečně se může jednat o extrakardiální pravolevé zkraty v plicním řečišti [2,3].
Prevalence PFO v populaci je uváděna mezi 19 a 36 %, ale v populaci pacientů s iCMP mladších 55 let je uváděna až 44–66 % [3,4]. U pacientů s tzv. kryptogenní etiologií iCMP je PFO diagnostikováno až šestkrát častěji než u pacientů se známou etiologií iCMP [5]. U pacientů s kryptogenní etiologií iCMP, kterým bylo diagnostikováno PFO, je toto až ve 2/3 považováno za příčinu proběhlého iktu [6]. Další onemocnění, u kterých je PFO diagnostikováno častěji než v běžné populaci, jsou migréna a syndrom spánkové apnoe [7–9].
Za zlatý standard v diagnostice PFO je považována jícnová echokardiografie s podáním echokontrastní látky obsahující mikrobubliny (cTEE) se senzitivitou a specificitou pro záchyt PFO blížící se 100 % [10–12]. Limitací této metody je spolupráce pacienta a schopnost tolerovat zavedení jícnové sondy.
Alternativní metodou s vysokou senzitivitou (96,8–98,0 %) a specificitou (78,4–98,0 %) je transkraniální dopplerometrie s podáním kontrastní látky (tzv. bublinkový test [cTCD]) [13–15]. Tato metoda je navíc schopna diagnostikovat i extrakardiální pravolevé zkraty [16–18]. Vyšetření cTCD může dle literatury zachytit ve srovnání s cTEE více pravolevých zkratů než cTEE v důsledku záchytu extrakardiálních zkratů [14,15,18], senzitivita cTCD je referována dokonce vyšší než u cTEE i během normálního dýchání [13].
Novou metodou diagnostiky pravolevých zkratů je tzv. Flow Detection System – AnazenTM (FDS). Jedná se o systém vyvinutý k identifikaci pravolevých zkratů za použití fluorescenční kontrastní látky (Idiocyanin Green; ICG), která je následně detekována infračervenou spektrofotometrií za pomoci senzoru umístěného na uchu vyšetřovaného pacienta. Cirkulační čas podané kontrastní látky je měřen FDS systémem a graficky zobrazen. Typ křivky určuje přítomnost pravolevého zkratu, a to jak nitrosrdečního (např. PFO), tak i extrakradiálního. Senzitivita a specificita FDS vůči TEE je uváděna v rozmezí 90–95 % [19].
Všechny tři uvedené metody k detekci pravolevých zkratů využívají Valsalvův manévr (VM). Avšak jedině u FDS je VM měřen a jeho dostatečnost graficky vyhodnocena přístrojem s možností nácviku VM ještě před samotným zahájením vyšetření. U metody cTCD je možno pouze odhadnout suficienci prováděného manévru pomocí poklesu TCD křivky z a. cerebri media.
Cílem této pilotní studie bylo zhodnotit korelaci těchto tří dostupných diagnostických metod v detekci pravolevých zkratů u mladých pacientů s iCMP do 55 let věku.
Pacienti a metodika
Pacienti
Do studie byli v průběhu devíti měsíců (srpen 2014 až duben 2015) zařazeni pacienti po iCMP nebo tranzitorní ischemické atace (TIA) ve věku 18–55 let, kteří podepsali informovaný souhlas. Vylučujícími kritérii byla kontraindikace nebo nemožnost provedení cTEE, cTCD, FDS nebo neschopnost provést dostatečný VM.
Všichni pacienti měli provedeno zobrazovací vyšetření mozku pomocí výpočetní tomografie nebo magnetické rezonance a neurologické vyšetření s potvrzením diagnózy iCMP nebo TIA. U všech pacientů byl zaznamenáván výskyt jakýchkoli nežádoucích účinků v průběhu jednotlivých vyšetření (cTEE, cTCD a FDS) a těsně po nich.
Studie byla provedena ve shodě s Helsinskou deklarací z roku 1975 (revize 2004 a 2008) a schválena lokální etickou komisí (MZ10-FNO 658/2014). Studie byla registrována na www.clinicaltrials.gov (NCT02331076).
Provedení jícnové echokardiografie s podáním echokontrastní látky obsahující mikrobubliny
K provedení cTEE byl použit echokardiografický přístroj Philips CX50 nebo Philips iE33 (Philips Healthcare, Andover, MA, USA) a jícnová sonda X7-2t. Při intoleranci jícnové sondy byl k lehké až střední sedaci použit intravenózně (i.v.) midazolam 1–5 mg s titrací dávky dle klinického efektu.
Zobrazení síňového septa (event. PFO) bylo provedeno z proximální jícnové bikavální projekce (mezi 90 a 110), vizualizace a kvantifikace pravolevého zkratu pak pomocí echokontrastní látky. Jako echokontrastní látka bylo použito 9 ml koloidního roztoku s 1 ml vzduchu, aktivovaného desetkrát ve dvou injekčních stříkačkách spojených trojcestným kohoutem. Následně byla kontrastní látka aplikována bolusově i.v. cestou kubitální žíly. Dvě aplikace echokontrastní látky byly provedeny za klidových podmínek s normálním dýcháním, dvě aplikace s následným VM, který byl zahájen vždy až po dosažení kontrastní náplně v pravé síni, s trváním více než 5 s.
Diagnóza pravolevého zkratu byla stanovena při vizualizaci průniku mikrobublin ve formě vysokointenzních signálů (High-Intensity Transient Signal; HITS) cestou PFO z pravé do levé síně za klidových podmínek nebo po VM (během prvních tří srdečních cyklů po dosažení opacifikace pravé síně/VM). Kvantifikace pravolevého zkratu: grade 0 = 0 HITS, grade I = 1–10 HITS, grade II = 11–20 HITS, grade III > 20 HITS. Vyšetření prováděl zkušený echokardiografista s 10–11 lety praxe.
Provedení transkraniální dopplerometrie s podáním kontrastní látky
Vyšetření byla provedena dle modifikovaného Spencerova protokolu [14]. Pacient byl vleže na zádech vyšetřen duplexní transkraniální 2 MHz sondou SP2730 na přístroji Esaote MyLab Twice (Esaote, Janov, Itálie). Dopplerovský signál byl monitorován z pravé střední mozkové tepny během klidného dýchání a následně i během VM. Jako kontrastní látka bylo podáno 9 ml aktivovaného fyziologického roztoku s 1 ml vzduchu a 0,3 ml pacientovy venózní krve. Aktivace byla provedena 10krát ve dvou injekčních stříkačkách spojených trojcestným kohoutem. Kontrastní látka byla aplikována bolusově i.v. cestou kubitální žíly. Vyšetření bylo provedeno dvakrát během klidného dýchání a dvakrát během VM. Za dostatečný byl VM považován při poklesu maximální průtokové rychlosti v a. cerebri media o 25 % oproti klidovému stavu. V dopplerovském modu byl sledován výskyt HITS během 30 s. Jako pravolevý zkrat byl hodnocen výskyt více než 5 HITS během prvních 20 s od podání kontrastní látky. Kvantifikace pravolevého zkratu – grade 0 = 0 HITS, grade I = 1–10 HITS, grade II = 11–50 HITS, grade III > 50 HITS. Vyšetření prováděl zkušený neurosonografista s osmi lety praxe.
Provedení vyšetření pomocí Flow Detection System – AnazenTM
Pacient byl vsedě vyšetřen systémem AnazenTM Flow Detection System s použitím Anazen FDS jednorázového vyšetřovacího kitu (Anazen, Cardiox Corporation, Columbus, Ohio, USA). Během VM byla do periferní žíly podána fluorescenční látka ICG v koncentraci 5 mg/ml. Vyšetření bylo provedeno dvakrát během VM, interval mezi oběma měřeními byl 9 min. Každé vyšetření bylo zahájeno výdechem do FDS trubice s vyhodnocením VM během vyšetření. FDS po dosažení suficientního VM indikoval zahájení aplikace bolu 2 ml ICG a automaticky ukončil VM s následným, 1 min trvajícím FDS měřením pomocí FDS ušních detektorů, které byly umístěny na vrcholy obou uší vyšetřovaného pacienta. Křivka ICG byla vyhodnocena dle kritérií AnazenTM [19] s následným grafickým a procentuálním zobrazením pravolevého zkratu. Vyšetření prováděla vyškolená sestra a lékař-neurolog.
Statistická analýza
Demografická data jsou uvedena jako počet a percentuální zastoupení. Za pacienty s PFO byli považováni jen pacienti, u nichž byl pravolevý zkrat prokázán všemi třemi metodami. Pro porovnání skupin v kvalitativním znaku byl použit Fisherův přesný test. Korelace mezi hodnocením PFO všemi třemi metodami byla provedena pomocí koeficientu vnitrotřídní korelace (interclass correlation coefficient). Pro korelaci cTCD a FDS s cTEE jako zlatým standardem byl použit Spearmanův korelační koeficient. Dále byly určeny senzitivita, specificita, pozitivní a negativní prediktivní hodnota pro cTCD a FDS, přičemž pro definitivní diagnózu PFO byla potřebná shoda minimálně dvou diagnostických metod. Všechny statistické testy byly provedeny na hladině signifikance p ≤ 0,05. Ke statistickému zpracování byl použit statistický software IBM SPSS Statistics 22.
Výsledky
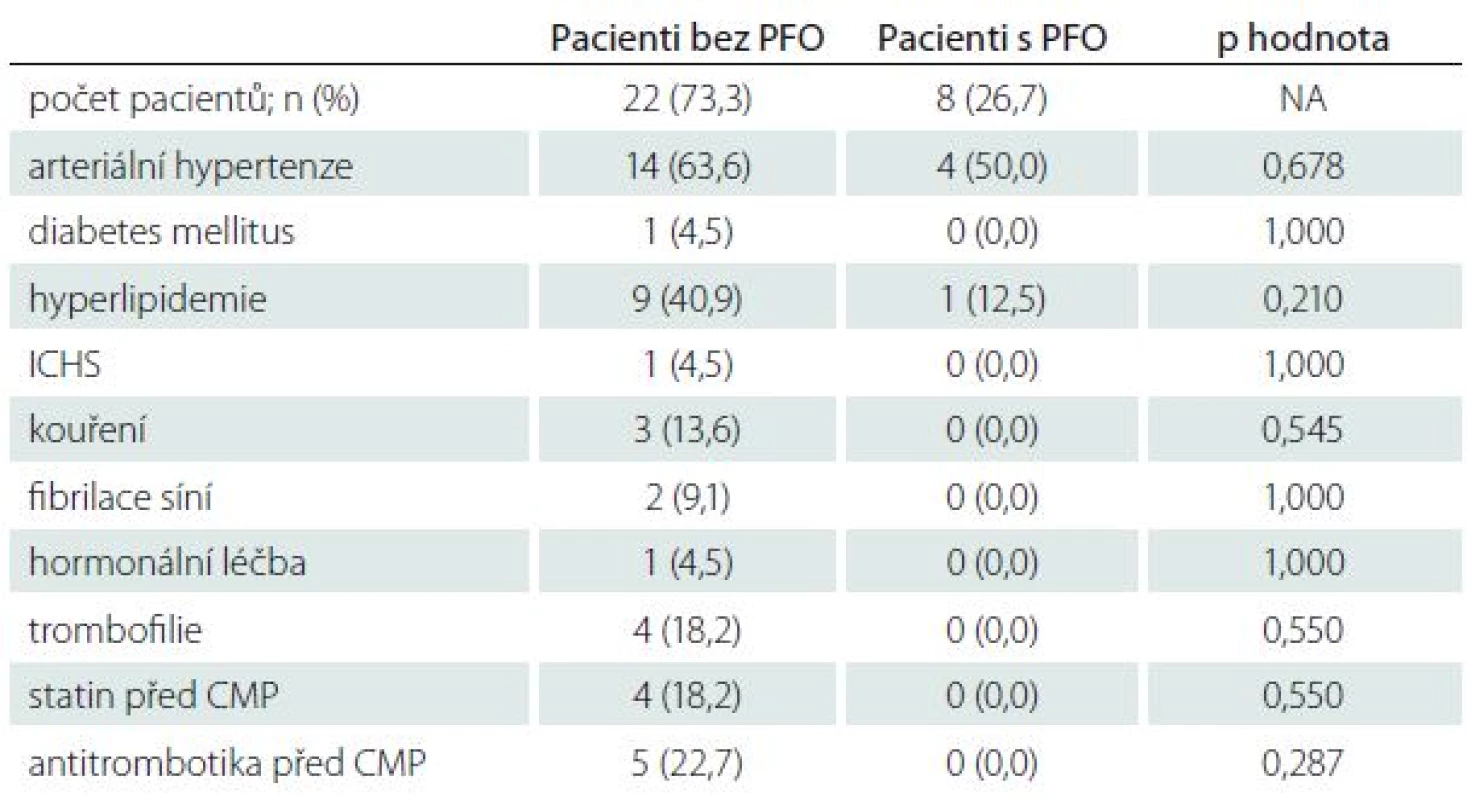
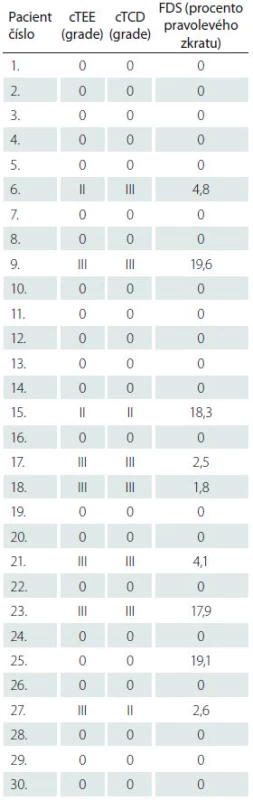
Do studie bylo celkem zařazeno 30 pacientů (21 mužů, průměrný věk 46,2 ± 8,5 let). Demografické údaje jsou uvedeny v tab. 1. Pravolevý zkrat byl detekován u osmi (26,7 %) pacientů pomocí cTEE, u osmi (26,7 %) shodných pacientů pomocí cTCD a u devíti (30,0 %) pacientů pomocí FDS – kromě osmi pacientů diagnostikovaných již dříve zmíněnými metodami se jednalo o jednoho dalšího pacienta (tab. 2).
Spearmanův korelační koeficient mezi cTEE a FDS byl 0,92, mezi cTEE a cTCD 1,0. Interclass correlation coefficient byl 0,975. Senzitivita, specificita, pozitivní a negativní prediktivní hodnota pro cTCD byly 100 %, 100 %, 100 %, 100 % a pro FDS 100 %, 95,5 %, 88,9 %, 100 %. Nebyly zaznamenány žádné nežádoucí účinky nebo komplikace u cTEE, cTCD ani FDS vyšetření.
Diskuze
V naší studii jsme prokázali PFO pomocí cTCD a cTEE u osmi (26,7 %) a pomocí metody FDS u devíti (30 %) z 30 pacientů po proběhlé iCMP nebo TIA do 55 let věku. Procento záchytu PFO u mladých pacientů po iCMP bylo ve dříve provedených studiích [3,4] vyšší (dosahovalo až 66 %), tyto studie však zahrnovaly mnohonásobně vyšší počet subjektů. V případě naší pilotní studie se tak může jednat o chybu malých čísel. Výsledek FDS u pacienta, kde cTCD i cTEE byly negativní, považujeme za falešně pozitivní, protože i v případě extrakardiálního pravolevého zkratu by tento měl být zachycen taktéž metodou cTCD [16–18].
V naší studii byla korelace všech tří metod (cTCD, cTEE a FDS) vysoká, senzitivita i specifita cTCD vůči cTEE byla 100%, u FDS 100% a 95,5%. Také již v minulosti provedené studie zabývající se korelací cTEE a cTCD prokázaly velmi dobrou senzitivitu (96,8–98 %) a specifitu (78,4–98 %) těchto dvou metod v diagnostice pravolevých zkratů [13–15]. FDS byla doposud testována vůči cTEE a cTCD pouze v populaci pacientů bez CMP, kde senzitivita a specifita FDS vůči cTEE byly 95 a 90 % a v případě FDS vůči cTCD pak 86 a 82 % [19].
Záchyt pravolevého zkratu v klidovém stavu je o 26–28 % nižší než při použití VM [15]. K co nejpřesnějšímu záchytu pravolevého zkratu je tedy nutný suficientní VM. Nicméně přesné měření a kalibraci tohoto manévru umožňuje pouze metoda FDS. U cTCD lze odhadnout dostatečnost VM pomocí poklesu PVS při TCD monitoraci a. cerebri media. Použití sedace u cTEE může naopak schopnost provést suficientní VM negativně ovlivnit.
Provedení cTCD i cTEE vyžaduje zkušené lékaře-specialisty a jejich dostupnost, zejména mimo větší centra, může být limitována. FDS oproti tomu představuje potenciálně dobře dostupnou metodu, kterou je schopna provést i vyškolená zdravotní sestra.
Léčba PFO není v platných doporučeních dosud jasně stanovena. Může se pohybovat od konzervativní léčby bez opatření a medikace, přes konzervativní léčbu s medikací antiagregační nebo antikoagulační, až po léčbu intervenčně-kardiologickou – endovaskulární okluzí PFO pomocí okludéru. Nejběžněji je okluze PFO indikována tehdy, pokud je prokázána paradoxní embolizace do mozku, tedy nejčastěji u pacientů po proběhlé iCMP/TIA nebo alespoň při nálezu postischemických změn na magnetické rezonanci mozku. Dalšími kritérii jsou věk pacienta a absence jiné etiologie CMP a současný průkaz pravolevého zkratu přes PFO.
Jasná indikační kritéria pro endovaskulární okluzi PFO však neexistují a dle provedených klinických studií a jejich metaanalýz není ani zcela jasný benefit endovaskulární okluze PFO oproti medikamentózní terapii. Studie CLOSURE [20], RESPECT [21] a PC-Trial [22] prokázaly v průměru úspěšnost implantace v 93,8 %, vaskulární komplikace výkonu byly přítomny průměrně v 1,13 %, k rozvoji CMP/TIA došlo ve skupině s okluzí PFO v průměru v 3,7 % oproti 5,3 % ve skupině pacientů léčených konzervativně. Subanalýza pro opakovaný výskyt CMP/TIA vyšla lehce lépe ve skupině s okluzí PFO (3,6 %) oproti skupině pacientů léčených konzervativně (5,8 %), nicméně tento rozdíl nebyl statisticky signifikantní. Hlavní limitací uvedených studií byla zejména velmi různorodá medikamentózní strategie u pacientů léčených konzervativně, další výraznou limitací byla absence dlouhodobého sledování obou skupin pacientů (pacienti byli sledováni v průměru 2–4 roky) [23]. V multicentrickém registru PRECISE, do kterého byly zařazeni pacienti po CMP či TIA s prokázaným pravolevým zkratem, bylo sledováno 267 pacientů po okluzi PFO, kdy v průměrné době sledování 11 měsíců nedošlo k žádné CMP či TIA. Limitací zde byla absence kontrolní skupiny a krátká doba sledování po okluzi PFO [24]. Potřeba hledat optimální řešení pro pacienty s PFO, zejména pokud prodělali CMP/TIA, zůstává nadále aktuální, protože, jak již bylo uvedeno výše, jedná se především o mladé pacienty, kteří se tedy budou v riziku recidivy CMP/TIA nacházet velmi dlouho.
Prezentovaná studie byla navržena jako pilotní, proto její hlavní limitaci představuje malý počet zařazených pacientů. Další důležitou limitací v porovnávání uvedených metod je kalibrace provádění VM, která byla v našem případě použita jen u metody FDS. Pouze u cTEE pak byla použita sedace.
Závěrem lze konstatovat, že korelace metod cTCD a FDS (jako nové metody) při detekci pravolevého zkratu se zlatým standardem cTEE se jeví vysoká. Vyšetření cTCD a FDS se tak vzhledem k jednoduchosti provedení ukazují jako ideá
Podpořeno Institucionální podporou MZ ČR na základě rozhodnutí č.1 RVO-FNOs/2014.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Martin Kuliha
Neurologická klinika
LF OU a FN Ostrava
17. listopadu 1790
708 00 Ostrava
e-mail: martin.kuliha@email.cz
Přijato k recenzi: 9. 2. 2016
Přijato do tisku: 4. 3. 2016
Zdroje
1. Feigin VL, Lawes CM, Bennett DA, et al. Stroke epidemiology: a review of population-based studies of incidence, prevalence, and case-fatality in the late 20th century. Lancet Neurol 2003; 2 (1): 43–53.
2. Rosamond W, Flegal K, Furie K, et al. Heart disease and stroke statistics – 2008 update: a report from the American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Circulation 2008; 117 (4): e25–146.
3. Hagen PT, Scholz DG, Edwards WD. Incidence and size of patent foramen ovale during the first 10 decades of life: an autopsy study of 965 normal hearts. Mayo Clin Proc 1984; 59 (1): 17–20.
4. McGaw D, Harper R. Patent foramen ovale and cryptogenic cerebral infarction. Intern Med J 2001; 31 (1): 42–7.
5. Overell JR, Bone I, Lees KR. Interatrial septal abnormalities and stroke: a meta-analysis of case-control studies. Neurology 2000; 55 (8): 1172–9.
6. Alsheikh-Ali AA, Thaler DE, Kent DM. Patent foramen ovale in cryptogenic stroke: incidental or pathogenic? Stroke 2009; 40 (7): 2349–55. doi: 10.1161/STROKEAHA.109.547828.
7. Anzola GP, Magoni M, Guindani M, et al. Potential source of cerebral embolism in migraine with aura: a transcranial Doppler study. Neurology 1999; 52 (8): 1622–5.
8. Sztajzel R, Genoud D, Roth S, et al. Patent foramen ovale, a possible cause of symptomatic migraine: a study of 74 patients with acute ischemic stroke. Cerebrovasc Dis 2002; 13 (2): 102–6.
9. Mojadidi MK, Bokhoor PI, Gevorgyan R, et al. Sleep apnea in patients with and without a right-to-left shunt. J Clin Sleep Med 2015; 11 (11): 1299–304. doi: 10.5664/jcsm.5190.
10. Schneider B, Zienkiewicz T, Jansen V, et al. Diagnosis of patent foramen ovale by transesophageal echocardiography and correlation with autopsy findings. Am J Cardiol 1996; 77 (14): 1202–9.
11. Hausmann D, Mügge A, Becht I, et al. Diagnosis of patent foramen ovale by transesophageal echocardiography and association with cerebral and peripheral embolic events. Am J Cardiol 1992; 70 (6): 668–72.
12. Pearson AC, Labovitz AJ, Tatineni S, et al. Superiority of transesophageal echocardiography in detecting cardiac source of embolism in patients with cerebral ischemia of uncertain etiology. J Am Coll Cardiol 1991; 17 (1): 66–72.
13. Caputi L, Carriero MR, Falcone C, et al. Transcranial Doppler and transesophageal echocardiography: comparison of both techniques and prospective clinical relevance of transcranial Doppler in patent foramen ovale detection. J Stroke Cerebrovasc Dis 2009; 18 (5): 343–8. doi: 10.1016/j.jstrokecerebrovasdis.2008.12.001.
14. Spencer MP, Moehring MA, Jesurum J, et al. Power m-mode transcranial Doppler for diagnosis of patent foramen ovale and assessing transcatheter closure. J Neuroimaging 2004; 14 (4): 342–9.
15. González-Alujas T, Evangelista A, Santamarina E, et al. Diagnosis and quantification of patent foramen ovale. Which is the reference technique? Simultaneous study with transcranial Doppler, transthoracic and transesophageal echocardiography. Rev Esp Cardiol 2011; 64 (2): 133–9. doi: 10.1016/j.recesp.2010.10.009.
16. Chimowitz MI, Nemec JJ, Marwick TH, et al. Transcranial Doppler ultrasound identifies patients with right-to-left cardiac or pulmonary shunts. Neurology 1991; 41 (12): 902–4.
17. Di Tullio M, Sacco RL, Massaro A, et al. Transcranial Doppler with contrast injection for the detection of patent foramen ovale in stroke patients. Int J Card Imaging 1993; 9 (1): 1–5.
18. Jauss M, Kaps M, Keberle M, et al. A comparison of transesophageal echocardiography and transcranial Doppler sonography with contrast medium for detection of patent foramen ovale. Stroke 1994; 25 (6): 1265–7.
19. Clinical Study Reports CDX-1119,1187 REV.B-D. Cardiox Shunt Detection Technology Study. Dublin: Cardiox Corporation 2012.
20. Furlan AJ, Reisman M, Massaro J, et al. Closure or medical therapy for cryptogenic stroke with patent foramen ovale. N Engl J Med 2012; 366 (11): 991–9. doi: 10.1056/NEJMoa1009639.
21. Carroll JD, Saver JL, Thaler DE, et al. Closure of patent foramen ovale versus medical therapy after cryptogenic stroke. N Engl J Med 2013; 368 (12): 1092–100. doi: 10.1056/NEJMoa1301440.
22. Meier B, Kalesan B, Mattle HP, et al. Percutaneous closure of patent foramen ovale in cryptogenic embolism. N Engl J Med 2013; 368 (12): 1083–91. doi: 10.1056/NEJMoa1211716.
23. Nagaraja V, Eslick GD. Stroke prevention by percutaneous closure of patent foramen ovale: a meta-analytic review. Int J Cardiol 2014; 172 (2): 524–6. doi: 10.1016/j.ijcard.2014.01.026.
24. Wöhrle J, Bertrand B, Søndergaard L, et al. PFO closuRE and CryptogenIc StrokE (PRECISE) registry: a multi-center, international registry. Clin Res Cardiol 2012; 101 (10): 787–93.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2016 Číslo 5
-
Všechny články tohoto čísla
- Rasmussenova encefalitída
- Jsou nemotorické projevy Parkinsonovy nemoci indikací k léčbě pomocí hluboké mozkové stimulace subthalamických jader?
- Jsou nemotorické projevy Parkinsonovy nemoci indikací k léčbě pomocí hluboké mozkové stimulace subthalamických jader?
-
Komentář ke kontroverzím
Hluboká mozková stimulace u Parkinsonovy nemoci – revize indikačních kritérií? - Léky navozená spánková endoskopie – cesta k lepším chirurgickým výsledkům při léčbě syndromu obstrukční spánkové apnoe
- Současná kortikoterapie u nádorů mozku
- Individualizovaný přístup k léčbě roztroušené sklerózy
- Aktuální pohled na management nízkostupňových gliových nádorů centrálního nervového systému
- Detekce pravolevých zkratů u mladých pacientů po ischemické cévní mozkové příhodě – pilotní studie
- Myxovirus resistance protein A v terapii interferony-β u pacientů s roztroušenou sklerózou a algoritmus sledování účinnosti léčby
- Myasténia gravis asociovaná s tymómom – súbor pacientov v Slovenskej republike (1978–2015)
- Bezpečnost karotického stentingu – srovnání protekčních systémů
-
Komentář k článku Pavlík et al
Bezpečnost karotického stentingu – srovnání protekčních systémů - Průkaz boreliové DNA u pacientů s neuroboreliózou
- Vztah likvorových hladin IL-6 ke změnám parciálního tlaku kyslíku v mozku a k rozvoji vazospazmů u pacientů po subarachnoidálním krvácení z ruptury aneuryzmatu mozkové tepny
- Stereotaktické biopsie mozkových patologií systémem Varioguide – zkušenosti ze 101 výkonů
- Myasthenia Gravis Composite – validace české verze
- Pilotní studie využití tenzometrické plošiny v domácí terapii poruch rovnováhy
- Neurofyziologická vyšetření u traumatických lézí brachiálního plexu
-
Komentář k článku Vaško et al
Neurofyziologická vyšetření u traumatických lézí brachiálního plexu - Paroxyzmálna kinezigénna dystónia ako primomanifestácia roztrúsenej sklerózy – kazuistika
- Idiopatická hypertrofická kraniální pachymeningitida – dvě kazuistiky
- Metodika stanovení smrti mozku pomocí transkraniální sonografie vypracovaná Neurosonologickou komisí a Cerebrovaskulární sekcí České neurologické společnosti ČLS JEP
- Webové okénko
-
Analýza dat v neurologii
LIX. Koncept atributivního rizika v analýze populačních studií – VI. Kauzalita vztahů
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Současná kortikoterapie u nádorů mozku
- Rasmussenova encefalitída
- Neurofyziologická vyšetření u traumatických lézí brachiálního plexu
- Průkaz boreliové DNA u pacientů s neuroboreliózou
