Protilátky CGRP v profylaktické léčbě migrény
CGRP antibodies in the prophylactic treatment of migraine
Aim: In this study, we retrospectively evaluate our center patients on the biological treatment of migraine with CGRP antibodies used after full reimbursement approval from March to the end of 2020. Only patients receiving erenumab and fremanezumab were enrolled, as galcanezumab was not approved until October 2020. Patients and methods: The sample consists of 130 patients, including 118 women (90.8%) and 12 men (9.2%) with an average age of 46.2 (21–76) years. The primary objective was to evaluate the effect of therapy at 3, 6, 9, and 12 months, the number of non-responders (monthly migraine day [MMD] reduction lower than 50%), reduction of acute medication overuse (MOH) days, relationship to disease duration, number of previous prophylaxes, migraine in family history (FH) and comorbidities. The incidence of adverse events (AE) was monitored. Results: The average number of MMD before treatment was 12.2. After 3 months, the MMD decreased by 60.5% (to 4.7), and in the following months, the effectiveness increased even further to more than 70%; greater effectiveness was achieved in chronic migraine (CM) compared to episodic (EM). After 12 months, the decrease was 69.9% for EM and 75.9% for CM. In contrast, the eff ectiveness of treatment in patients with and without positive FH was practically the same. After 12 months of treatment, the effect was more pronounced in patients with MOH (76.2% decrease) than without MOH. Efficacy was similar in men and women. Fifty-two patients received two prophylactics before starting biological therapy, 45 patients had three prophylactic drugs and 29 patients used four prophylactic drugs. The effectiveness of biological therapy was similar in all three groups (after 12 months, the decrease in MMD was 70.3 vs. 73.2 vs. 70.7%). The efficacy of erenumab and fremanezumab (administered in month or three-month intervals) was not significantly different. Therapy was discontinued due to insufficient effect only in 6 patients. AE occurred in only 10 (7.7%) patients, of whom 9 (8.6%) were treated with erenumab and 1 (4.8%) was treated with fremanezumab. Therapy was discontinued due to AE (constipation) only in 1 patient on erenumab. Conclusion: CGRP (calcitonin generelated peptide) antibodies in the treatment of migraine are significantly effective and well tolerated in our group of patients in accordance with previous randomized and observational trials.
Keywords:
Migraine – prophylactic treatment – CGRP antibodies
Autoři:
J. Šípková 1; T. Nežádal 1,2; D. Čtrnáctá 1; M. Bajaček 1; J. Dvořák 1
Působiště autorů:
Centrum pro diagnostiku a léčbu bolestí hlavy, Neurologické oddělení, ÚVN Praha
1; Neurochirurgická a neuroonkologická klinika 1. LF UK a ÚVN Praha
2
Vyšlo v časopise:
Cesk Slov Neurol N 2022; 85(3): 248-256
Kategorie:
Krátké sdělení
doi:
https://doi.org/10.48095/cccsnn2022248
Souhrn
Cíl: V uvedené studii retrospektivně hodnotíme pacienty našeho centra na biologické léčbě migrény protilátkami CGRP nasazené po schválení plné úhrady od března do konce roku 2020. Do sledování byli zařazeni pouze pacienti s aplikací erenumabu a fremanezumabu, neboť galkanezumab byl schválen až v říjnu 2020. Soubor a metodika: Soubor tvoří 130 pacientů, z toho 118 žen (90,8 %) a 12 mužů (9,2 %) v průměrném věku 46,2 (21–76) let. Primárním cílem bylo vyhodnotit efekt terapie po 3, 6, 9 a 12 měsících, dále počet non-respondérů (redukce migrenózních dnů v měsíci [monthly migraine day; MMD] méně než 50 %), redukci dní s nadužíváním akutní medikace (medication overuse; MOH) a vztah k trvání onemocnění, počtu předchozích profylaxí, migréně v rodinné anamnéze (RA) a komorbiditám. Sledován byl výskyt nežádoucích účinků (NÚ). Výsledky: Průměrný počet MMD před nasazením léčby byl 12,2. Po 3 měsících došlo ke snížení MMD o 60,5 % (na 4,7), v dalších měsících účinnost ještě dále stoupala na více než 70 %, větší účinnosti bylo dosaženo u chronické migrény (CM) oproti epizodické (EM). Po 12 měsících činil pokles u EM 69,9 %, a u CM 75,9 %. Naopak účinnost léčby u pacientů s pozitivní RA a bez ní byla prakticky totožná. Po 12 měsících léčby byl efekt výraznější u pacientů s konkomitantní MOH (pokles o 76,2 %) než bez MOH. Účinnost u mužů a u žen byla obdobná. 52 pacientů před nasazením biologické léčby užívalo dvě profylaktika, 45 pacientů tři a 29 pacientů čtyři a více profylaktik. Účinnost biologické léčby byla ve všech třech skupinách podobná (po 12 měsících pokles MMD o 70,3 vs. 73,2 vs. 70,7 %). Účinnost erenumabu a fremanezumabu (podávání v jedno - či tříměsíčních intervalech) se významně nelišila. Kvůli nedostatečnému efektu byla léčba vysazena jen u šesti pacientů. NÚ se vyskytly pouze u 10 (7,7 %) pacientů, z toho u devíti (8,6 %) pacientů léčených erenumabem a u jednoho (4,8 %) pacienta léčeného fremanezumabem. Pro NÚ byla terapie vysazena pouze u jednoho pacienta na erenumabu (obstipace). Závěr: Protilátky CGRP (calcitonin gene-related peptide) v léčbě migrény jsou v našem souboru pacientů významně účinné a dobře tolerované, stejně jako v předchozích randomizovaných a observačních studiích.
Klíčová slova:
migréna – protilátky CGRP – profylaktická léčba
Úvod
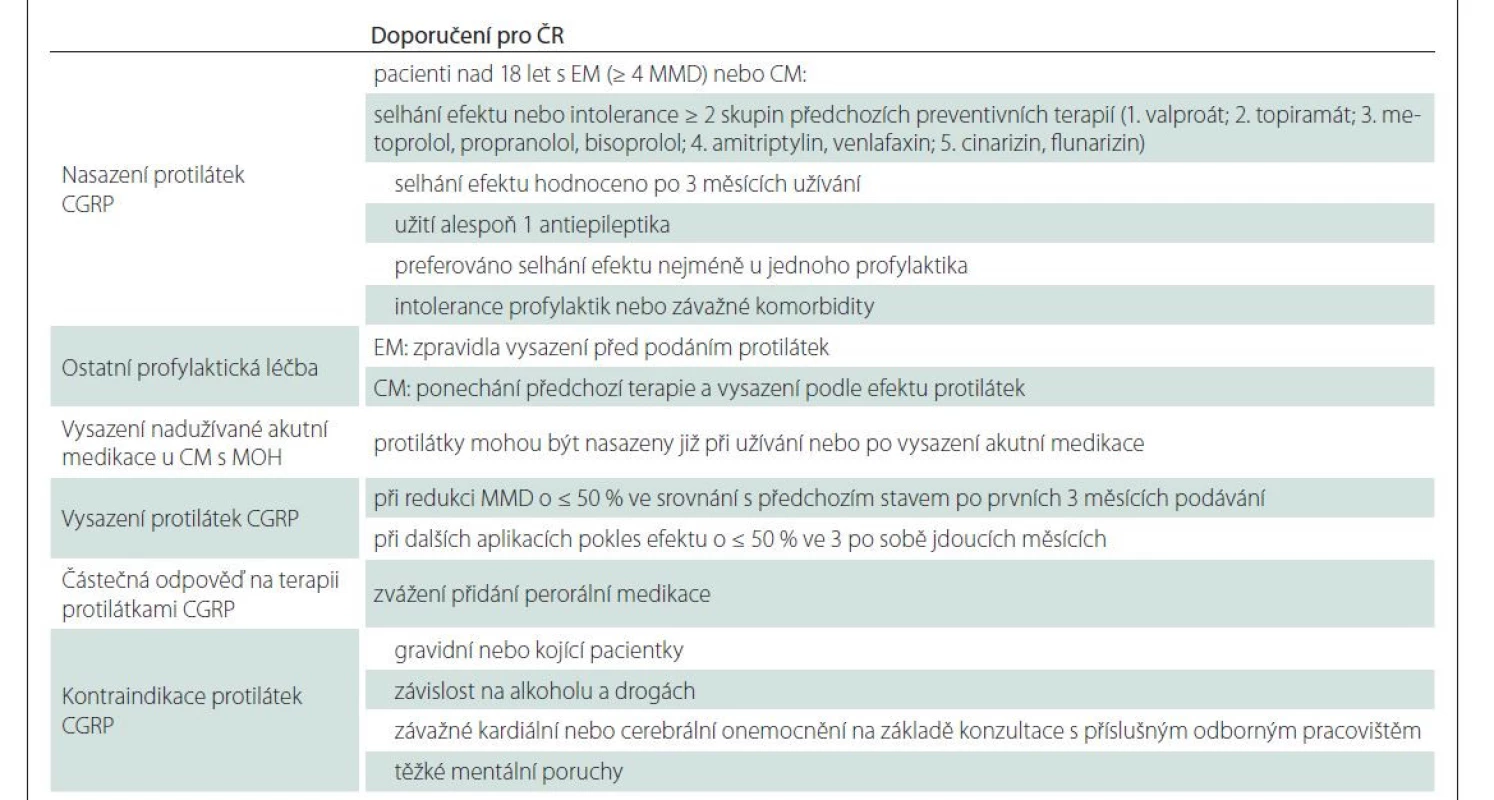
Migréna je velmi častým neurologickým onemocněním, dokonce třetí nejčastější chorobou vůbec a podle Global Burden of Disease 2020 zároveň druhou nejvíce handicapující diagnózou celosvětově, u mladých žen se řadí dokonce na první místo v příčině disability [1,2]. Prevalence migrény činí 17,1 % u žen a 5,6 % u mužů, nejčastěji se vyskytuje v produktivním věku 30–39 let [3]. Stávající zavedená perorální profylaktická léčba má ale svá úskalí: selhání účinnosti nebo tolerability i nízkou compliance pacientů. V případě selhání nejméně dvou profylaxí (z toho jedna antiepileptika), při nejméně 4 dnech s bolestí hlavy za měsíc (monthly migraine day; MMD), jsou indikovány protilátky CGRP (calcitonin gene-related peptid) (tab. 1) [4–6].
CGRP a jeho klíčová úloha při léčbě migrény
Již od 90. let minulého století se do centra zájmu vědců zkoumajících patofyziologii a léčbu migrény dostává neuropeptid CGRP, u kterého byl prokázán přímý vztah k aktuálně probíhajícímu migrenóznímu záchvatu. CGRP má zásadní úlohu v periferní části celého děje. Podílí se na cévní vazodilataci, aktivaci mastocytů, vzniku perivaskulárního zánětu i na periferní senzitizaci. Nachází se v mnoha lokalitách centrálního i periferního nervového systému, např. v periferních trigeminových zakončeních, v určitých částech mozkového kmene vč. ganglion trigeminale Gasseri, v senzorických centrech, jádrech hlavových nervů a v neuronálních drahách směřujících do hypotalamu a talamu. CGRP neprochází hematoencefalickou bariérou. Při záchvatu migrény dochází ke zvyšování sérových hladin CGRP v intrakraniálním řečišti [7]. Protrahovaná aktivace trigeminálních drah pomocí CGRP pak může způsobovat centrální senzitizaci cestou neuronů druhého řádu, a tedy potenciálně vést i k transformaci epizodické migrény (EM) v chronickou (CM) [8]. Receptory CGRP jsou přítomné také na hladké svalovině intrakraniálních cév. Jejich aktivací dochází k vazodilataci. Aktivace receptorů CGRP na mastocytech způsobuje degranulaci cytokinů a dalších zánětlivých mediátorů během neurogenního zánětu. Postsynaptické receptory CGRP jsou lokalizovány na neuronech v trigeminových jádrech ve kmeni a ve ventroposteromediálním jádru talamu, kde se podílí na přenosu nocicepce [9]. Trigeminální ganglion a dura mater se nachází před hematoencefalickou bariérou (HEB), čehož využívají nově vyvinuté specifické monoklonální protilátky namířené proti receptoru CGRP nebo proti CGRP samotnému. Jedná se o velké molekuly s vysokou molekulovou hmotností, takže téměř neprocházejí HEB. Mají výraznou cílovou specifi tu, čímž se minimalizují nežádoucí účinky (NÚ) v jiných místech působení, a zároveň se tím zlepšuje i jejich tolerabilita. Mají dlouhý poločas účinku 20–45 dní, proto se s výhodou užívají jako profylaktická léčba, kterou lze podávat jednou měsíčně anebo i v delších intervalech. Nemají lékové interakce, nejsou totiž metabolizovány v játrech, ale jsou pozvolna štěpeny na jednotlivé aminokyseliny pomocí retikuloendoteliálního systému (RES) [10]. Humánní erenumab je antagonistou receptoru CGRP. Humanizované monoklonální protilátky fremanezumab, galkanezumab a eptinezumab se váží přímo na CGRP [11]. Všechny se užívají subkutánně v pravidelných intervalech à 4 týdny, u fremanezumabu lze využít i kvartální schéma podávání. Eptinezumab lze užít nejen s.c., ale i v intravenózní infuzi každé 3 měsíce. Monoklonální protilátky můžeme využít k léčbě chronické migrény CM i EM, popřípadě migrény kombinované s nadužíváním akutní medikace (medication overuse; MOH). Erenumab prokázal svoji účinnost i u perimenstruační migrény. Fremanezumab je v současné době testován i u epizodické a chronické cluster headache a u pacientů s post-traumatickou bolestí hlavy. U galkanezumabu byl prokázán účinek i u epizodické cluster head ache [12]. Vedlejší účinky monoklonálních protilátek jsou mírné, většinou se jedná o lokální reakci v místě vpichu (indurace, erytém, bolestivost, pruritus), zácpu, únavu, bolesti zad, artralgie, svalové křeče, nauzeu, zvracení, katar horních cest dýchacích a uroinfekci. Vzhledem k humanizaci monoklonálních protilátek je jejich imunogenní potenciál nízký [4,11]. Rizika dlouhodobé blokády CGRP doposud nejsou plně známa a jsou předmětem dalšího zkoumání, stejně tak i možný vznik neutralizačních protilátek. První studie však naznačují, že imunogenní potenciál erenumabu je nízký i po prvních pěti letech užívání. Neutralizační protilátky se nejvíce tvoří v prvním roce léčby a jejich výskyt je většinou přechodný [13].
Na území ČR jsou doposud registrovány tři účinné látky – erenumab, fremanezumab a galkanezumab. V roce 2020 u nich byla postupně schválena i úhrada zdravotními pojišťovnami pro diagnózy: EM bez aury, EM s aurou a CM [14]. Aplikace je vázána na podávání ve specializovaných centrech pro diagnostiku a léčbu bolestí hlavy [4].
Metodika
V našem souboru retrospektivně hodnotíme pacienty našeho centra na biologické léčbě migrény protilátkami CGRP nasazené po schválení plné úhrady od března 2020 do konce roku 2020. Do sledování byli zařazeni pacienti splňující současná indikační kritéria [4] (tab. 1). Hodnocena byla pouze aplikace erenumabu a fremanezumabu, neboť galkanezumab byl schválen až 1. 10. 2020, a tito pacienti by tak nesplnili požadovanou délku sledování. Dávkování je standardní: 140 mg erenumabu po 28 dnech (dávka 70 mg není v ČR hrazena), 225 mg fremanezumabu po 1 měsíci nebo 675 mg po 3 měsících.
Soubor tvoří 130 pacientů, z toho 118 (90,8 %) žen a 12 (9,2 %) mužů v průměrném věku 46,2 (21–76) let.
Primárním cílem bylo hodnocení efektu terapie po 3, 6, 9 a 12 měsících, dále byly sledovány počet non-respondérů (nedosáhli redukce MMD ≥ 50 %), redukce dní s MOH a vztah k trvání onemocnění, počtu předchozích profylaxí, migréně v rodinné anamnéze (RA) a komorbiditám. Sledován byl výskyt NÚ.
Výsledky
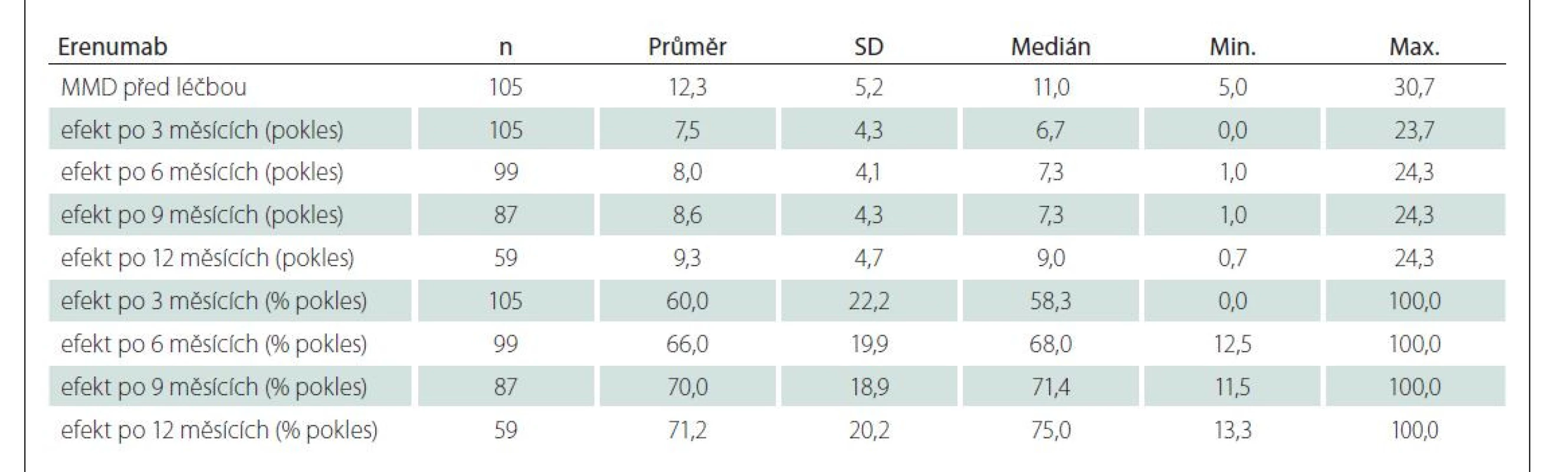
Průměrný počet MMD před nasazením léčby byl 12,2. Po 3 měsících došlo ke snížení o 60,5 % (o 7,5 MMD), v dalších měsících účinnost ještě dále stoupala na více než 70 % (tab. 2, obr. 1). Účinnost terapie CGRP byla vyšší u CM než u EM. Po 3 měsících léčby počet MMD u pacientů s EM klesl o 58,4 %, u CM dokonce o 66,3 %, v dalších měsících účinnost ještě nadále mírně rostla. Po 12 měsících byl pokles u EM o 69,9 %, u CM o 75,9 % (tab. 3 a 4).
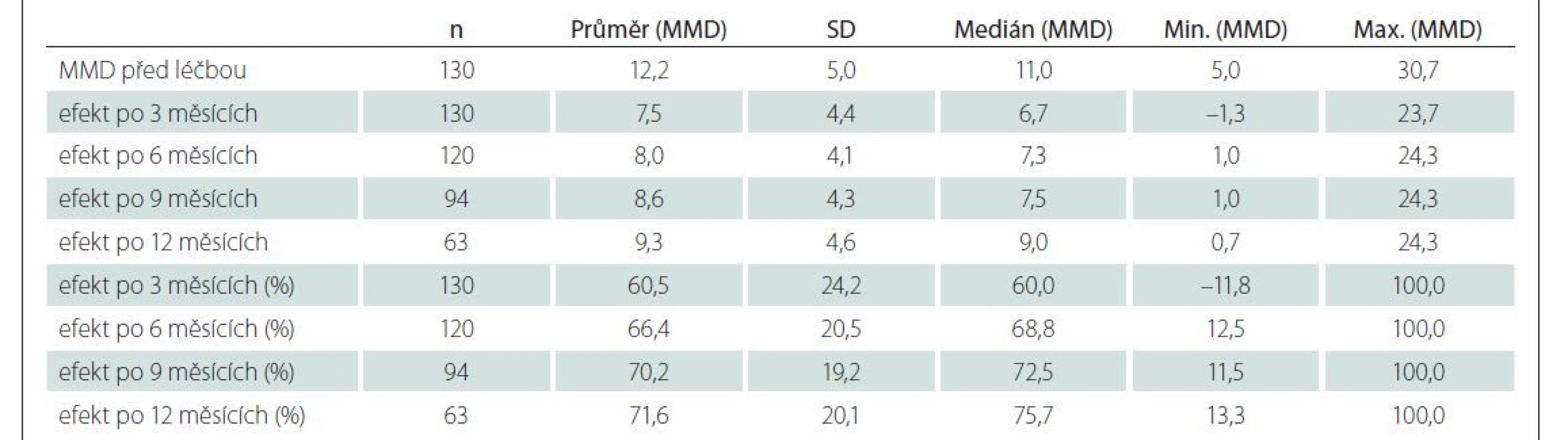
MMD – počet dní s migrénou za měsíc
Fig. 1. CGRP effect after 3, 6, 9 and 12 months.
MMD – month migraine days



Současný výskyt bolestí hlavy z MOH byl referován u 23 (24,2 %) osob s EM a u 27 (77,1 %) léčených s CM. V prvních 9 měsících léčby nebyl pozorován významný rozdíl efektu terapie u pacientů s konkomitantní MOH oproti pacientům bez ní. Po 12 měsících léčby byl však efekt výraznější u pacientů s MOH (pokles o 76,2 %, 28 pacientů v souboru vs. bez MOH o 68,0 %, 35 pacientů v souboru) (tab. 5 a 6, obr 2).
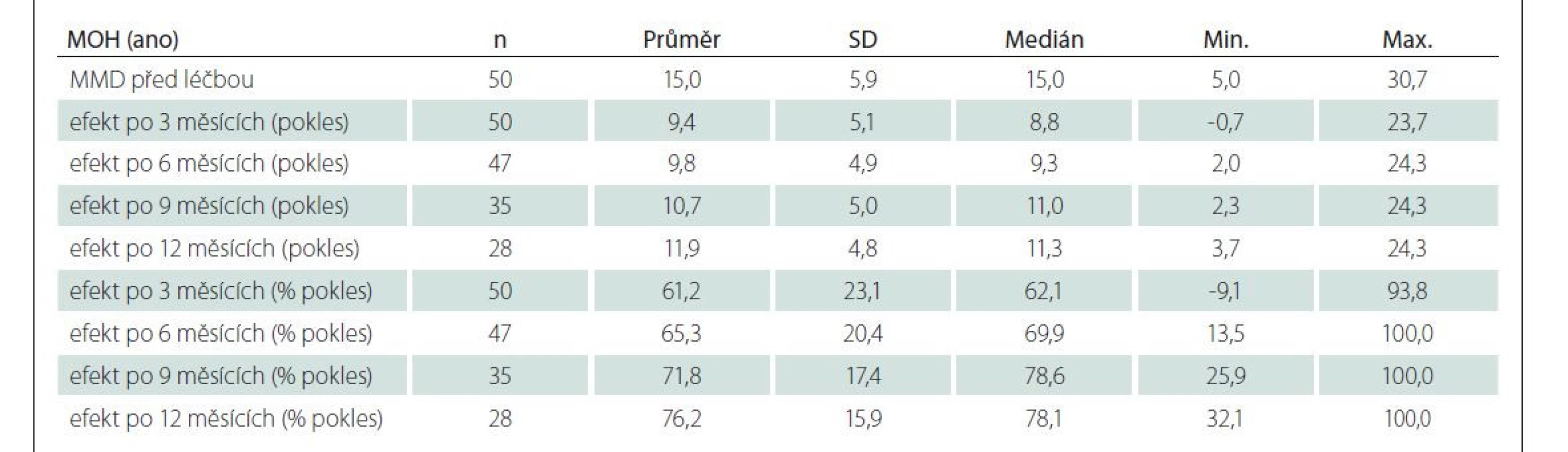
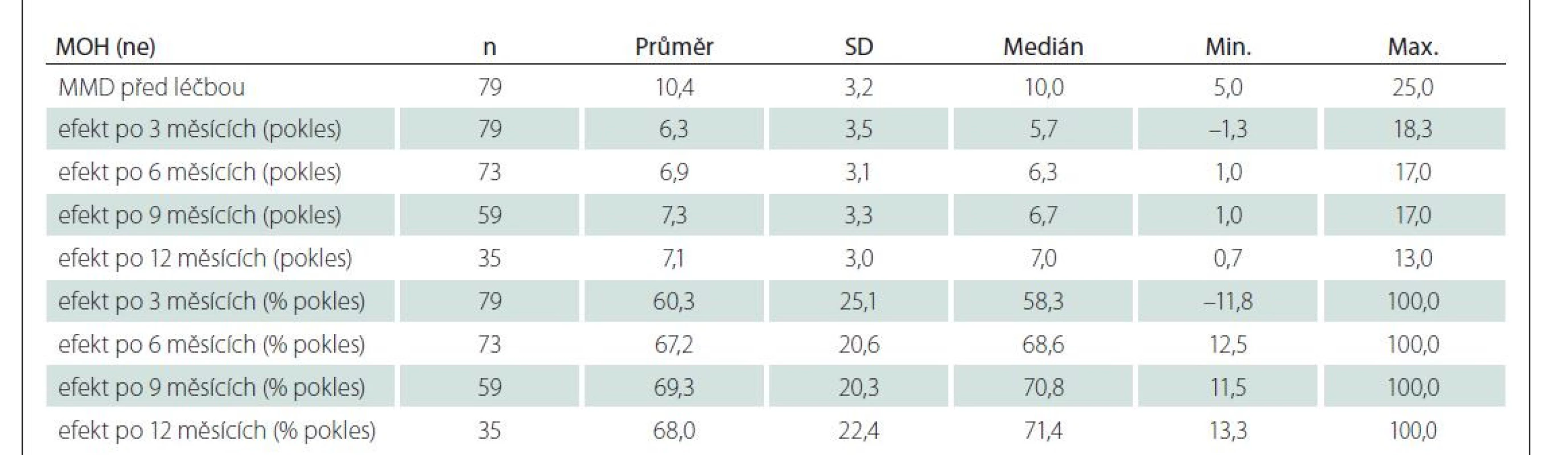
MMD – počet dní s migrénou za měsíc; MOH – bolest hlavy z nadužívání léčiv
Fig. 2. Effect of CGRP therapy in patients with concomitant MOH.
MMD – month migraine days; MOH – medication overuse

Dále byly sledovány počet selhání (či netolerování) profylaktické medikace před nasazením terapie CGRP a její účinnost vzhledem k počtu užívaných medikamentů. Celkem 52 pacientů před nasazením biologické léčby užívalo dvě profylaktika, 45 pacientů tři a 29 pacientů čtyři a více profylaktik, účinnost biologické léčby byla ve všech třech skupinách obdobná (po 3 měsících léčby pokles MMD o 64 vs. 55,7 vs. 60,9 %, po 12 měsících pokles MMD o 70,3 vs. 73,2 vs. 70,7 %).
Účinnost erenumabu a fremanezumabu se významně nelišila (tab. 7 a 8), skupiny však nebyly početně vyrovnané (erenumab užívalo 105 a fremanezumab 21 pacientů), tudíž výsledky je třeba interpretovat obezřetně. Nebyl zaznamenán významný rozdíl mezi měsíčním a kvartálním užitím fremanezumabu, ale znovu je třeba brát v úvahu relativně malý počet pacientů (9 pacientů po dobu 6 měsíců ve skupině s měsíčním podáváním, 12 pacientů po dobu 3 měsíců a 9 pacientů po dobu 6 měsíců ve skupině s kvartální frekvencí užívání). Účinnost u mužů a u žen se významně nelišila, avšak vzhledem k nízkému počtu mužů v souboru (12 vs. 118) je opět nutné tyto výsledky interpretovat obezřetně.

Průměrná doba trvání migrény v době zahájení léčby byla 27,3 (3–66) let. Korelace mezi délkou trvání migrény a mírou účinnosti terapie CGRP nebyla zjištěna.
Pozitivní RA byla zaznamenána ve stejné míře u pacientů s EM (56 [58,9 %]) i CM (22 [62,9 %]). Pokles počtu MMD za 3 měsíce dosahoval 61 % u pozitivní RA a 59,8 % u negativní RA. Počet MMD za 12 měsíců poklesl o 72,5 % u pozitivní RA, o 70,2 % u negativní RA.
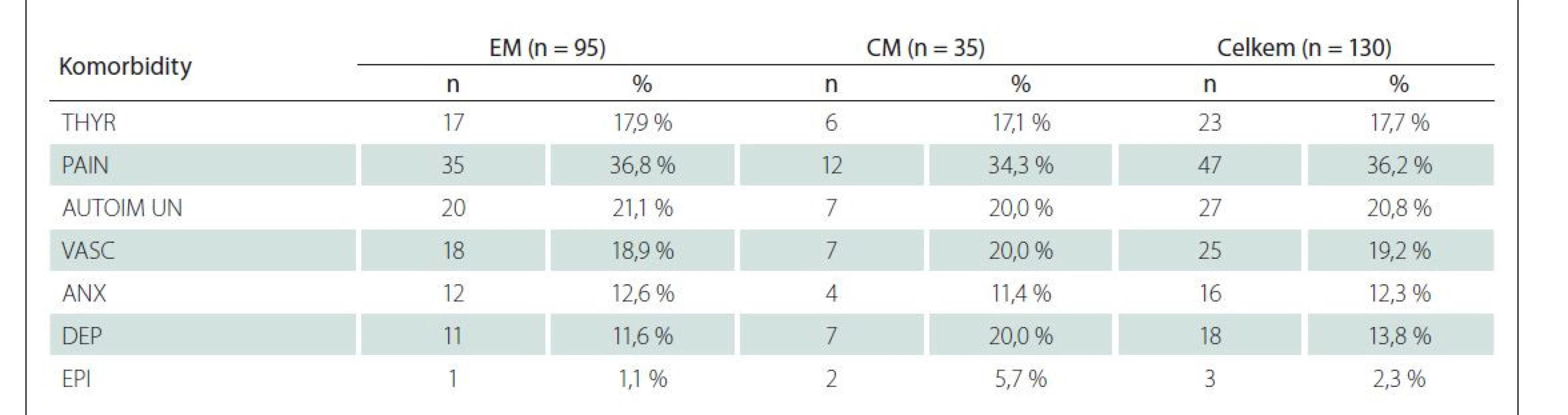
Komorbidity jsou uvedeny v tab. 9. Mezi sledované komorbidity jsme zařadili porušenou funkci štítné žlázy (hypofunkce, stav po tyroidektomii, hypertyreoidismus), která byla přítomna u 23 (17,7 %) sledovaných. Bolestivé stavy (nejčastěji vertebrogenní potíže, kombinace s jiným typem bolesti hlavy, artralgie) se vyskytovaly u 47 (36,2 %) pacientů. Autoimunitní onemocnění (autoimunitní tyreoiditis, revmatoidní artritida, atopický ekzém, Crohnova choroba, revmatická horečka v dětství, Sjögrenův syndrom) referována v 27 (20,8 %) případech. Vaskulární onemocnění (arteriální hypertenze, žilní městky, Raynaudův syndrom, mozkové aneuryzma) se vyskytovaly u 25 (19,2 %) pacientů, epilepsie u třech (2,3 %) pacientů. Úzkostný syndrom byl zaznamenán u 16 (12,3 %) sledovaných a depresivní syndrom u 18 (13,8 %) sledovaných. Incidence těchto komorbidit byla velmi podobná u EM i CM. Pouze depresivní symptomatika byla dokumentována ve větší míře u pacientů s CM oproti EM (20,0 vs. 11,6 %).
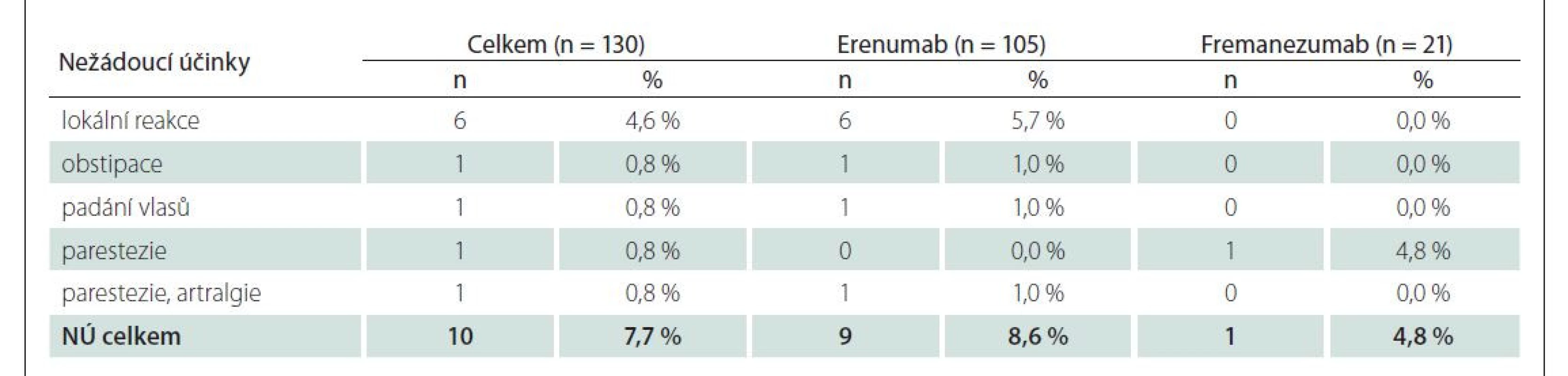
Výskyt NÚ byl poměrně nízký. Z celkového souboru se vyskytly u deseti (7,7 %) pacientů, z toho u devíti (8,6 %) osob léčených erenumabem a u jednoho (4,8 %) pacienta na terapii fremanezumabem. Ve většině případů se jednalo o mírné nežádoucí účinky a léčba nemusela být přerušena. Šest pacientů (všichni užívající erenumab) mělo lokální reakci v místě vpichu, jeden pacient (léčený fremanezumabem) zaznamenal parestezie, jeden pacient (na erenumabu) kromě parestezií ještě artralgie. Pouze v jednom případě se jednalo o středně závažný NÚ (úporná obstipace), kvůli kterému musela být léčba erenumabem ukončena. Ze skupiny léčených fremanezumabem nikdo nemusel léčbu ukončit z důvodu nežádoucích účinků (tab. 10). Celkově léčbu předčasně ukončilo deset (7,7 %) pacientů (z toho osm [7,6 %] osob užívajících erenumab a dvě [9,5 %] osoby užívající fremanezumab). Léčba byla ukončena nejčastěji z důvodu nedostatečného efektu, tj. poklesu počtu MMD o méně než 50 % ve 3 po sobě následujících měsících. Nedostatečný efekt byl zaznamenán u šesti (4,6 %) pacientů, pět (4,8 %) pacientů užívalo erenumab (čtyři ukončili léčbu po 6 měsících, jeden po 12 měsících), jeden (4,8 %) pacient užíval fremanezumab (léčbu ukončil po 3 měsících, byla podána jedna kvartální dávka). Kvůli těhotenství byla přerušena léčba u dvou pacientek [15]. Jedna pacientka přestala docházet na kontroly, tudíž léčba dále nepokračuje (alespoň ne na našem pracovišti) (tab. 11).

Diskuze
Cílem této práce bylo zhodnotit údaje o všech pacientech našeho centra užívajících erenumab anebo fremanezumab alespoň 3 měsíce. Dosavadní výsledky hodnotíme jako velmi dobré. Potvrdili jsme dobrou účinnost terapie CGRP jak u EM, tak CM a u současně se vyskytující MOH, obdobně jako v předchozích randomizovaných studiích [16–20]. Redukce MMD je nezávislá na počtu předchozích užívaných profylaktických terapií [21,22]. Tento efekt je stabilní a dlouhodobý [13].
Jedná se o náš první soubor pacientů převážně retrospektivně sledovaný po dobu až jednoho roku. Vzhledem k tomu, že část pacientů byla před registrací na našem pracovišti léčena několika vzorky protilátek, nebylo u všech pacientů možné realizovat testování dotazníky (např. Headache Impact Test [HIT-6], The Migraine Disability Assessment Test [MIDAS] apod.) od úplného zahájení terapie, a tak nebyly ve studii hodnoceny.
Další limitací této práce je určitá nekonzistentnost pacientů v souboru, významná část pacientů (36,9 %) před začleněním do našeho sledování již užívala biologickou léčbu ať už krátkodobě u ambulantních neurologů (vzorky), či v rámci třetí fáze klinických studií. U části respondentů tudíž byla dokumentována dobrá účinnost ještě před zařazením do studie.
Profylaktická léčba byla u naprosté většiny pacientů vysazena před nasazením protilátek CGRP, ponechána byla pouze v jednotlivých případech. Převážně se jednalo o antidepresiva u psychiatrických komorbidit, která pacienti užívali dlouhodobě a zpravidla neměla vliv na počet MMD. Vzhledem k malému procentu a rozmanitosti důvodů jsme toto statisticky nehodnotili. U několika pacientů s CM byla profylaxe, dříve částečně účinná, vysazena během sledování bez zhoršení stavu.
Vzhledem k povaze našeho souboru se kromě randomizovaných studií nabízí srovnání se současnými z běžné klinické praxe. Při srovnání s italskou observační studií s erenumabem z roku 2020 z oblasti Abruzzo [23] je účinek CGRP prakticky totožný (snížení počtu MMD po šesti měsících užívání o 66,4 vs. 69,7 %). Srovnání s touto studií má však zásadní omezení, a to jiný poměr pacientů s EM a CM. V české studii bylo poměrné zastoupení následující: EM 74,1 %, CM 26,9 %, MOH 38,5 %. Naproti tomu v italské EM 5,6 %, CM 94,4 %, MOH 71,9 %. V našem souboru převažují pacienti s EM, neboť byli „forsírovaně“ zařazeni výše uvedení pacienti již zlepšení na prvním či několika vzorcích protilátek CGRP u necentrových neurologů, kde tato diagnóza převažovala. V Itálii převažují pacienti z center pro léčbu bolestí hlavy, kdy byla léčba přednostně nasazována pacientům s nejfrekventnějšími migrénami s odpovídajícím procentem MOH. Pro nedostatečný efekt byla v naší studii vysazena léčba celkem u šesti (4,6 %) pacientů ze 130 a jeden (0,8 %) pacient musel terapii ukončit z důvodu NÚ (obstipace). V italské studii byly CGRP protilátky vysazeny kvůli nedostatečnému účinku u 11 (12,4 %) pacientů z 89, u 1 (1,1 %) kvůli NÚ (alergická reakce). Při srovnání NÚ bylo v naší studii dokumentováno pouze 7,7 % pacientů s NÚ, nejčastěji se jednalo o lokální reakci (šest pacientů z deseti), zatímco v italské zaznamenali 22,5 % případů NÚ. U 12 (13,5 %) pacientů byla pozorována obstipace a pouze u dvou (2,2 %) lokální reakce. Dále byly zaznamenány NÚ, které v české studii nebyly pozorovány – pruritus, kožní rash, flu-like syndrom, abdominální křeče, meteorismus, nauzea, vertigo, přechodné vaginální krvácení. Ani v jedné studii nebyly zaznamenány kardiovaskulární NÚ.
Velkou výhodou biologické léčby je její efekt i na chronickou a rezistentní migrénu a konkomitantní MOH. Španělská studie z kliniky Vall d’Hebron z roku 2021 [24], sledující účinek erenumabu a galkanezumabu právě u takto postižených pacientů, zaznamenala redukci počtu MMD o ≥ 50 % u 50,4 % pacientů (70 ze 139) po 6 měsících léčby. Ve skupině se současnou MOH a non-MOH byl účinek velmi podobný (63,4 vs. 57,5 %). V naší studii byl takový účinek zaznamenán dokonce u 84,4 % pacientů (27 z 32) trpících CM, ve skupině se současnou MOH u 77,8 % (21 z 27) a u non-MOH u všech pěti pacientů. Pokud bychom hodnotili celý náš soubor, to znamená i pacienty s EM, tak by byl pokles počtu MMD ≥ 50 % referován u 80,8 % (97 ze 120) po 6 měsících léčby. Někteří pacienti s MOH v našem souboru dříve prodělali detoxikační léčbu při hospitalizaci, efekt byl zpravidla pouze přechodný nebo nedostatečný. V období 1 roku před nasazením CGRP protilátek však tato léčba nebyla provedena u žádného z pacientů.
Průběžné výsledky z německo-rakouské observační studie [25] u pacientů na fremanezumabu (FINESSE) přinášejí ve výsledcích obdobnou redukci bolestí hlavy z 12,7 na 6,2 MMD (48,7 %), ale s nižším celkovým počtem respondérů, s vyšším podílem u pacientů s EM (53,2 %) než u pacientů s CM (43,0 %). Tento rozdíl však lze přičíst rovněž i určité „preselekci“ pacientů v našem souboru, kde byla již část nemocných na terapii vzorky nebo ve studiích. Indikační kritéria jsou přísnější v Německu, nicméně ve studiích i v našem souboru nebyl zjištěn vliv počtu předchozích profylaxí na efektivitu biologické léčby. ČR je pak zařazena do obdobné evropské studie s fremanezumabem – PEARL (The Pan-European Real Life) [26].
Do budoucna plánujeme soubor sledovat i nadále, další pacienty již prospektivně, a samozřejmě začlenit i pacienty léčené galkanezumabem. V září 2021 byl na našem pracovišti spuštěn ReMig – Český registr pacientů s migrénou na biologické léčbě, kam jsou postupně zařazováni všichni pacienti z ČR, kteří zahájili terapii CGRP od začátku roku 2021.
Závěr
Výsledky našeho pozorování jsou obdobné jako v jiných studiích, potvrzují vysokou účinnost a dobrou snášenlivost protilátek CGRP u EM, CM i současné MOH. Nástup účinku je rychlý, s délkou terapie se efekt dále zlepšuje a z dlouhodobého hlediska je stabilní.
Etické aspekty
Práce byla provedena ve shodě s Helsinskou deklarací z roku 1975 a jejími revizemi v letech 2004 a 2008. Tento článek nepodléhá schválení etickou komisí, jedná se o retrospektivní sledování souboru pacientů léčených v centru pro diagnostiku a léčbu bolestí hlavy v Ústřední vojenské nemocnici.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Přijato k recenzi: 29. 1. 2022
Přijato do tisku: 25. 5. 2022
MUDr. Jitka Šípková
Centrum pro diagnostiku a léčbu
bolestí hlavy
Neurologické oddělení
ÚVN Praha
U Vojenské nemocnice 1200/1
169 02 Praha 6
e-mail: jitka.sipkova@uvn.cz
Zdroje
1. Global burden of 369 diseases and injuries in 204 countries and territories, 1990–2019: a systematic analysis for the global burden of disease study 2019. Lancet 2020; 396(10258): 1204–1222. doi: 10.1016/ S0140 - 6736(20)30925-9.
2. Global, regional, and national burden of migraine and tension-type headache, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol 2018; 17(11): 954–976. doi: 10.1016/ S1474 - 4422(18)30322-3.
3. Diamond S, Bigal ME, Silberstein SD et al. A patterns of diagnosis and acute and preventive treatment for migraine in the United States: results from the American Migraine Prevalence and Prevention Study. Headache 2007; 47(3): 355−363. doi: 10.1111/ j.1526-4610.2006.00 631.x.
4. Nežádal T, Marková J, Bártková A et al. CGRP monoklonální protilátky v léčbě migrény – indikační kritéria a terapeutická doporučení pro Českou republiku. Cesk Slov Neurol N 2020; 83/ 116(4): 445–451. doi: 10.14735/ amcsnn2020445.
5. American Headache Society. The American Headache Society position statement on integrating new migraine treatments into clinical practise. Headache 2019; 59(1): 1–18. doi: 10.1111/ head.13456.
6. Sacco S, Bendtsen L, Ashina M et al. European headache federation guideline on the use of monoclonal antibodies acting on the calcitonin gene related peptide or its receptor for migraine prevention. J Headache Pain 2019; 20(1): 6. doi: 10.1186/ s10194-018-0955-y.
7. Goadsby PJ, Edvinsson L, Ekman R. Vasoactive peptide release in the extracerebral circulation of humans during migraine headache. Ann Neurol 1990; 28(2): 183–187. doi: 10.1002/ ana.410280213.
8. Iyengar S, Ossipov MH, Johnson KW. The role of calcitonin gene-related peptide in peripheral and central pain mechanisms including migraine. Pain 2017; 158(4): 543–559. doi: 10.1097/ j.pain.0000000000000831.
9. Tepper J. Anti-calcitonin gene-related peptide (CGRP) therapies: update on a previous review after the American Headache Society 60th Scientifi c meeting, June 2018. Headache 2018; 58(Suppl 3): 276–290. doi: 10.1111/ head.13417.
10. Hargreaves R, Olesen J. Calcitonin gene-related peptide modulators – the history and renaissance of a new migraine drug class. Headache 2019; 59(6): 951–970. doi: 10.1111/ head.13510.
11. Nežádal T. CGRP monoklonální protilátky v profylaktické léčbě migrény. Neurol Praxi 2019; 20(5): 356–360. doi: 10.36290/ neu.2019.141.
12. Goadsby PJ, Dodick DW, Leone M et al. Trial of galcanezumab in prevention of episodic cluster headache. N Engl J Med 2019; 381(2): 132–141. doi: 10.1056/ NEJMoa1813440.
13. Ashina M, Goadsby PJ, Reuter U et al. Long-term efficacy and safety of erenumab in migraine prevention: results from a 5-year, open-label treatment phase of a randomized clinical trial. Eur J Neurol 2021; 28(5): 1716–1725. doi: 10.1111/ ene.14715.
14. Nežádal T, Marková J, Bártková A et al. Mezinárodní klasifikace bolestí hlavy (ICHD-3) – oficiální český překlad. Cesk Slov Neurol N 2020; 83(2): 145–152. doi: 10.14735/ amcsnn2020145.
15. Rajdová A, Vlčková E, Niedermayerová I et al. Bolesti hlavy v graviditě. Cesk Slov Neurol N 2020; 83/ 116(3): 269–276. doi: 10.14735/ amcsnn2020269.
16. Goadsby PJ, Reuter U, Hallström Y et al. A controlled trial of erenumab for episodic migraine. N Engl J Med 2017; 377(22): 2123−2132. doi: 10.1056/ NEJMoa1705848.
17. Tepper S, Ashina M, Reuter U et al. Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised, double-blind, placebo-controlled phase 2 trial. Lancet Neurol 2017; 16(6): 425–434. doi: 10.1016/ S1474-4422(17)30083-2.
18. Silberstein SD, Dodick DW, Bigal ME et al. Fremanezumab for the preventive treatment of chronic migraine. N Engl J Med 2017; 377(22): 2113–2122. doi: 10.1056/ NEJMoa1709038.
19. Dodick DW, Silberstein SD, Bigal ME et al. Effect of fremanezumab compared with placebo for prevention of episodic migraine: a randomized clinical trial. JAMA 2018; 319(19): 1999−2008. doi: 10.1001/ jama.2018. 4853.
20. Brandes JL, Kudrow D, Yeung PP et al. Effects of fremanezumab on the use of acute headache medication and associated symptoms of migraine in patients with episodic migraine. Cephalalgia 2020; 40(5): 470–477. doi: 10.1177/ 0333102419885905.
21. Reuter U, Goadsby PJ, Lanteri-Minet M et al. Efficacy and tolerability of erenumab in patients with episodic migraine in whom two-to-four previous preventive treatments were unsuccessful: a randomised, double-blind, placebo-controlled, phase 3b study. Lancet 2018; 392(10161): 2280–2287. doi: 10.1016/ S0140 - 6736(18)32534-0.
22. Ferrari MD, Diener HC, Ning X et al. Fremanezumab versus placebo for migraine prevention in patients with documented failure to up to four migraine preventive medication classes (FOCUS): a randomised, double-blind, placebo-controlled, phase 3b trial. Lancet 2019; 394(10203): 1030–1040. doi: 10.1016/ S0140 - 6736(19)31946-4.
23. Ornello R, Casalena A, Frattale I et al. Real-life data on the efficacy and safety of erenumab in the Abruzzo region, central Italy. J Headache Pain 2020; 21(1): 32. doi: 10.1186/ s10194-020-01102-9.
24. Caronna E, Gallardo VJ, Alpuente A et al. Anti-CGRP monoclonal antibodies in chronic migraine with medication overuse: real-life effectiveness and predictors of response at 6 months. J Headache Pain 2021; 22(1): 120. doi: 10.1186/ s10194-021-01328-1.
25. Straube A, Broessner G, Gaul C et al. FINESSE: fremanezumab for preventive treatment in migraine. Neurology 2022; 98 (18 Suppl): P16-2.001.
26. Ashina M, Amin FM, Kokturk P et al. PEARL study protocol: a real-world study of fremanezumab effectiveness in patients with chronic or episodic migraine. Pain Manag 2021; 11(6): 647–654. doi: 10.2217/ pmt-2021 - 0015.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2022 Číslo 3
-
Všechny články tohoto čísla
- Subkutánní forma natalizumabu v terapii vysoce aktivní relabující-remitující roztroušené sklerózy
- Intracerebrální krvácení při COVID-19
- Neurologické příznaky asociované s onemocněním COVID-19 podle celostátního online průzkumu
- Zlepšuje trojrozměrné předoperační plánování přesnost vložení pedikulárních šroubů?
- Patológia nervus medianus u akromegálie
- Ovlivnění spasticity pomocí elektrické stimulace podle Jantsche – pilotní studie
- Protilátky CGRP v profylaktické léčbě migrény
- Přehodnocení fenotypu SPG8 – první případ L619F WASHC5 hereditární spastické paraplegie v Evropě
- Tracheostomie v léčbě obstrukční spánkové apnoe není vždy definitivní řešení
- Stanovisko Sekce pro diagnostiku a léčbu bolestí hlavy
- MUDr. Richard Voldřich – vítěz Ceny Rudolfa Petra
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Neurologické příznaky asociované s onemocněním COVID-19 podle celostátního online průzkumu
- Ovlivnění spasticity pomocí elektrické stimulace podle Jantsche – pilotní studie
- Stanovisko Sekce pro diagnostiku a léčbu bolestí hlavy
- MUDr. Richard Voldřich – vítěz Ceny Rudolfa Petra
