Tonsilla cerebelli – anatomie, funkce a její význam pro neurochirurgii
Autoři:
D. Ospalík 1*; R. Bartoš 2,3*; H. Zítek 2; A. Malucelli 2; A. Hejčl 2; M. Sameš 2; V. Němcová 3
Působiště autorů:
Neurologické oddělení, Krajská zdravotní, a. s. – Masarykova nemocnice Ústí nad Labem, o. z.
1; Neurochirurgická klinika Univerzity J. E. Purkyně, Krajská zdravotní, a. s. – Masarykova nemocnice Ústí nad Labem, o. z.
2; Anatomický ústav, 1. LF UK, Praha
3
Vyšlo v časopise:
Cesk Slov Neurol N 2024; 87(1): 22-31
Kategorie:
Přehledný referát
doi:
https://doi.org/10.48095/cccsnn202422
Souhrn
* Dušan Ospalík a Robert Bartoš se na článku podíleli stejným dílem.
Cílem naší práce bylo čtenáři neurochirurgovi přiblížit detailní anatomii mozečkové tonzily se zaměřením i na její jednotlivé povrchy, jelikož ve většině publikací je tato prezentována pouze v rámci anatomie celé mozečkové hemisféry, případně anatomie cerebelomedulární fissury nebo průběhu arteria cerebelli posterior inferior. Laboratorní kadaverózní disekce tonzily jsme prováděli na čtyřech (v rovině vermis sagitálně rozdělených) mozečkových hemisférách a jednom kompletním mozečku i s jeho pedunkly a spodinou fossa rhomboidea. Tu jsme využili k demonstraci telovelárního přístupu. Domníváme se, že pro bezpečné zvládnutí telovelárního přístupu na operačním sále je laboratorní disekce velice vhodná a umožní neurochirurgovi poznat i méně známé struktury laterálního recessu, cerebelomedulární fissury i pochopit telovelární junkci. V přehledném referátu dokumentujeme také jednotlivé operace vztahující se k tonzile i telovelárnímu přístupu: operaci Chiariho malformace se syringomyelií, plexus papilomu IV. komory či kavernomu jejího laterálního recessu a cystického hemangioblastomu medulla oblongata. Na základě literárních údajů dokumentujeme historii vzniku operačního přístupu, který je příkladnou ukázkou spolupráce dvou světových neurochirurgů (Rhoton a Matsushima) a byla podložena dlouhodobou laboratorní prací. V referátu se věnujeme vrozeným variantám herniace tonzil mozečku (Chiariho malformace), ale i příčinám sekundárním a možnostem jejich zobrazení. Zmiňujeme klinický význam patologického sestupu tonzil a souvislost se syringomyelií.
Klíčová slova:
Cerebellum – foramen magnum – tonsilla cerebelli – mozkový kmen – telovelární přístup – Chiariho malformace – syringomyelie
Anatomický úvod
Tonzila představuje kaudomediální část mozečkové hemisféry, je tedy párovou strukturou. Řadíme ji k neocerebellu, byť její středová vermální „partnerka“ – uvula – je funkčně paleocerebellem, podobně jako pyramis vermis [1]. Tonzila je homologní savčímu ventrálnímu paraflocculu. Zatímco do flocculu jdou spoje z vestibulárních jader, do paraflocculu jdou spoje z jader pontinních.
Tonzila má přibližný tvar obráceného kužele s elipsoidní basí kraniálně, přičemž výška tonzily je větší než delší průměr base (obr. 1). Laterální strana (biventerická) má rovnocenné mělké horizontální fissury. Mediální strana má taktéž horizontální a šikmo nahoru orientované fissury, ale na našem kadaveru byly tři z nich hlubší, dělící mediální aspekt tonzily do několika drobných „lobulů“, jejichž objem je větší než objem folií na laterální straně, což je dobře patrné při pohledu na tonzilu zepředu. Na superoposteriorní (uvulární) straně je tonzilární pedunkl povrchněji, folia jej nepřekrývají a směřují radiálně do jeho středu, přičemž dole a nahoře mají vertikální směr. Anteriorní strana hledící do laterálního recessu IV. komory a přiléhající ke korpus restiforme má folia výraznější, v dolním pólu jsou taktéž vertikální a tonzilární pedunkl překrývají. Směrem dozadu je tonzilární pedunkl menší a zkosený, směřuje bílou hmotou do uvuly, vpředu je protáhlejší a směřuje bílou hmotu do lobulus biventer.
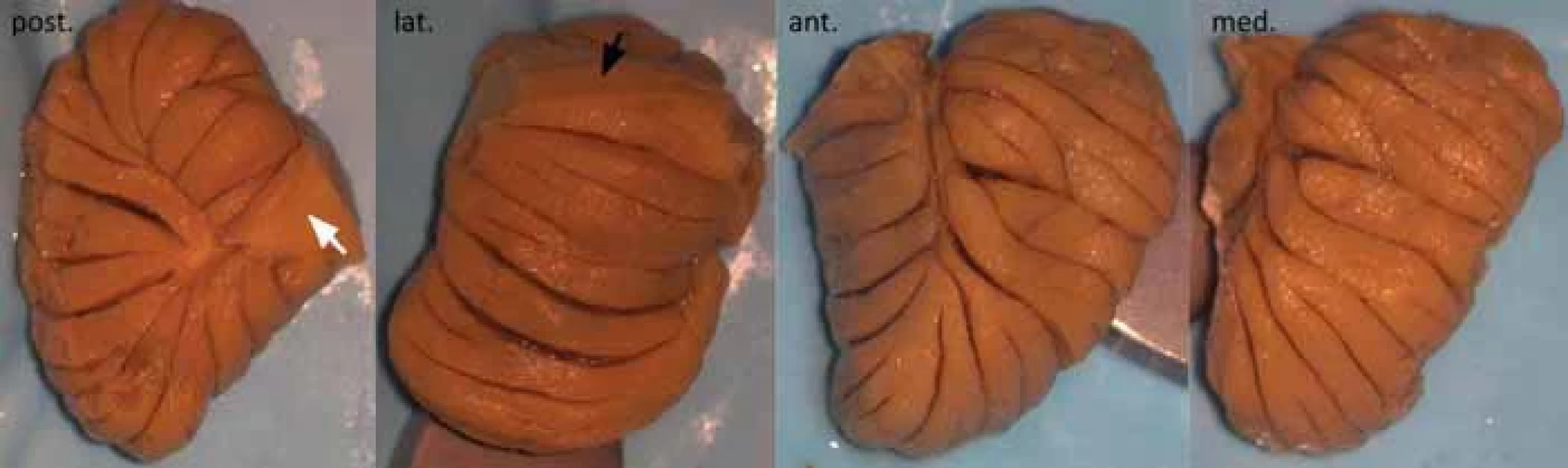
Fig. 1. Detailed view on separate tonsilla cerebelli surfaces.
ant. – anterior (medullovelar); lat. – lateral (biventeric), black arrow marks the biventeric part of the peduncle; med. – medial (tonsillovermal); post – posterior (uvular), white arrow marks the uvular part of the peduncle
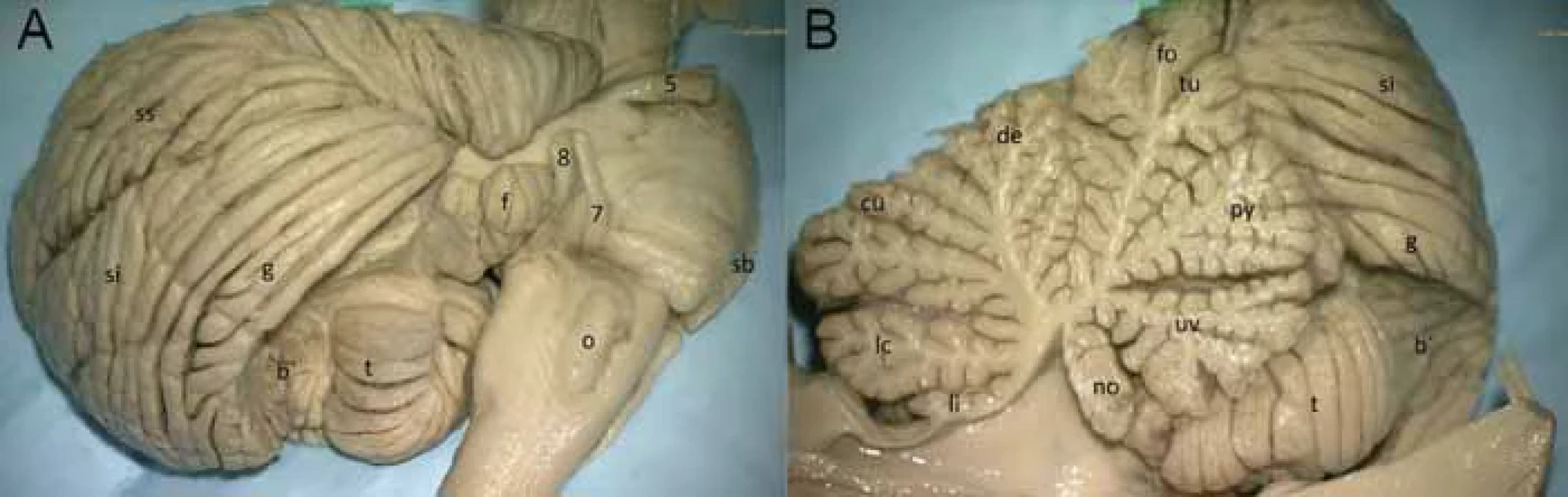
Fig. 2. View on the cerebellar tonsil from the lateral (A) and medial (B) side; from the lateral side it was covered by the biventer lobule, and the medial side is partially covered by the nodule, uvula and pyramis vermis.
5 – n. trigeminus; 7 – n. facialis; 8 – n. vestibulocochlearis; b´ – lobulus biventer (partially removed); cu – culmen; de – declive; f – fl occulus; fo – folium; g – lobulus gracilis; lc – lobulus centralis; li – lingula; no – nodulus; o – olive; py – pyramis vermis; sb – sulcus basilaris; si – lobulus semilunaris inferior; ss – lobulus semilunaris superior; t – tonsilla cerebelli; tu – tuber; uv – uvula
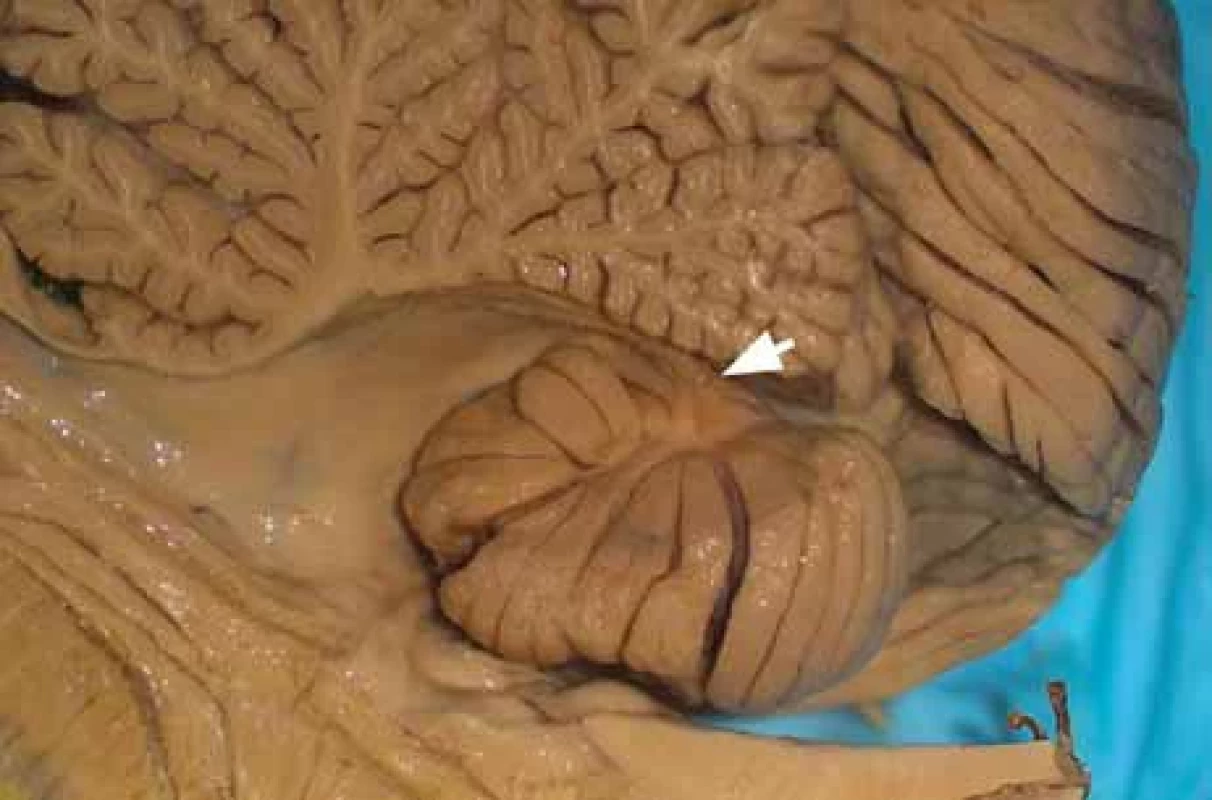
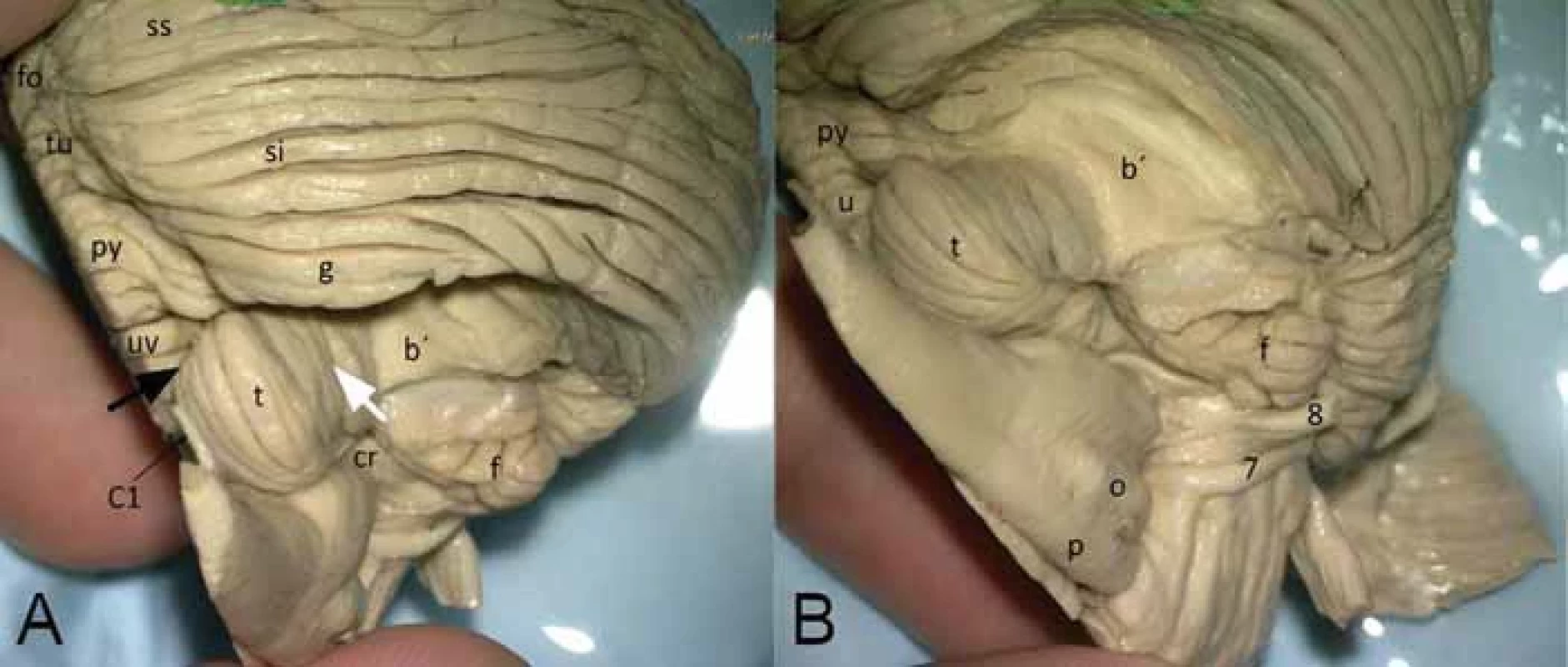
Fig. 4. Posterior (A) and inferior (B) view of the tonsilla cerebelli after removal of the biventer lobule.
(A) Segments of the vermis continuing in the hemispheric lobules; also substantiates similiar relation of the uvula to the tonsil (fo + ss, tu + si and g, pyr + b´, uv + t, cr, f). (B) View of the ventral side of the brain stem and tonsil; on the left is the caudal end of the medulla oblongata and in the middle below is the pons Varoli. black arrow – sulcus uvulotonsillaris; white arrow – fi ssura tonsillobiventerica (secunda); 7 – n. facialis; 8 – n. vestibulocochlearis; b´ – lobulus biventer (partially removed); cr – corpus restiforme; f – fl occulus; fo – folium; g – lobulus gracilis; o – olive; p – pyramis medullae oblongatae; py – pyramis vermis; si – lobulus semilunaris inferior; ss – lobulus semilunaris superior; t – tonsil; tu – tuber; uv – uvula vermis
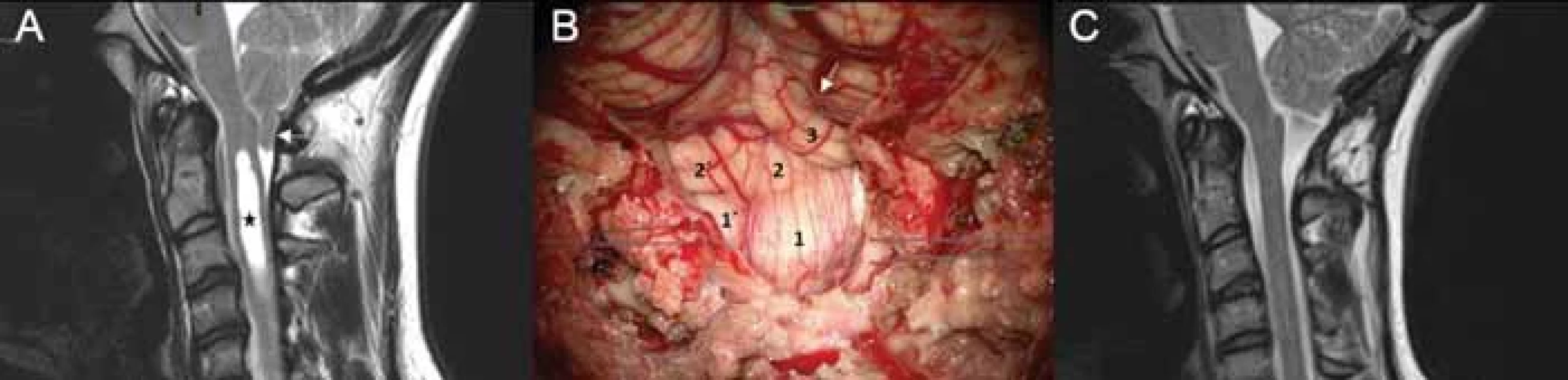
Fig. 5. Surgery of the Chiari malformation type I with syringomyelia.
(A) MRI before surgery showing caudal descent of the tonsil (arrow); syringomyelic cavity (asterix); (B) degenerated structure of the caudal part of the cerebellar tonsil descending below the resected arch of C1 (1,1´ – caudal part of the tonsil has a diff erent structure than its cranial, medulla oblongata non-compressing part 2,2´,3 – caudal part of the lobulus biventer is also dislocated downwards (its folia run obliquely to the course of the tonsillar folia; arrow depicts the fi ssura interbiventerica); (C) MRI 6 months after the surgery documents suffi cient decompression of the medulla oblongata gained by resection of the lower part the cerebellar tonsils with subsequent complete disappearance of the syringomyelic cavity.
Operační anatomie
Z pohledu operační anatomie je důležité, že tonzila je od zbytku mozečku oddělena převážně volnými povrchy (obr. 2), pouze superolaterálně se napojuje na lobulus biventer hemisféry a na uvulu vermis tonzilárním pedunklem (obr. 3).
Ventrální strana horní části tonzily leží na dolním medulárním velu (velum medullare inferius), nodulu a tela choroidea. Nad tonzilou je distální část cerebellomedulární cisterny, takzvaná supratonzilární (telovelotonzilární) štěrbina – cleft. V intimním vztahu s tonzilou probíhá tonzilomedulární a telovelotonzilární segment arteria cerebellaris posterior inferior (PICA). Vzadu mezi oběma tonzilami končí zadní cerebellární incisura jako fissura intertonsillaris neboli vallecula, a jak se kraniálně k sobě tonzily přibližují, ta se mění v intertonzilární sulkus. Ještě kraniálněji je mezi uvulou a tonzilou na vnitřním aspektu hluboký uvulotonzilární sulkus. Mezi tonzilou a lobulus biventer je taktéž hluboká fissura – tonsillobiventerica neboli secunda (obr. 4A, B). Pro orientaci při operaci je významné, že při pohledu subokcipitální kraniotomií folia tonzily směřují vertikálně oproti šikmo (lobulus biventer) a horizontálně směřujícím foliím subokcipitální plochy mozečkové hemisféry (obr. 3, 4A, 5). Dolní a mediální okraj tonzily přiléhá k medulla oblongata a tvoří kaudální hranici cerebellomedulární fissury. Vallecula nás spolu s obexem přivedou do IV. komory skrze foramen Magendie. Znalost anatomie mozečkové tonzily ulehčí její resekci při výkonu v oblasti zadní jámy, u jejího postižení tumorem a při operaci Chiariho malformace (CM) typu I (obr. 5).
Vallecula, intertonzilární, uvulotonzilární sulkus a cerebellomedulární fissura jsou také cestou telovelárního přístupu neboli přístupu cerebellomedulární cisternou (tCMF). Smyslem telovelárního přístupu je zachování jader mozečku, která jsou uložena velice intimně – dorzolaterálně vůči stropu IV. komory a pod kraniální částí vermis – a zde mohou být poškozeny tradičním transvermálním přístupem do IV. komory. Ten může zejména u dětí způsobit takzvaný cerebelární mutizmus [2]. Pro telovelární/tCMF přístup je důležité si uvědomit, že cerebellomedulární fissura je vývojovým ekvivalentem posterolaterální fissury, oddělující flocculus a nodulus od tonzily a uvuly.
Pokud máme popsat naši laboratorní disekci (obr. 6) a některé klinické případy, postupujeme takto: Přístup začínáme preparací intertonzilárního sulku a poté uvulotonzilárního sulku. Dále je nutná znalost průběhu PICA v jejím tonzilomedulárním, telovelotonzilárním a kortikálním segmentu, její kaudální (s těsným vztahem k prodloužené míše) a poté kraniální kličky (loop), přičemž musíme mít na mysli i variety průběhu [3]. Po preparaci sulků a PICA můžeme tonzilu elevovat a odsunout kraniolaterálně a poté odstřihnout tela choroidea při jejím úponu (tenii) podél laterokaudálního okraje fossa rhomboidea, čímž zjednáváme přístup do laterálního recessu IV. komory (obr. 7). Pokud eventuálně dále transcidujeme horizontální raménko plexus choroideus a velum medullare inferius – tenkou vrstvičku neurální tkáně spojující flocullus s nodulem, dosahujeme tím supralaterálního recessu a případně kraniální retrakcí uvuly ozřejmíme fossa rhomboidea až kraniálně do ústí Sylvijského akveduktu (obr. 8).
Tento přístup po své kadaverozní studii navrhl a do klinické praxe zavedl japonský neurochirurg Toshio Matsushima v roce 1992 [4], jeho klíčová publikace pochází z roku 2001 [5]. Jako „telovelární“ přístup jej dále anatomicky dokumentovali a popularizovali Mussi s Rhotonem v roce 2000 [6,7]. Krása tohoto přístupu v sobě snoubí nutnost nabytí detailní znalosti anatomie v laboratoři s následnou elegancí mikrochirurgické manipulace v blízkosti vitálních struktur. Je také nádherné a inspirující pozorovat další společnou práci Matsushimy a Rhotona a pokračování prací v této anatomické oblasti [8]. Koneckonců již na konci článku z roku 2001 Matsushima děkuje Rhotonovi, že v roce 1981 mohl v jeho laboratoři anatomii IV. komory studovat.
Nejedná se o postupem dogmatický přístup – při středočárovém přístupu je vhodné dle rozsahu léze přizpůsobit komplexnost tonzilární a uvulární disekce na: „extensive type“ (pro horní spodinu IV. komory), „lateral wall type“ (pro mozečkové pedunkly) a „lateral recess type“ (pro laterální recessus) [5]. Při prvním typu extenzivně mobilizujeme obě tonzily, a to i oboustrannou uvulotonzilární disekcí, retrakce směřuje spíše kraniálně, tenia je uvolněna oboustranně a stejně tak jsou proťaty telovelární junkce a velum medullare inferius. Pro druhý typ je nutná výraznější laterální retrakce tonzily i lobulus biventer. Postačí však pouze unilaterální otevření tela choroidea, telovelární junkce a velum medullare inferius (pro přístup do supralaterálního recessu) a je vhodný šikmý kontralaterální mikroskopický pohled. Přístup do laterálního recessu je podobný, ale není oproti přístupu k laterální stěně IV. komory nutné preparovat uvulotonzilární sulkus a pochopitelně ani tnout telovelární junkci, postačí odstřižení tenie a otevření laterálního recessu, je tedy nejméně extenzivní. Kromě tohoto klasického středočárového přístupu byl vypracován i laterální jednostranný tCMF přístup [8]. Takto mohou být rozlišeny čtyři typy lézí: (a) intraCMF léze (tedy mimo komoru); (b) intraventrikulární léze, oba typy jsou vhodné pro mediální disekční „cestu“; (c) „čisté“ léze cerebellomedulární cisterny, vhodné pro laterální přístup a (d) léze zasahující jak do CMF, tak i do cerebellomedulární cisterny, vhodné pro kombinaci obou přístupů [9]. U intraventrikulárních lézí byla Matsushimou et al. popsána i nutnost naříznutí dolní části vermis pro přístup do rostrální části IV. komory nebo fastigia [9], tento fakt je podložen i anatomickou studií Tanriovera et al. [10], což jsme zjistili i u našeho pacienta s plexus papilomem (obr. 7). Pro všechny tyto přístupy je však iniciálním jmenovatelem právě anatomie mozečkové tonzily a její mobilizace.
Cévní neurochirurg Lawton et al. podporuje také znalost anatomie tonzily a tonzilobiventerické fissury při propagaci svého supratonzilárního (tonsillobiventeric fissure) přístupu do oblasti dolního cerebelárního pedunklu a zadní části středního [11]. Tento více laterální přístup popisuje jako elegantní a bezpečný u šesti pacientů s kavernomem, ovšem několik dalších slavných neurochirurgů (A. Rhoton, M. G. Yaşargil, A. H. Kaye, M. Samii – v pořadí komentářů ke článku) s ním nesouhlasí, navrhují zejména technicky jednodušší dosažitelnost dolního cerebelárního pedunklu klasickým telovelárním přístupem, při menší kostěné expozici, připomínají nepřesnost navigace danou likvorovou dekompresí a riziko poškození nucleus dentatus. Sám autor přiznává pouze větší riziko poškození distálních větví PICA vystupujích z tonzilobiventerické fissury. I přes výhrady recenzentů Lawton svoji snahu nevzdává a o 10 let později představuje anatomickou studii pro „tonsillobiventeric fissure approach“ i do laterálního recessu IV. komory, a to v její inferolaterální variantě. Za výhodu považuje vertikální směr tonzilobiventerické fissury vzhledem ke kmeni na rozdíl od nevýhodně paralelního směru cerebellomedulární fissury [12]. Tato výhoda vynikne více v jím používané pronační poloze pacienta, pro nás zvyklé operovat v „semisitting“ pozici není tak zřejmá. Lawton kvituje absenci provedení laminektomie C1, v předchozím článku o supratonzilárním přístupu k dolnímu mozečkovému pedunklu [11] ji ale přiznává vzhledem k vyšší trajektorii přístupu jako „optional“, v případě přístupu do laterálního recessu není dle něj nutná ani výraznější anteflexe hlavy. Za další výhodu považuje fakt, že není nutná preparace telovelotonzilárního segmentu PICA, tedy vyhýbá se tím manipulaci s medulárními perforátory tonzilomedulárního a proximálního telovelotonzilárního segmentu, nicméně distální větve PICA (distální telovelotonzilární a kortikální) v ohrožení zůstávají a taktéž i retrotonzilární žíly uvnitř fissury.
Dalším autorem zaobírajícím se tématem středočárového subtonzilárního přístupu je M. Tatagiba [13]. Disekci a elevaci tonzily propaguje při středočárových přístupech k meningeomu hypoglosseálního kanálu [14], meningeomu jugulárního tuberkulu [15] nebo i při glossopharyngeální neuralgii [16]. My jsme ocenili možnost manipulace s tonzilou při laterálním subtonzilárním přístupu k cystickému hemangioblastomu medulla oblongata [17].
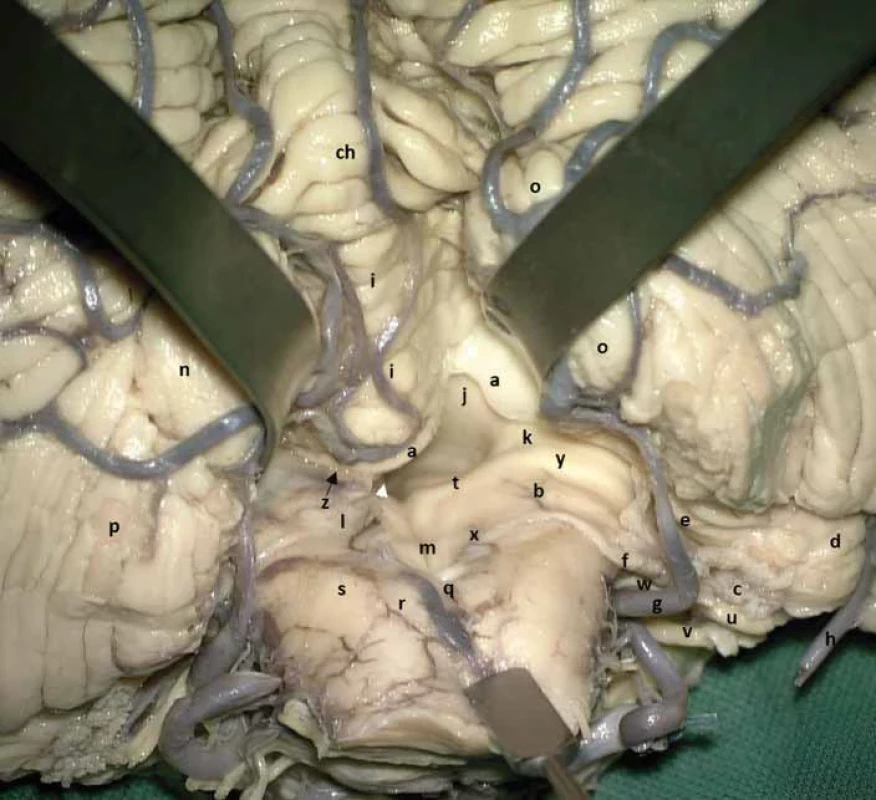
Fig. 6. Laboratory performance of the telovelar approach clarifying anatomical structures of the fossa rhomboidea, its lateral recess, cerebellomedullary fi ssure and cistern. It is worth noting, for example, the rhomboid lip or telovelar junction. The tonsils are not resected, but moved superolaterally with rectractors.
a – velum medulare inferius (partially cut); b – recessus lateralis; c – plexus choroideus; d – fl ocullus; e – pedunculus fl occuli; f – rhomboid lip; g – a. cerebelli inferior posterior; h – a. cerebelli inferior anterior; ch – pyramis; i – uvula; j – peduculus cerebellaris superior; k – pedunculus cerebellaris inferior; l – tela choroidea ventriculi quarti; m – sulcus medianus ventriculi quarti; n – tonsilla cerebelli sinistra; o – tonsilla cerebelli dextra; p – lobulus biventer; q – obex; r – tuberculum gracile (clava); s – tuberculum cuneatum; t – stria medullaris; u – n. statoacusticus; v – n. vagus; w – n. glossopharyngeus; x – tenia choroidea ventriculi quarti; y – tuberculum acusticum; z – telovelar junction; white arrow is directed towards the Sylvian aqueduct
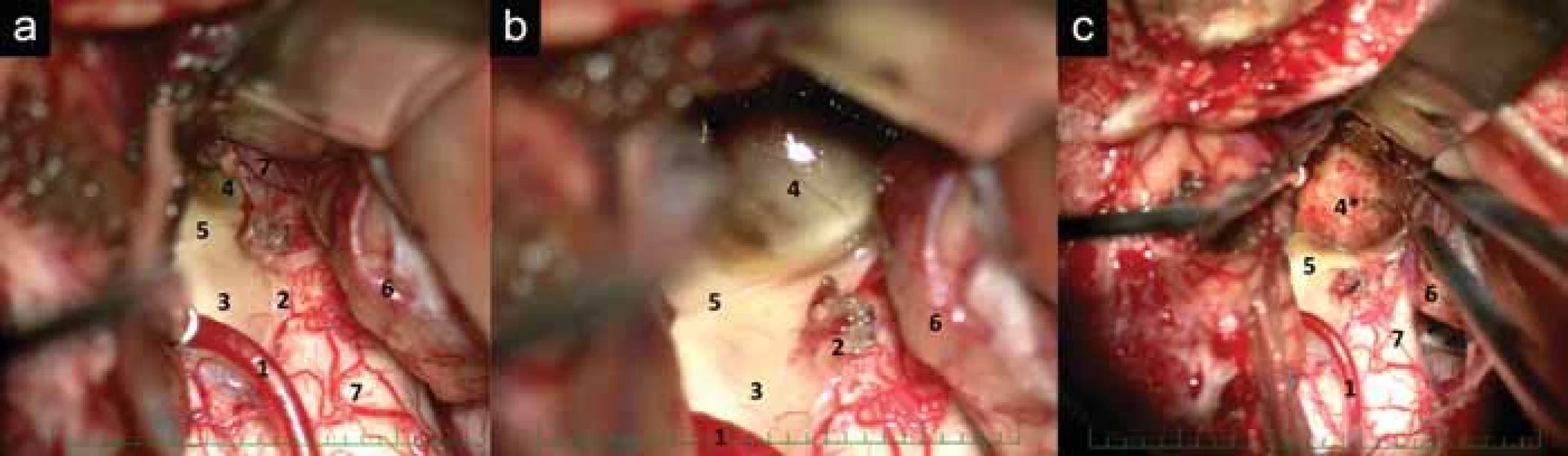
Fig. 7. Surgery of the area acustica cavernoma – (A) telovelar approach; (B) details and clarifi cation of the cavernoma; (C) the cavity after cavernoma resection.
1 – a. cerebelli inferior posterior; 2 – tenia of the tela choroidea; 3 – calmus scriptorius; 4 – cavernoma; 4* – cavity after resection of the cavernoma; 5 – striae medullares; 6 – tonsil; 7 – area of the posterior fascicles nuclei
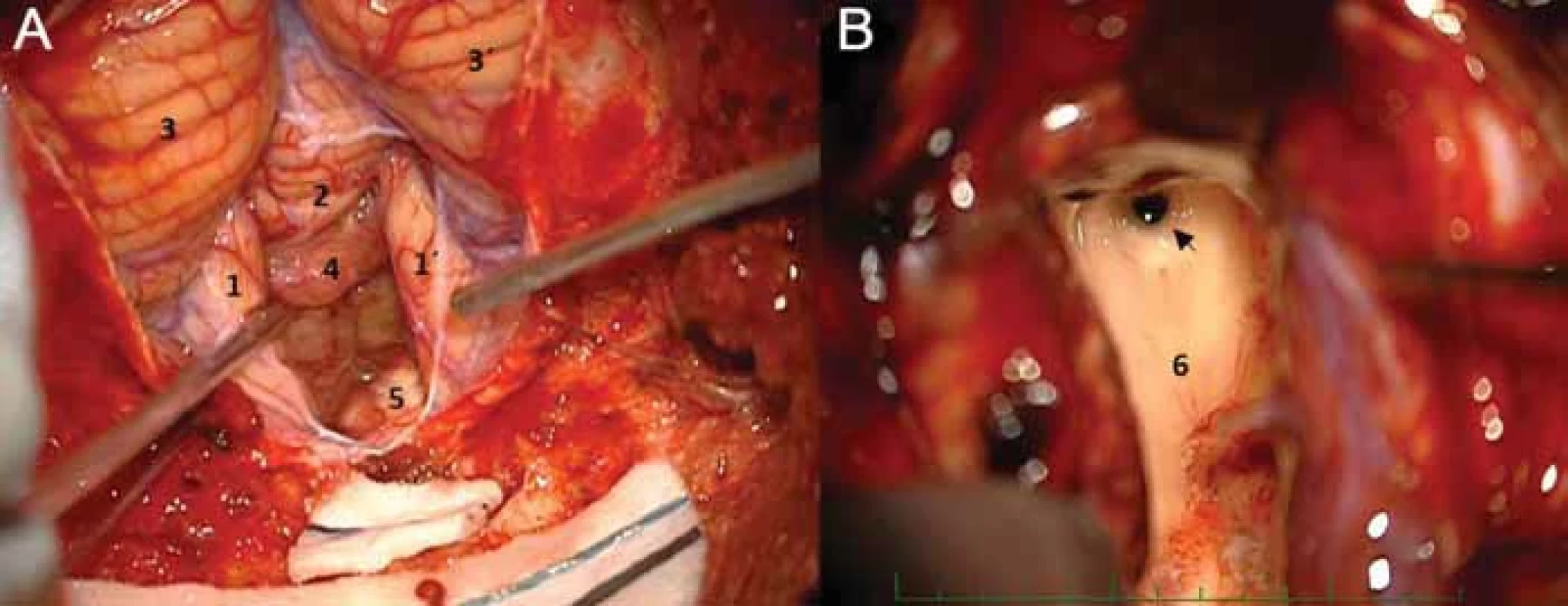
Fig. 8. Surgery of the fourth ventricle plexus papilloma from the telovelar approach – (A) vallecula cerebelli fi lled in by the tumor; (B) view to the Sylvian aqueduct after the completion of the resection with the tumor coat on the fl oor of the 4th ventricle.
1, 1´ – tonsils; 2 – the boundary between the pyramis and uvula; 3, 3´ – cerebellar hemispheres; 4 – plexus papilloma; 5 – medulla oblongata; 6 – fl oor of the 4th ventricle; arrow – aqueductus Sylvii
Klinický význam tonzil mozečku
Tonzily mozečku se funkčně řadí k neocerebellu, vývojově nejmladší části mozečku. Funkční spoje neocerebella jsou převážně z pontu (kortiko-ponto-cerebelární) a jsou zodpovědné za hladké provedení naučených volních pohybů [1,18]. Zdá se, že tonzily (a paraflocullus) hrají klíčovou roli v generaci downbeating nystagmu [19]. Dle některých prací se usuzuje na funkční zapojení tonzil mozečku v patofyziologii migrény [20]. Dle studie Dartory změny v metabolizmu glukózy (dle fludeoxyglukóza [FDG] PET) v tonzilách mohou značit konverzi do mírné kognitivní poruchy u jinak zdravých dospělých [21]. V odborné literatuře je však význam tonzil mozečku zmiňován pro možnost jejich herniace do foramen magnum se svou specifickou symptomatikou. Klinickou prezentaci Chiariho malformace typu I lze rozdělit do tří subtypů na podkladě anatomie dislokovaných struktur zadního mozku: 1) komprese mozečku; 2) komprese mozkového kmene a kraniální míchy; 3) alterace toku mozkomíšního moku skrz foramen magnum. Z mozečkových příznaků byly referovány ataxie, dysmetrie, dyskoordinace. Spinální příznaky zahrnují zejména oslabení a poruchu čití končetin, hyperreflexii a atrofii svalů. Z kmenových příznaků byly referovány nystagmus (horizontální a downbeating nystagmus), diplopie, dysartrie, dysfonie, paralýza hlasivek, ochabnutí patra a atrofie jazyka [22]. U CM1 je nicméně nejčastějším referovaným symptomem bolest hlavy [23]. Mezinárodní klasifikace bolestí hlavy z roku 2018 uvádí diagnostická kritéria bolestí hlavy při CM. Kritéria zahrnují MR specifický nález a okcipitální nebo subokcipitální bolest s vazbou na kašel nebo Valsalvův manévr, která odezní do 5 min a plně vymizí po úspěšném (operačním) vyřešení CM, a přitom není lépe vysvětlitelná jinou etiologií. Bývá asociace s výše uvedenými kmenovými, spinálními nebo mozečkovými příznaky [24]. Méně častými jsou neurokognitivní symptomy – poruchy paměti, afázie, deprese, úzkost a častou popisovanou emocí je strach [23]. Dle Kokurkina et al. byl prokázán signifikantně významný vztah mezi tíží kognitivního deficitu a mírou ektopie mozečkových tonzil [25]. Opomíjeným příznakem při CM je porucha spánku, spánková apnoe (hypopnoe) dle některých zdrojů může být až u 50 % případů CM [26]. Celkem 14–30 % případů CM1 je asymptomatických [27,28]. Vzhledem k tomu, že asymptomatické CM1 i CM1 s mírnou klinikou jsou relativně benigním a neprogresivním onemocněním, je rozumné spíše pacienta sledovat, i když má významnou herniaci tonzil nebo syringomyelii [29]. Při významné intrakraniální expanzi je akutní herniace tonzil mozečku skrze foramen magnum až život ohrožujícím stavem. Může dojít ke kompresi dolního kmene, míchy a přívodných mozkových tepen –PICA, vertebrálních arterií a jejich větví a odstupujícího segmentu přední spinální arterie. Komprese těchto cév vede k ischemii mozkového kmene, tonzil a kaudálního mozečku s příznaky léze těchto důležitých nervových struktur [30]. Herniace tonzil mozečku a CM jsou asociované se syringomyelií. Syringomyelický syndrom je dán lézí přední míšní komisury a má specifický klinický obraz. Jedná se o segmentální lézi algického a termického čití (taktilní je zachováno) a segmentální chabou parézu horních končetin s atrofiemi a fascikulacemi [31]. V případě syringobulbie jsou i symptomy léze mozkového kmene, nejčastěji se projevující jako bulbární syndrom, případně Hornerův syndrom, nystagmus nebo poruchy dýchání. Pro diagnostiku může být matoucí, že se léze může projevovat i unilaterální hemiparézou [32,33].
Cerebelární ektopie a Chiariho malformace
Cerebelární ektopie (a herniace tonzil mozečku) může být vrozená (CM) i získaná při tlakovém efektu okolních struktur (mass effect) nebo při změnách tlakových poměrů mozkomíšního moku. CM představují spektrum nejčastějších kongenitálních malformací cervikokraniální junkce s poklesem mozečkových tonzil a někdy i mozkového kmene skrze foramen magnum. Liší se příznaky, věkem jejich nástupu a etiologií asociovanou se syringomyelií [26,34,35]. Hans Chiari, rakouský patolog a anatom dlouhodobě působící i v Čechách (byl dokonce poslancem Českého zemského sněmu), v roce 1891 popsal tři varianty malformací mozečku, které spojuje herniace struktur zadní jámy lební do cervikokraniální junkce, čtvrtou variantu popsal následně v roce 1896. Chiari I (CM1) je charakterizována sestupem tonzil mozečku pod foramen magnum a je nejčastějším typem CM [35,36]. Chiari II (CM2) již představuje větší herniaci rhombencephala skrze cervikokraniální junkci a je asociovaná se syringomyelií, lumbosakrální dysraphií a defekty neurální trubice [34]. Incidence myelomeningokély asociované s CM2 nicméně klesá po zavedení prenatální suplementace foláty [37]. Chiari III byla Chiarim popsána na základě jediného případu kazuistiky pětiměsíčního dítěte s rozštěpem páteře, zvětšenou lebkou, konvergentním strabismem, absencí tentoria, cervikální hydromyelokélou komunikující se IV. komorou a kompletní herniací mozečku do páteřního kanálu [34]. Chiari IV (CM4) představuje mozečkovou hypoplazii, mozeček není herniován do kraniocervikální junkce. Na rozdíl od CM4 je Dandy Walkerova varianta charakterizována agenezí nebo hypotrofií vermis mozečku s cystickou dilatací IV. komory a dislokací tentoria kraniálně [38].
Syringomyelie může být přítomna i u minimální herniace tonzil, a proto někteří autoři navrhli další stupeň – Chiari 0 (CM0). CM0 odpovídá herniaci tonzil mozečku méně než 3 mm s přítomností syringomyelie (interval 3–5 mm je považován za hraniční) [34]. Pro diagnózu CM0 bez syringomyelie je potřeba symptomů specifických pro CM1, neboť mnoho MR obrazů odpovídajících CM0 je asymptomatických. Benefit chirurgického řešení CM0 by měl být dále zkoumán v prospektivních kontrolovaných studiích [39]. V průběhu let různí autoři definovali další typy CM. Chiari 0,5 definuje Morgenstern termínem „tonsillar wrapping“, kdy radiologický nález nesplňuje kritéria CM1, ale tonzily mozečku již ventrolaterálně „obalují“ prodlouženou míchu [40]. Chiari 1,5 představuje na rozdíl od CM1 i herniaci mozkového kmene [26]. Chiari 3,5 navrhl Fisahn na základě jedné historické kazuistiky rozsáhlé vrozené malformace okcipitocervikální encefalokély, absencí krku s patologickým uložením střeva v zadním mediastinu a komunikací encefalokély s jícnem a žaludkem [41]. Tubbs v roce 2012 navrhl do klasifikace přidat Chiari V na základě jednoho případu hydrocefalu s agenezí mozečku, okcipitální herniací skrze foramen magnum a sakrální myelomeningokélou [42]. V odborné literatuře se můžeme setkat i s další klasifikací, která rozděluje CM na typ A (se syringomyelií) a typ B (bez syringomyelie) [43].
Získaná cerebelární ektopie (Chiari-like)
V klinické praxi se mohou objevovat případy, které napodobují CM, ale vznikají na jiném patofyziologickém podkladě. Rozlišení těchto stavů a porozumění jim může pomoci k volbě optimální léčebné strategie a vyhnutí se zbytným chirurgickým výkonům. Postraumatická arachnoiditida kraniocervikální junkce může být následkem porodního poranění a perinatálního krvácení. V kraniocervikální junkci při CM bývá často zesílení tvrdé pleny (v literatuře referováno jako „durální proužek“ [„dural band“]), nicméně toto zesílení může vznikat i postraumaticky, redukovat prostor v cisterna magna, komprimovat tonzily a imitovat CM [44]. Herniace tonzil mozečku je spojena i se spontánní intrakraniální hypotenzí s klinickými příznaky posturální bolesti hlavy, s nauzeou, zvracením a kognitivním deficitem. Pro diagnostiku lze použít CT myelogram, MR myelogram, popřípadě digitální subtrakční myelogram. Na MR mozku bývá navíc enhancement tvrdé pleny, mozek se jeví povislý, bývají rozšířené venózní siny a bývá zvětšena hypofýza. Intrakraniální hypotenzi lze řešit krevní zátkou či chirurgicky [44–46]. Idiopatická intrakraniální hypertenze může vést k obrazu CM. Na MR bývají známky intrakraniální hypertenze vč. nálezu prázdného sedla (empty sella), tortuozity očních nervů a zvýšené akumulace mozkomíšního moku podél nich. Při likvorovém vyšetření je měřen vysoký intratekální tlak. MR obraz CM bývá asociován i s cystami (např. arachnoidálními či choroidálního plexu), které vedou k poklesu mozečkových tonzil svým tlakovým/objemovým efektem v zadní jámě [44]. Podobně mohou působit prostorově významné změny zadní jámy, intrakraniální hematomy, hydrocefalus či mozkový edém [34]. Byla popsána symptomatická herniace mozečkových tonzil po lumbální drenáži, lumboperitoneálním shuntu, ale i po supratentoriální shuntové operaci [26,47,48]. Abnormálním vývojem mezodermu může dojít k patologii cervikokraniální junkce, při které dochází k poklesu mozečkových tonzil, příkladem může být bazilární imprese/invaginace, hypoplazie klivu, retrokurvace dentu čepovce, okcipitalizace atlasu a syndrom Klippel-Feil [26]. Bazilární impresí, invaginací se rozumí patologie cervikokraniální junkce, ať již vrozená, či degenerativní, při které periforaminální kostěnné struktury (případně dens axis) jsou invaginovány do zadní jámy a při relativní imobilitě tentoria komprimují struktury zadní jámy [49,50]. Někteří autoři specifikují invaginaci jako vrozenou anomálii, zatímco impresi jako lézi získanou [51]. CM může vznikat sekundárně při malé zadní jámě a často se vyskytuje u takových onemocnění, jako jsou achondroplazie, fibrózní dysplazie či kraniosynostóza [26,34].
Zobrazení u Chiariho malformace
Radiologicky je na CM1 usuzováno při herniaci tonzil mozečku o 5 a více mm pod foramen magnum [34]. Pro diagnostiku poklesu tonzil pod foramen magnum se používá základní MR zobrazení [22]. Je nutné podotknout, že posuzování ektopie mozečku u CM1 na MR se může značně lišit mezi posuzujícími, a dle Lawrence je doporučováno posuzování MR více specialisty před definitivní diagnózou CM1, zejména před chirurgickým výkonem. Pozice tonzil je k foramen magnum posuzována ve střední sagitální rovině vůči McRaeově linii (McRaeova linie spojuje basion a opisthion, nejpřednější a nejzadnější bod foramen magnum ve střední sagitální rovině) [52,53]. Tonzily mozečku jsou nicméně paramediální struktury, a to je potřeba zohlednit při posuzování herniace ve střední sagitální rovině. Někteří autoři doporučují měření polohy tonzil vůči foramen magnum i v koronární rovině [54]. Základní MR zobrazení nám navíc neřekne nic o dynamice mozkomíšního moku. Vyšetření MR s fázovým kontrastem (cine flow MR) nám poskytne informaci o cirkulaci mozkomíšního moku ve foramen magnum. Za normálních okolností při systole mok směřuje kaudálně skrz foramen zadním subarachnoidálním prostorem (za mozkovým kmenem), při diastole kraniálně předním subarachnoidálním prostorem (před mozkovým kmenem). Vyšetření MR s fázovým kontrastem (cine flow) nám může odhalit patologii cirkulace likvoru při CM. Některé studie vyzdvihují použití těchto sekvencí MR jako diagnostický prostředek pro CM [22]. Za normálních okolností je rychlost toku mozkomíšního moku v subarachnoidálním prostoru kraniocervikální junkce vcelku konstantní a s nižšími vrcholovými průtokovými rychlostmi (peak systolic velocity; PSV) (systolická PSV 1,2–3,3 cm/s, diastolická PSV 1,6–4,5 cm/s). U symptomatických pacientů s CM1 nejsou toky při vyšetření MR fázovým kontrastem uniformní (místy je v subarachnoidálním prostoru urychlení a místy zpomalení) a bývá signifikantně vyšší urychlení toku (systolická PSV 1,8–4,8 cm/s, diastolická PSV 2,5–5,3 cm/s) [55]. Pro měření dynamiky likvoru ve foramen magnum lze využít i ultrazvuk, který lze s výhodou provádět i peroperačně při chirurgické dekompresi [56].
Syringomyelie a syrinx
Chiari i další vědci začali zkoumat souvislost mezi mozečkovou ektopií a patologií likvorových cest (hydrocefalem a syringomyelií). Vzniklo mnoho teorií pro formaci syrinx u CM1. Moderní zobrazovací metody ve studii Oldfielda a Heisse podporují teorii, že herniace tonzil mozečku do foramen magnum narušuje cirkulaci likvoru během srdečního cyklu, při systole klesá mozeček do foramen, omezuje tím tok likvoru skrze foramen magnum a zvyšuje se tlak, který působí na míchu v subarachnoidálních prostorech, tím se formuje dutina – syrinx [34,57]. Syrinx je patologickým substrátem pro specifický typ myelopatie, syringomyelii. Naproti tomu termín hydromyelie se používá pro patologické rozšíření centrálního míšního kanálu [58]. V případě zasahování syringomyelické dutiny do mozkového kmene hovoříme o syringobulbii [32]. Chirurgická intervence zvětšující likvorový prostor ve foramen magnum uvolní cirkulaci likvoru, tonzily mozečku nabudou normální pozice a tvaru (pokud nejsou resekovány) a syrinx regreduje [34]. Nutno poznamenat, že není evidence pro chirurgické řešení asymptomatické syringomyelie či hydromyelie [58]. Obecně je syringomyelie asociovaná s poruchou cirkulace likvoru ve foramen magnum nebo na spinální úrovni např. u CM1, arachnoiditidy nebo bazilární invaginace [59]. Klinicky je významné, že syringomyelie se může vyskytovat i u spontánní intrakraniální hypotenze (neřeší se tedy primárně dekompresní operací) [60].
Chirurgické techniky u Chiariho malformace typu I
Chirurgický přístup k CM1 nemá jasný konsenzus, v roce 2020 publikovali Arnautovic et al. [61] přehled 145 operačních sérií z let 1965–2013 z USA i Evropy, průměrný počet pacientů v každé sérii byl 31, tedy celkově se jednalo o úctyhodných 4 495 pacientů. Většinou (v 99 %) byla jako operační výkon referována dekomprese zadní jámy/foramen magnum, v 92 % byla otevřena dura, poté byl v 65 % proveden určitý stupeň arachnoidální disekce, který v 27 % vyústil v resekci tonzil. Americká prospektivní multicentrická studie publikovaná ve stejném roce [62] zahrnula 68 dětských pacientů, operovaných 14 chirurgy, primárním sledovaným výsledkem byl efekt na syringomyelii, přičemž hranicí uspokojivého vývoje byla její > 50% redukce, 42 pacientů podstoupilo dekompresi zadní jámy s duroplastikou a redukcí objemu tonzil (PFDD-T) a 26 podstoupilo stejnou proceduru bez manipulace s tonzilami (PFDD). Ke kýženému výsledku došlo v 52 % u skupiny PFDD a v 63,6 % u skupiny PFDD-T, ovšem bez statistické významnosti profitu redukce objemu tonzil. Daleko větší, ale retrospektivní kohortu 437 dětí zpracovali v roce 2023 Braga et al. [63], zde vychází jednoznačně lépe redukce objemu tonzil, syringomyelie se zlepšila po 79,8 % operací typu PFDD-T oproti 58,7 % typu PFDD. Doporučení vydaná v systematickém přehledu CNS (Congress of Neurological Surgeons) publikovaném v roce 2023 v časopise Neurosurgery [64], konstatují na cílený dotaz týkající se benefitu redukce tonzil u CM1, že „chirurgové mohou provést resekci nebo redukci tonzily mozečku pro zlepšení syrinx a/nebo symptomů“. Dle našeho názoru po vyloučení instability kraniocervikálního přechodu neurochirurg, pro kterého je intradurální operativa běžnou procedurou a cítí, že během resekce tonzil u daného pacienta neriskuje, by měl resekci tonzil při ošetření CM1 provést, a to do té míry, kdy je anatomicky restituováno proudění likvoru v oblasti kraniocervikálního přechodu, obex je zcela volný a nehrozí ani riziko budoucího sestupu zbytku tonzil. Přínosnou pro tuto problematiku může být „technická poznámka“ tří evropských pracovišť stupňující manipulaci s tonzilami do [65] „Tří R“ – jedná se o (1) intrakraniální repozici pomocí koagulace; dále (2) o subpiální aspiraci a redukci objemu tonzily a nakonec (3) resekci, která je prováděna zejména u sklerotických tonzil. Jednotlivé výkony jsou komplementární a rozsah výkonu je proveden dle „pocitu“ dostatečnosti dekomprese. Individuální rozhodnutí u daného pacienta proponuje i recentní zkušenost vídeňského pracoviště s 81 pacienty [66]. Výkon pouze s naříznutím nebo snesením vnější vrstvy ztluštělé dury (tedy bez otevření dury) je nejméně rizikový, ovšem nese s sebou největší pravděpodobnost selhání, byl proveden 11 pacientům v souboru (14 %). Nejvyšší počet chirurgických komplikací měla pouhá arachnoidální disekce a manipulace s tonzilami provedená u 21 pacientů při dekompresi foramen magnum spojené s duroplastikou (PFDD celkově provedena u 45/81 pacientů, tzn. 56 %). Lze namítnout, že se jednalo v naprosté většině případů „pouze“ o likvorovou píštěl, pouze u jednoho pacienta došlo k intradurálnímu krvácení s nutností následné resekce tonzily. Resekce nebo subpiální redukce objemu tonzil byla primárně provedena 25 pacientům (31 %) a byla spojena s nejlepším klinickým výsledkem v Chicago Chiari Outcome Scale (COOS), nicméně opět v jednom případě nastala vážná komplikace daná trombózou jedné PICA s nutností urgentní revize.
„Volba ideálního neurochirurgického výkonu pro CM1 zůstává jednou z největších debat na poli dětské neurochirurgie“ [63] a náš přehledný referát tento problém nemá ambici a ani nemůže vyřešit, nicméně domníváme se, že i u této diagnózy detailní znalost mikroanatomie mozečkové tonzily umožní neurochirurgovi racionálně se během výkonu rozhodnout a operaci provést pokud možno nekomplikovaně.
Závěr
Tonzily mozečku jsou součástí neocerebella a mají specifické postavení v kraniocervikální junkci. Herniace tonzil mozečku skrze foramen magnum má variabilní klinický obraz od absence symptomů až po život ohrožující stav při kmenové lézi. Spektrum vrozených CM je poměrně široké, s různým klinickým významem – nejčastějším typem je typ I. Při obstrukci likvorových cest ve foramen magnum může vzniknout syringomyelie, stav často asociovaný s CM. MR je metodou volby pro zobrazení herniace mozečkových tonzil a patologické cirkulace mozkomíšního moku. Znalost anatomie a možností operačních přístupů nám umožňuje volbu vhodné operační techniky chirurgie zadní jámy a cervikokraniální junkce.
Grantová podpora
Práce byla částečně podpořena grantem IGA-KZ-2021 - 1-16.
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Zdroje
1. Bispo RFM, Ramalho AJC, Gusmão LCB et al. Cerebellar vermis: topography and variations. Int J Morphol 2010; 28 (2): 439–443. doi: 10.4067/S0717-95022010000200018.
2. Radovnický T, Sameš M. Cerebelární mutizmus po resekci meduloblastomu u dítěte – kazuistika. Cesk Slov Neurol N 2008; 71/104 (4): 483–486.
3. Ucerler H, Saylam C, Cagli S et al. The posterior inferior cerebellar artery and its branches in relation to the cerebellomedullary fissure. Clin Anat 2008; 21 (2): 119–126. doi: 10.1002/ca.20581.
4. Matsushima T, Fukui M, Inoue T et al. Microsurgical and magnetic resonance imaging anatomy of the cerebellomedullary fissure and its application during fourth ventricle surgery. Neurosurgery 1992; 30 (3): 325–330. doi: 10.1227/00006123-199203000-00003.
5. Matsushima T, Inoue T, Inamura T et al. Transcerebellomedullary fissure approach with special reference to methods of dissecting the fissure. J Neurosurg 2001; 94 (2): 257–264. doi: 10.3171/jns.2001.94.2.0257.
6. Mussi AC, Rhoton AL Jr. Telovelar approach to the fourth ventricle: microsurgical anatomy. J Neurosurg 2000; 92 (5): 812–823. doi: 10.3171/jns.2000.92.5.0812.
7. Mussi AC, Matushita H, Andrade FG et al. Surgical approaches to IV ventricle – anatomical study. Childs Nerv Syst 2015; 31 (10): 1807–1814. doi: 10.1007/s00381-015 - 2809-0.
8. Akiyama O, Matsushima K, Nunez M et al. Microsurgical anatomy and approaches around the lateral recess with special reference to entry into the pons. J Neurosurg 2018; 129 (3): 740–751. doi: 10.3171/2017.5.JNS17251.
9. Matsushima T, Rutka J, Matsushima K. Evolution of cerebellomedullary fissure opening: its effects on posterior fossa surgeries from the fourth ventricle to the brainstem. Neurosurg Rev 2021; 44 (2): 699–708. doi: 10.1007/s10143-020-01295-2.
10. Tanriover N, Ulm AJ, Rhoton AL Jr et al. Comparison of the transvermian and telovelar approaches to the fourth ventricle. J Neurosurg 2004; 101 (3): 484–498. doi: 10.3171/jns.2004.101.3.0484.
11. Lawton MT, Quiñones-Hinojosa A, Jun P. The supratonsillar approach to the inferior cerebellar peduncle: anatomy, surgical technique, and clinical application to cavernous malformations. Neurosurgery 2006; 59 (4 Suppl 2): ONS244–251. doi: 10.1227/01.NEU.0000232767.16809.68.
12. Tayebi Meybodi A, Lawton MT, Tabani H et al. Tonsillobiventral fissure approach to the lateral recess of the fourth ventricle. J Neurosurg 2017; 127 (4): 768–774. doi: 10.3171/2016.8.JNS16855.
13. Herlan S, Roser F, Ebner FH et al. The midline suboccipital subtonsillar approach to the cerebellomedullary cistern: how I do it. Acta Neurochir (Wien) 2017; 159 (9): 1613–1617. doi: 10.1007/s00701-017-3270-5.
14. Tatagiba M, Koerbel A, Roser F. The midline suboccipital subtonsillar approach to the hypoglossal canal: surgical anatomy and clinical application. Acta Neurochir (Wien) 2006; 148 (9): 965–969. doi: 10.1007/s00701-006-0816-3.
15. Lieber S, Nunez M, Evangelista-Zamora R et al. Mid - line suboccipital subtonsillar approach with C1 laminectomy for resection of foramen magnum meningioma: 2-dimensional operative video. J Neurol Surg B Skull Base 2019; 80 (Suppl 4): S365–S367. doi: 10.1055/s-0039 - 1698823.
16. Roser F, Ebner FH, Schuhmann MU et al. Glossopharyngeal neuralgia treated with an endoscopic assisted midline suboccipital subtonsillar approach: technical note. J Neurol Surg A Cent Eur Neurosurg 2013; 74 (5): 318–320. doi: 10.1055/s-0032-1327447.
17. Bartoš R, Lodin J, Marek T et al. Combined treatment of a medulla oblongata hemangioblastoma via permanent cysto-cisternal drainage and (postponed) gamma knife radiosurgery: a case report and review of the literature. Int J Neurosci 2020; 9 : 1–5. doi: 10.1080/00207454. 2020.1819267.
18. Schlerf JE, Verstynen TD, Ivry RB et al. Evidence of a novel somatopic map in the human neocerebellum during complex actions. J Neurophysiol 2010; 103 (6): 3330–3336. doi: 10.1152/jn.01117.2009.
19. Eulenburg P, Best C, Bense S et al. Hypometabolism in cerebellar tonsil and flocculus regions during downbeat nystagmus. Aktuelle Neurologie 2005; 32 (S4): S2005-919329. doi: 10.1055/s-2005-919329.
20. Karsan N, Bose PR, O’Daly O et al. Alterations in functional connectivity during different phases of the triggered migraine attack. Headache 2020; 60 (7): 1244–1258. doi: 10.1111/head.13865.
21. Dartora CM, Koole M, da Silva AMM. Glucose metabolism changes in cerebellar tonsils as an early predictor of cognitive decline. Alzheimer Dementia 2021; 17 (S4): e054007. doi: 10.1002/alz.054007.
22. Steinman SG, Plunkett S. Understanding Chiari malformations. Pract Neurol Bryn Mawr Commun 2022; 6.
23. Fischbein R, Saling JR, Marty P et al. Patient-reported Chiari malformation type I symptoms and diag - nostic experiences: a report from the national Conquer Chiari Patient Registry database. Neurol Sci 2015; 36 (9): 1617–1624. doi: 10.1007/s10072-015-2219-9.
24. Headache Classification Committee of the International Headache Society (IHS) The International Classification of Headache Disorders, 3rd ediditon. Cephalagia 2018; 38 (1): 1–211. doi: 10.1177/0333102417738202.
25. Kokurkina RG, Mendelevich EG. Cognitive dysfunction in patients with Chiari malformation type 1 and its relationship with the degree of cerebellar tonsil ectopia. Neurol Neuropsychiatr Psychosomat 2022; 14 (4): 20–24. doi: 10.14412/2074-2711-2022-4-20-24.
26. Moncho SJD, Ferré A, López-Bermeo D et al. A critical update of the classification of Chiari and Chiari-like malformations. J Clin Med 2023; 12 (14): 4626. doi: 10.3390/jcm12144626.
27. Meadows J, Kraut M, Guarnieri M et al. Asymptomatic Chiari type I malformations identified on magnetic resonance imaging. J Neurosurg 2000; 92 (6): 920–926. doi: 10.3171/jns.2000.92.6.0920.
28. Elster AD, Chen MY. Chiari I malformations: clinical and radiologic reappraisal. Radiology 1992; 183 (2): 347–353. doi: 10.1148/radiology.183.2.1561334.
29. Langridge B, Phillips E, Choi D. Chiari malformation type 1: a systematic review of natural history and conservative management. World Neurosurg 2017; 104 : 213–219. doi: 10.1016/j.wneu.2017.04.082.
30. Munakomi S, Das JM. Brain herniation. [online]. Dostupné z: http: //www.ncbi.nlm.nih.gov/books/NBK 542246/.
31. Ambler Z, Bednařík J, Růžička E. Klinická neurologie – část obecná. Praha: Triton 2008.
32. Shen J, Shen J, Huang K et al. Syringobulbia in patients with Chiari malformation type I: a systematic review. Biomed Res Int 2019; 2019 : 4829102. doi: 10.1155/2019/ 4829102.
33. Agrawal A, Kohat AK, Sahu Ch et al. Syringobulbia with syringomyelia presenting as unilateral multiple cranial nerve palsies with ipsilateral hemiparesis in an adult: a rare case and literature review. Ann Indian Acad Neurol 2023; 26 (4): 601–603. doi: 10.4103/aian.aian_33_23.
34. Rosenblum JS, Pomeraniec IJ, Heiss JD. Chiari malformation (update on diagnosis and treatment). Neurol Clin 2022; 40 (2): 297–307. doi: 10.1016/j.ncl.2021.11.007.
35. Kular S, Cascella A. Chiari I malformation. [online]. Dostupné z: http: //www.ncbi.nlm.nih.gov/books/NBK55 4609/.
36. Ambler Z, Bednařík J, Růžička E. Klinická neurologie – část speciální. Praha: Triton 2010.
37. Khalaveh F, Seidl R, Czech T et al. Myelomeningocele-Chiari II malformation – neurological predictability based on fetal and postnatal magnetic resonance imaging. Prenat Diagn 2021; 41 (8): 922–932. doi: 10.1002/ pd.5987.
38. Zamora EA, Tahani A. Dandy-Walker malformation. [online]. Dostupné z: http: //www.ncbi.nlm.nih.gov/books/NBK538197/.
39. Bogdanov EI, Faizutdinova AT, Heiss JD. The small posterior cranial fossa syndrome and Chiari malformation type 0. J Clin Med 2022; 11 (18): 5472. doi: 10.3390/jcm11185472.
40. Morgenstern PF, Tosi U, Uribe-Cardenas R et al. Ventrolateral tonsillar position defines novel Chiari 0.5 classification. World Neurosurg 2020; 136 : 444–453. doi: 10.1016/j.wneu.2020.01.147.
41. Fisahn Ch, Shoja MM, Turgut M et al. The Chiari 3.5 malformation: a review of the only reported case. Childs Nerv Syst 2016; 32 (12): 2317–2319. doi: 10.1007/ s00381-016-3255-3.
42. Tubbs RS, Muhleman M, Loukas M et al. A new form of herniation: the Chiari V malformation. Childs Nerv Syst 2012; 28 (2): 305–307. doi: 10.1007/s00381-011-1616-5.
43. Sova M, Smrčka M, Smrčka V et al. Chiariho malformace – vlastní zkušenosti. Cesk Slov Neurol N 2007; 70/103 (3): 304–307.
44. Park RJ, Unnikrishnan S, Berliner J et al. Cerebellar tonsillar descent mimicking Chiari malformation. J Clin Med 2023; 12 (8): 2786. doi: 10.3390/jcm12082786.
45. Chan TLH, Vuong K, Chugh T et al. Cerebellar tonsillar descent: a diagnostic dilemma between Chiari malformation type 1 and spinal cerebrospinal fluid leak. Heliyon 2021; 7 (4): e06795. doi: 10.1016/j.heliyon.2021. e06795.
46. Zítek H, Stratilová M, Radovnický T et al. Spontánní intrakraniální hypotenze. Cesk Slov Neurol N 2022; 85/118 (1): 18–23. doi: 10.48095/cccsnn202218.
47. Sugrue PA, Hsieh PC, Getch CC et al. Acute symptomatic cerebellar tonsillar herniation following intraoperative lumbar drainage: case report. J Neurosurg 2009; 110 (4): 800–803. doi: 10.3171/2008.5.17568.
48. Lazareff JA, Kelly J, Saito M. Herniation of cerebellar tonsils following supratentorial shunt placement. Childs Nerv Syst 1998; 14 (8): 394–397. doi: 10.1007/s00 3810050252.
49. Donnally ICJ, Munakomi S, Varacallo M. Basilar invagination. [online]. Dostupné z: http: //www.ncbi.nlm.nih.gov/books/NBK448153/.
50. Hinck VC, Hopkins CE, Savara BS. Diagnostic criteria of basilar impression. Radiology 1961; 76 (4): 572–585. doi: 10.1148/76.4.572.
51. Pinter NK, McVige J, Mechtler L. Basilar invagination, basilar impression, and platybasia: clinical and imaging aspects. Curr Pain Headache Rep 2016; 20 (8): 49. doi: 10.1007/s11916-016-0580-x.
52. Lawrence BJ, Urbizu A, Allen PA et al. Cerebellar tonsil ectopia measurement in type I Chiari malformation patients show poor inter-operator reliability. Fluids Barriers CNS 2018; 15 (1): 33. doi: 10.1186/s12987-018-0118-1.
53. Barros DPM, Ribeiro ECO, Nascimento JJC et al. Reliability and agreement in the cerebellar tonsil tip localization: two methods using the McRae line concept in MRI. World Neurosurg 2022; 165: e611–e618. doi: 10.1016/ j.wneu.2022.06.108.
54. Tubbs RS, Yan H, Demerdash A et al. Sagittal MRI often overestimates the degree of cerebellar tonsillar ectopia: a potential for misdiagnosis of the Chiari I malformation. Childs Nerv Syst 2016; 32 (7): 1245–1248. doi: 10.1007/s00381-016-3113-3.
55. Haughton VM, Korosec FR, Medow JE et al. Peak systolic and diastolic CSF velocity in the foramen magnum in adult patients with Chiari I malformations and in normal control participants. AJNR Am J Neuroradiol 2003; 24 (2): 169–176.
56. Filip M, Linzer P, Šámal F et al. Peroperační měření průtoku likvoru pomocí ultrazvuku. Cesk Slov Neurol N 2011; 74/107 (3): 320–324.
57. Oldfield EH. Pathogenesis of Chiari I – pathophysiology of syringomyelia: implications for therapy: a summary of 3 decades of clinical research. Neurosurgery 2017; 64 (CN Suppl 1): 66–77. doi: 10.1093/neuros/nyx377.
58. Leclerc AL, Matveeff L, Emery E et al. Syringomyelia and hydromyelia: current understanding and neurosurgical management. Rev Neurol 2021; 177 (5): 498–507. doi: 10.1016/j.neurol.2020.07.004.
59. Bogdanov EI, Heiss JD, Mendelevich EG et al. Clinical and neuroimaging features of „idiopathic“ syringomyelia. Neurology 2004; 62 (5): 791–794. doi: 10.1212/01.wnl.0000113746.47997.ce.
60. Middlebrooks EH, Okromelidze L, Vilanilam GK et al. Syrinx secondary to Chiari-like tonsillar herniation in spontaneous intracranial hypotension. World Neurosurg 2020; 143: e268–e274. doi: 10.1016/j.wneu.2020.07.108.
61. Arnautovic A, Splavski B, Boop FA et al. Pediatric and adult Chiari malformation type I surgical series 1965–2013: a review of demographics, operative treatment, and outcomes. J Neurosurg Pediatr 2015; 15 (2): 161–177. doi: 10.3171/2014.10.PEDS14295.
62. Koueik J, Sandoval-Garcia C, Kestle JRW et al. Outcomes in children undergoing posterior fossa decompression and duraplasty with and without tonsillar reduction for Chiari malformation type I and syringomyelia: a pilot prospective multicenter cohort study. J Neurosurg Pediatr 2019; 18 : 1–9. doi: 10.3171/2019.8.PEDS19154.
63. Braga BP, Montgomery EY, Weprin BE et al. Cerebellar tonsil reduction for surgical treatment of Chiari malformation type I in children. J Neurosurg Pediatr 2023; 10 : 1–10. doi: 10.3171/2023.1.PEDS22222.
64. Pattisapu JV, Ackerman LL, Infinger LK et al. Congress of neurological surgeons systematic review and evidence-based guidelines for patients with Chiari malformation: surgical interventions. Neurosurgery 2023; 93 (4): 731–735. doi: 10.1227/neu.0000000000002635.
65. Galarza M, Gazzeri R, Alfieri A et al. „Triple R“ tonsillar technique for the management of adult Chiari I malformation: surgical note. Acta Neurochir (Wien) 2013; 155 (7): 1195–1201. doi: 10.1007/s00701-013-1749-2.
66. Khalaveh F, Steiner I, Reinprecht A et al. Individualized surgical treatment of Chiari 1 malformation: a single-center experience. Clin Neurol Neurosurg 2023; 230 : 107803. doi: 10.1016/j.clineuro.2023.107803.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2024 Číslo 1
-
Všechny články tohoto čísla
- Nízkotlaký hydrocefalus
- Tonsilla cerebelli – anatomie, funkce a její význam pro neurochirurgii
- Editorial
- Využitie umelej inteligencie pri hodnotení obrazu CT u pacientov s CMP – aktuálne možnosti
- Adaptace a psychometrická validace české verze Addenbrookského kognitivního testu (ACE-III-CZ) – pilotní studie
- Retrospektivní hodnocení a jednoleté sledování 58 pacientů podle etiologie defektu nervové trubice
- Vztah mezi objemem postresekčního rezidua a celkovým přežíváním pacientů s glioblastomem – studie v rámci jednoho neuroonkologického centra
- Poděkování recenzentům
- Začiatky mozgovej angiografie vo svete a v Československu
- Ischemie corpus callosum
- Standardizace využití MR v managementu roztroušené sklerózy. Konsenzus českého expertního radiologicko-neurologického panelu
- Zpráva o 36. českém a slovenském neurologickém sjezdu
- Zpráva ze světového neurochirurgického kongresu 2023
- Přehled difuzních gliomů dle klasifikace WHO 2021, 2. část – difuzní gliomy dětského typu
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Přehled difuzních gliomů dle klasifikace WHO 2021, 2. část – difuzní gliomy dětského typu
- Tonsilla cerebelli – anatomie, funkce a její význam pro neurochirurgii
- Standardizace využití MR v managementu roztroušené sklerózy. Konsenzus českého expertního radiologicko-neurologického panelu
- Adaptace a psychometrická validace české verze Addenbrookského kognitivního testu (ACE-III-CZ) – pilotní studie
