Nově vzniklý refrakterní status epilepticus a syndromy z blízkého spektra (NORSE/ FIRES)
New-onset refractory status epilepticus and considered spectrum disorders (NORSE/ FIRES)
New-onset refractory status epilepticus (NORSE) is defined as status epilepticus in a patient without active epilepsy or other preexisting relevant neurological disorder. It is characterized by refractory epileptic seizures, without a clear active structural, toxic, or metabolic cause. In most cases, the disease is preceded by mild febrile illness. Very frequently, the ethiology of NORSE can not be proven (cryptogenic NORSE). In a minority of cases is causal autoimmune encephalitis and viral infection of CNS. Conventional antiepileptic medications show very limited success. Therapy includes immunotherapy, ketogenic diet or another non pharmacological options. The long-term prognosis of patients is variable, in most cases cognitive impairments and epilepsy are present.
Key words:
new-onset refractory status epilepticus – clinical presentation – diagnostic protocol – therapy
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
:
K. Česká; O. Horák; H. Ošlejšková; Š. Aulická
:
Klinika dětské neurologie LF MU a FN Brno, Centrum vysoce specializované péče pro farmakorezistentní epilepsie MZ ČR, Brno
:
Cesk Slov Neurol N 2018; 81(6): 658-662
:
Review Article
prolekare.web.journal.doi_sk:
https://doi.org/10.14735/amcsnn2018658
Nově vzniklý refrakterní status epilepticus (new-onset refractory status epilepticus; NORSE) je definován jako status epilepticus, který se rozvinul u pacienta bez aktivní epilepsie nebo jiného neurologického onemocnění. Syndrom je charakterizován refrakterními epileptickými záchvaty bez prokazatelné aktivní strukturální, toxické nebo metabolické příčiny. Rozvoji onemocnění ve většině případů předchází mírné febrilní onemocnění. Velmi často se příčinu NORSE nepodaří prokázat (kryptogenní NORSE). Etiologicky se v menším procentu upatňují autoimunitní encefalitidy a virové infekce CNS. Standardní antiepiletická medikace nebývá efektivní. V léčbě se uplatňují imunoterapie, ketogenní dieta, resp. další nefarmakologické možnosti. Dlouhodobá prognóza pacientů je variabilní, ve většině případů je přítomno kognitivní postižení společně s epilepsií.
Klíčová slova:
nově vzniklý refrakterní status epilepticus – klinický obraz – diagnostický protokol – terapie
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Úvod
Nově vzniklý refrakterní status epilepticus (new-onset refractory status epilepticus; NORSE) je definován jako status epilepticus, který se rozvinul u pacienta bez aktivní epilepsie nebo jiného neurologického onemocnění. Syndrom je charakterizován refrakterními epileptickými záchvaty bez prokazatelné aktivní strukturální, toxické nebo metabolické příčiny. Typicky se NORSE prezentuje jako super-refrakterní status epilepticus, ale toto kritérium není podmínkou diagnózy [1 – 3]. Ve většině případů NORSE předchází mírné febrilní onemocnění [4].
Refrakterní epileptický status (refractory status epilepticus; RSE) je definován jako epileptický status, který nereaguje na podání antiepileptika 1. a 2. volby, a je nutno přistoupit k podání celkových anestetik. V případě, že jeho trvání je delší než 24 h, jedná se o super-RSE [4].
V souvislosti s nově vzniklým RSE se v literatuře setkáváme s řadou termínů, např. devastujíci epilepsie u dětí školního věku, de novo vzniklý kryptogenní refrakterní febrilní status epilepticus, akutní encefalitida s refrakterními repetitivními parciálními záchvaty (acute encephalitis with refractory repetitive partial seizures; AERRPS), horečkou indukovaná refrakterní epileptická encefalopatie, katastrofická idiopatická epileptická encefalopatie, těžký RSE na podkladě předpokladané encefalitidy. Všechny tyto pojmy se nyní slučují pod NORSE, což přispívá ke sjednocení managementu a včasné indikaci imunoterapie [1,5].
Etiologie a epidemiologické charakteristiky
Příčinu NORSE se asi v 60 % případů nepodaří prokázat – jedná se o tzv. kryptogenní NORSE. Z etiologicky objasněných případů převažují autoimunitní encefalitidy (paraneoplastické i neparaneoplastické), u nichž je NORSE součast fenotypu. Podle práce Gasparda et al se některá z autoimunitních encefalitid prokázala u 37 % pacientů ze sledované kohorty 130 nemocných [3]. V minoritní části případů se v etiologii uplatňují virové infekce CNS (herpes virus [HSV] 1, varicella zoster virus [VZV], cytomegalovirus [CMV], Epstein-Barr virus [EBV]). Klinický průběh je však bez ohledu na vyvolávající příčinu vždy obdobný. Proto se předpokládá, že se jedná o onemocnění na autoimunitním podkladě [3]. Tento fakt podporuje i studie z roku 2015, která prokazuje zvýšenou expresi interleukinu (IL) 6, C-X-C chemokinu 10 a IL-8 v likvoru u pacientů s AERRPS [1,6].
Demograficky má NORSE dva vrcholy výskytu. První je ve věku kolem 30 a následně pak kolem 65 let [3,7]. Procentuálně převládají ženy (poměr přibližně 2 : 1) [7]. U mladších dětí (dle literatury a našich zkušeností se jedná o pacienty ve věku 2 – 4 let) existuje specifický syndrom IHH +/ – E (infantile hemiconvulsion-hemiplegia/ and epilepsy syndrome) – syndrom zahrnující hemikonvulze, hemiplegii s epilepsií nebo bez ní, který se může manifestovat také jako NORSE. Typické jsou stranově alternující motorické záchvaty a vysoká tělesná teplota při manifestaci RSE, který je následován tranzientní nebo permanentní hemiplegií. Několik měsíců po statu se může rozvinout farmakorezistentní epilepsie [8].
Podskupinou NORSE je tzv. epileptický syndrom asociovaný s febrilním onemocněním (febrile infection-related epilepsy syndrome; FIRES). Jedná se o zřídkavý, akutní, potenciálně fatální epileptický syndrom, kterému předchází febrilní infekt. Latence mezi febrilním infektem a manifestaci RSE je uváděna v rozmezí 24 h až 2 týdnů [2]. Postihuje děti ve věku 3 – 15 let s predominancí chlapců [2]. Obdobně jako NORSE se vyskytuje u pacientů bez předchozí anamnézy epilepsie a prezentuje se jako progresivní nástup záchvatů s přechodem do prolongovaného RSE. Incidence je extrémně nízká – např. dle prospektivní multicentrické studie v Německu 1 : 1 000 000 [9]. Rozvoji RSE v rámci FIRES předchází banální febrilní infekt (nejčastěji infekt horních dýchacích cest, gastroenteritida) u původně zdravých dětí. Záchvaty nereagují na běžnou antiepileptickou medikaci. Jsou přechodně přerušeny v barbiturátovém kómatu, ale při vyvádění z kómatu dochází velice často k relapsu záchvatů.
Průběh je dvoufázový. Pro první akutní fázi (1 – 12 týdnů) je typický náhlý rozvoj záchvatové aktivity, která rychle přechází do refrakterního status epilepticus. Typické jsou záchvaty fokální přecházející do bilaterálního tonicko-klonického záchvatu [9]. Následuje druhá chronická fáze, pro niž je charakteristická farmakorezistentní epilepsie, nezřídka s periodickým výskytem záchvatů v kumulacích [10]. Nemoc ovlivňuje kognitivní funkce a způsobuje také poruchy paměti a řeči, a/ nebo dysfunkce frontální laloku.
Patofyziologie
Toho času není znám jasný mechanizmus, který by mohl vysvětlit podstatu rozvoje kryptogenního NORSE a FIRES. U FIRES byla prokázána intratékální nadprodukce prozánětlivých cytokinů a chemokinů. Některé z nich mají prokonvulzivní efekt. Není však jasné, zda intratékální zánět je příčinou nebo důsledkem RSE. Dosud nebyly provedeny srovnávací testy FIRES a refrakterního statu bez zánětu v úvodu. Svoji roli může v patofyziologii onemocnění hrát také individuální predispozice jedince daná variací v podtypech humánního leukocytárního antigenu, jako je tomu u jiných, postinfekčních neurologických onemocnění [1].
Klinické charakteristiky NORSE
Podle práce Gasparda et al jsou prodromální symptomy pozorovány u 60 % pacientů. Jejich počátek je zaznamenán 1 – 14 dnů před rozvojem onemocnění. Většinou se jedná o zmatenost (45 %), zvýšenou tělesnou teplotu (34 %). Bolesti hlavy a únava se objevují přibližně u 20 % pacientů. Změny chování, gastrointestinální symptomy a infekce horních cest dýchacích se vyskytují přibližně u 15 % pacientů. Halucinace se vyskytují asi u 25 % pacientů [3].
Nejčastějším typem záchvatů jsou generalizované tonicko-klonické paroxysmy (přibližně u 60 – 70 % pacientů). V menším procentu pak záchvaty fokální s poruchou vědomí nebo bez ní. V úvodu onemocnění jsou záchvaty většinou intermitentní, v dalším průběhu se zvyšující se frekvencí a tendencí ke kombinaci jednotlivých typů záchvatů. Status absencí nebyl dosud popsán [3].
Doporučený diagnostický manuál podle NORSE Institute
V roce 2017 byl organizací pod názvem NORSE Institute (kolokvium lékařů z 8 zemí světa) vypracován doporučený extenzivní diagnostický manuál pro pacienty s RSE. Podrobnější seznam vyšetření, který bude společností pravidelně aktualizován, je dostupný na internetové adrese: www.norseinstitute.org [8].
- Anamnéza – s důrazem na imunosupresi, medikaci, epidemiologickou anamnézu, kontakt se zvířaty, drogy, toxiny;
- MR mozku s kontrastní látkou, MRA a venografie;
- kontinuální EEG monitorace [8].
Další doporučená vyšetření podle možné etiologie onemocnění [8]
- Infekční etiologie – krevní obraz, diferenciální krevní obraz, biochemie vč. C-reaktivního proteinu (CRP) a prokalcitoninu, hemokultura. Ze séra a likvoru – imunoglobuliny G a M, Chlamydia pneumoniae, Bartonella henselae, Mycoplasma pneumonia, Coxiella burnetii, Shigella species a Chlamydia psittaci. Výtěr z nosu a krku – respirační virové patogeny (polymerázová řetězová reakce [polymerase chain reaction; PCR]). Likvor – cytologie, protein, glukóza, příp. přítomnost infekčního patogenu – PCR HSV1, HSV2, VZV, EBV, HIV, CMV, lidský herpes virus 6, enteroviry, virus chřipky A/ B, parvovirus. Další testy dle geografické polohy a epidemiologické anamnézy.
- Autoimunitní/ paraneoplastická etiologie – sérum a likvor – protilátky proti leucin-rich glioma inactivated proteinu 1, protilátky proti contactin-associated proteinu 2, protilátky proti glutamát dekarboxyláze, protilátkami proti glutamátovým N-metyl-D-aspartátovým receptorům, protilátky proti glutamátovému receptoru α-amino-3-hydroxy-5-metyl 4-izoxazoleproprionát, receptor pro kyselinu γ-aminomáselnou typu B/ A (γ-amino-butyrát; GABA-B, GABA-A), glycínový receptor, amfifyzin, colapsin response mediator protein 5, neurexin-3alpha, adenylat kináza, protilátky anti-Hu, protilátky anti-Yo a protilátky anti-Ri. Sérum – antinukleární protilátky, protilátky proti cytoplazmě neurofilů, protilátky proti štítné žláze, protilátky proti DNA (anti-dsDNA), CRP, protilátky proti extrahovatelným nukleárním antigenům, antityreoglobulin, protilátky proti endomysiu, chladové a tepelné aglutiníny.
- Neoplazie – CT resp. MR hrudníku/ břicha/ pánve, UZ varlat, mamogram, cytologie likvoru, flow cytometrie likvoru.
- Metabolická etiologie – hodnota laktátdehydrogenázy, jaterní funkce, elektrolyty, amoniak, skríning porfýrie. Hladiny vitaminů B1, B12, foláty, laktát, pyruvát, troponin; testy pro případné mitochondriální onemocnění – svalová biopsie a MR spektroskopie.
- Toxikologická etiologie – benzodiazepiny, amfetaminy, kokain, fentanyl, alkohol, těžké kovy, extáze, syntetické kanabinoidy.
- Genetická etiologie – spolupráce s genetikem. Zvážit – myoklonická epilepsie s potrhanými červenými svalovými vlákny, syndrom mitochondriální encefalomyopatie, laktátové acidózy a „stroke-like“ epizod, mitochondriální DNK polymeráza gama, skríning kyselin s velmi douhým řetězcem. Zvážit také 24h sběr moči na hodnotu mědi a vyšetření ceruloplazminu.
Návod není dogmatický a dle našich klinických zkušeností jsou některá z doporučených testů NORSE Institutem v akutní fázi onemocnění diskutabilní a není možné je v podmínkách menších nemocnic provést. Také jejich interpretace v akutní fázi nemusí být vždy jednoznačná a pro diagnosticko-terapeutický proces přínosná.
Přikládáme diagnostický manuál osvědčený na našem pracovišti. Máme za to, že cílem diagnostického postupu je nejen pokus o objasnění etiologie, ale především odhalení případné kontraindikace včasné imunoterapie. Základem je podrobná anamnéza, neurologické vyšetření, EEG/ video EEG monitorace, MR mozku s kontrastní látkou, MRA a venografie. Další vyšetření jsou vypsána v tab. 1.

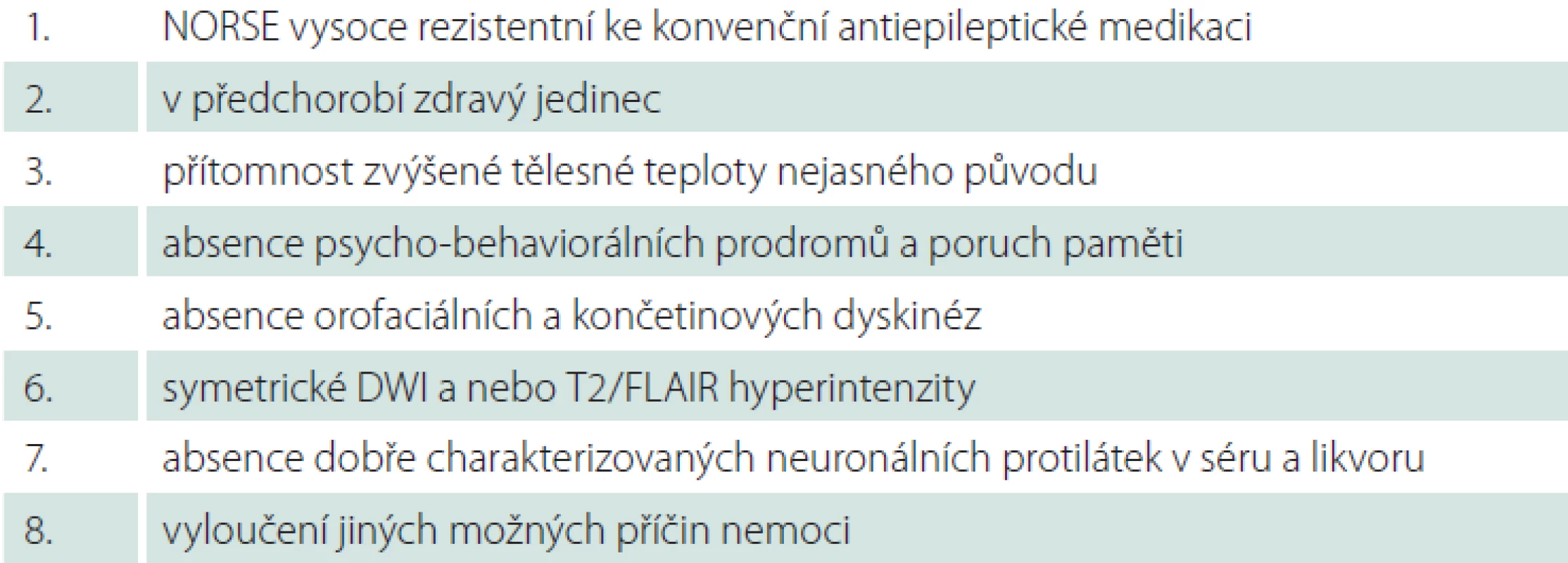
Jako pomocný diagnostický nástroj k odlišení kryptogenního NORSE může sloužit tzv. kryptogenní-NORSE (cryptogenic-NORSE; C-NORSE) skóre (0 – 6 bodů), které je založeno na klinických charakteristikách – tab. 2. První dva body jsou podmínkou diagnózy. Etiologie NORSE je pravděpodobně kryptogenní, když pacient splňuje nejméně 5 z prvních 6 bodů [5].
Terapie NORSE
V léčbě NORSE je standardní antiepileptická medikace většinou neúspěšná. Také použití celkových anestetik, vč. barbiturátů nepřináší ve většině případů (po jejich vysazení či snížení dávkování) terapeutický úspěch. Jako další terapeutická možnost se používá imunoterapie. Podmínky jejího nasazení, resp. načasování, délka terapie a dávkování však nejsou standardizovány. Obecně se autoři shodují, že nejdůležitější je její včasné zahájení (doporučováno do 10. dne od vzniku statu). To vede ke snížení nemocniční mortality a morbidity a také k příznivější dlouhodobé prognóze [3,4,12].
Jako imunoterapie první volby se doporučuje použití steroidů (pulzní dávkování metylprednizolonu), intravenózních imunoglobulinů nebo plazmaferéza. V imunoterapii druhé linie pak takrolimus, rituximab, cyklofosfamid. O efektivitě a bezpečnosti terapie 2. linie je nedostatek dostupných informací. Proto oficiální doporučení dávkování neexistuje. V tab. 3 přikládáme léčebné schéma používané na našem pracovišti. Dávkování prvoliniové imunoterapie je identické s oficiálním doporučením NORSE Institute. V tab. 3 uvádíme také používané dávkování u druholiniové terapie. Součastí tabulky jsou též údaje o efektivitě jednotlivých imunoterapeutických možností podle NORSE Institute. Slibnou terapeutickou možností je anakinra (neglykolyzovaný lidský antagonista receptoru pro IL-1; IL-1Ra). Její použítí bylo publikováno v několika kazuistických sděleních, a zkušenosti jsou tudíž omezené [1,8].

V rámci nefarmakologické léčby v efektivitě dominuje jednoznačně ketogenní dieta. U FIRES je efektivní v 50 % a u NORSE asi u 60 % [1,2,12]. Ve srovnání s jinými nefarmakologickými možnostmi léčby je ketogenní dieta v akutní fázi onemocnění také nejdostupnější možnost. Její použití na základě našich klinických zkušeností u RSE jednoznačně doporučujeme. Z dalších nefarmakologických terapeutických strategií byly použity řízená hypotermie, hluboká mozková stimulace, implantace vagového stimulátoru a operační řešení (např. kalosotomie). Ve všech pracích se ale jedná o pozorování na malém počtu pacientů [1,4].
Komplikace a dlouhodobý outcome pacientů s NORSE
Dlouhodobý zdravotní stav po překonání NORSE je variabilní. Ve většině případů je u pacientů přítomno kognitivní postižení společně s epilepsií. Chronická encefalopatie se vyskytuje u 29 – 83 % pacientů. Mortalita se u NORSE pohybuje kolem 30 %. Rizikovými faktory pro horší průběh nemoci jsou nižší věk pacienta a potřebná délka terapeutického komatu s burst-suppression vzorcem v EEG (medián délky umělé plicní ventilace je podle práce Kantanena et al u RSE 6 – 11 dní, u pacientů s horší prognózou je časové rozmezí větší než u pacientů s příznivým outcomem) [10,13]. Prognóza FIRES je nepříznivá s těžkými neurologickými následky. Mortalita je přítomna u 1/ 5 pacientů [2].
Závěr
Etiologie epileptického statu se ve většině připadů diagnostikuje standardizovaným protokolem (podrobná anamnéza, hematologické a biochemické testy krve, toxikologické vyšetření, strukturální zobrazení mozku a EEG). Přibližně u 20 % statů se příčina tímto základním diagnostickým protokolem neobjasní. Časné nalezení kauzality má dopad na terapeutický postup a prognózu pacienta [1].
Přesný diagnostický a terapeutický manuál v případě NORSE a FIRES prozatím neexistuje. NORSE Institute definuje extenzivní vyšetření, která mají sloužit jako doporučení [1,8].
V terapii selhávají standardní postupy léčby statu konvenčními antiepileptiky. Proto se přistupuje k časnému zahájení imunoterapie (prvoliniová – steroidy, intravenózní imunoglobuliny a plazmaferéza; a druholioniová – cyklofosfamid, rituximab), resp. nefarmakologické léčby – ketogenní dieta (především v případě FIRES), hypotermie, epileptochirurgie. Slibnou léčebnou možností je anakinra [1,5]. FIRES i NORSE jsou jednotky asociované s vysokou morbiditou a mortalitou.
Podpořeno z fondů LF MU – juniorský výzkumník MU Dr. Štefánia Aulická, Ph.D.
Přijato k recenzi: 25. 8. 2018
Přijato do tisku: 30. 10. 2018
MUDr. Štefánia Aulická, Ph.D.
Klinika dětské neurologie LF MU a FN Brno
Centrum pro epilepsie Brno
Černopolní 9
613 00 Brno
Sources
1. Gaspard N, Hirsch LJ, Sculier C et al. New-onset refractory status epilepticus (NORSE) and febrile infection-related epilepsy syndrome (FIRES): state of the art and perspectives. Epilepsia 2018; 59(4): 1 – 8. doi: 10.1111/ epi.14022.
2. Marashly A, Lew S, Koop J. Successful surgical management of new onset refractory status epilepticus (NORSE) presenting with gelastic seizure in a 3 year old girl. Epilepsy Behav Case Rep 2017; 8 : 18 – 26. doi: 10.1016/ j.ebcr.2017.05.002.
3. Gaspard N, Brandon PF, Alvarez V et al. New-onset refractory status epilepticus. Etiology, clinical features, and outcome. Neurology 2015; 85(18): 1604 – 1613. doi: 10.1212/ WNL.0000000000001940.
4. Gal CRE, Jumma O, Mohanraj R. Five cases of new onset refractory status epilepticus (NORSE) syndrome: Outcome with early immunotherapy. Seizure 2013; 22(3): 217 – 220. doi: 10.1016/ j.seizure.2012.12.016.
5. Marečková I, Vojtěch Z, Procházka T et al. Případ de novo vzniklého super-refrakterního epileptického statu. Neurol Praxi 2015; 16(6): 366 – 369.
6. Lizuka T, Kanazawa N, Kaneko J et al. Cryptogenic NORSE. Its distinctive clinical features and response to immunotherapy. Neurol Neuroimmunol Neuroinflamm 2017; 4(6): e396. doi: 10.1212/ NXI.0000000000000396.
7. Wilder-Smith EP, Lim EC, Teoh HL et al. The NORSE (new-onset refractory status epilepticus) syndrome: defining a disease entity. Ann Acad Med Singapore 2005; 34(7): 417 – 420.
8. NORSE Institute. Norse diagnostic checklist. [online]. Available from URL: https:/ / static1.squarespace.com/ static/ 56433eade4b0b66656c0301c/ t/ 58b5dfa36b8f5b9a4 2283592/ 1488314276155/ Annotated+NORSE+Diagnostic+Checklist+pdf.pdf .
9. van Baalen A, Hausler M, Plecko-Startinig B et al. Febrile infection-related epilepsy syndrome without derectable autoantibodies and response to immunotherapy: a case series and discussion of epileptogenesis in FIRES. Neuropediatrics 2012; 43(4): 209 – 216. doi: 10.1055/ s-0032-1323848.
10. Fox K, Wells ME, Tennison M et al. Febrile infection-related epilepsy syndrome (FIRES): a literature review and case study. Neuroradiogn J 2017; 57(3): 224 – 233. doi: 10.1080/ 21646821.2017.1355181.
11. Aulická Š, Aulický P, Česká K et al. Management konvulzivního status epilepticus v dětském věku. Anesteziol Intenziv Med. In press 2018.
12. Li J, Saldivar Ch, Maganti RK. Plasma exchange in cryptogenic new onset refractory status epilepticus. Seizure 2013; 22(1): 70 – 73. doi: 10.1016/ j.seizure.2012.09.011.
13. Kantanen AM, Reinikainen M, Parvianen I et al. Long-term outcome of refractory status epilepticus in adults: a retrospectice population – based study. Epilepsy Research 2017; 133 : 13 – 21. doi: 10.1016/ j.eplepsyres.2017.03.009.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2018 Issue 6
-
All articles in this issue
- Diagnostics, symptomatology and findings in diseases and disorders of the autonomic nervous system in neurology
- Patients with extensive early changes (ASPECTS < 5) – recanalization YES
- Patients with extensive early changes (ASPECTS < 5) – recanalization NO
-
Pacient s rozsiahlymi skorými zmenami (ASPECTS < 5) – rekanalizácia
Komentár ku kontroverziám - Pragnancy and multiple sclerosis from a neurologist’s point of view
- Quality of life of caregivers of patients with progressive neurological disease
- New-onset refractory status epilepticus and considered spectrum disorders (NORSE/ FIRES)
- The efficacy of cochlear implantation in adult patients with profound hearing loss
- Clinical results of cervical discectomy and fusion with anchored cage – prospective study with a 24-month follow-up
- A comparison of mini-invasive percutaneous versus classic open pedicle screw fixation of thoracolumbar fractures – retrospective analysis
- Dural reconstruction with usage of xenogenic biomaterial
- Meningococcal meningitis with Chiari malformation (type I)
- Comment to the article N. Dahmardeh et al. Fingolimod attenuates harmaline-induced passive avoidance memory and motor impairments in a rat model of essential tremor
- Evaluation of systolic and diastolic cardiac functions and heart rate variability in patients with juvenile myoclonic epilepsy
- Reconstruction of the anterior skull base with free muscle flap after iatrogenic injury
- A Bulgarian family with epileptic seizures as a first manifestation of familial cerebral cavernous malformations
- Solitary cerebellar metastasis of uterine cervical carcinoma
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Diagnostics, symptomatology and findings in diseases and disorders of the autonomic nervous system in neurology
- New-onset refractory status epilepticus and considered spectrum disorders (NORSE/ FIRES)
- Clinical results of cervical discectomy and fusion with anchored cage – prospective study with a 24-month follow-up
- Pragnancy and multiple sclerosis from a neurologist’s point of view
