Míšní metastáza adenokarcinomu – kazuistika
Spinal Cord Metastasis of Adenocarcinoma – Case Report
Metastasis of adenocarcinoma to the spinal cord is a rare condition that accounts for 1–3 % of spinal tumours. The authors present the case of a 74-year-old man who suddenly developed quadriparesis and was subsequently diagnosed as a tumour of the cervical spinal cord. The spinal tumour was removed surgically and a metastasis of an adenocarcinoma was shown histologically, probably from the sigmoid colon. Early diagnosis of spinal metastases by means of magnetic resonance and microsurgical resection can improve prognosis and neurological deficit of patients to some extent. The available literature presents a total of 71 cases of surgery, which is recommended in selected cases, in particular for patients with a potentially radio-resistant metastasis. The aim of surgery is the decompression of functional nerve tissue and histological verification of the origin of the tumour. Survival time after such an operation is approximately twice that when therapy does not involve surgery.
Key words:
spinal cord metastasis – adenocarcinoma – spinal cord – operation
Autoři:
L. Hrabálek 1; O. Kalita 1; J. Ehrmann 2; J. Srovnal 2; M. Hajdúch 3
Působiště autorů:
Neurochirurgická klinika LF UP a FN Olomouc
1; Katedra patologie, Centrum molekulární biologie a medicíny LF UP a FN Olomouc
2; Laboratoř experimentální medicíny, Dětská klinika LF UP a FN Olomouc
3
Vyšlo v časopise:
Cesk Slov Neurol N 2008; 71/104(5): 583-587
Kategorie:
Kazuistika
Poděkování: Molekulární vyšetření nádoru bylo umožněno díky grantové podpoře Ministerstva školství, mládeže a tělovýchovy (LC07017, MSM 6198959216) a Ministerstva průmyslu (MPO 1H-PK/45) České republiky.
Souhrn
Metastázy adenokarcinomu do míchy jsou vzácné a tvoří jen 1–3 % všech nádorů míchy. Autoři prezentují případ 74letého muže s náhle vzniklou kvadruparézou a následně diagnostikovaným tumorem krční míchy. Míšní expanze byla radikálně chirurgicky odstraněna a histologicky byla prokázána metastáza adenokarcinomu, pravděpodobně z colon sigmoideum. Časná diagnostika míšních metastáz pomocí magnetické rezonance a mikrochirurgická technika resekce mohou částečně zlepšit prognózu a neurologický deficit pacientů. V dostupné literatuře je prezentováno celkem 71 případů chirurgické léčby, ta je doporučena ve vybraných případech, a to zvláště u pacientů s potenciálně radiorezistentní metastázou. Cílem chirurgické léčby je dekomprese funkční nervové tkáně a histologické ověření původu nádoru. Doba přežití po operaci je přibližně dvojnásobná ve srovnání s neoperační terapií.
Klíčová slova:
míšní metastázy – adenokarcinom – mícha – operace
Úvod
Metastázy adenokarcinomu do míchy jsou vzácné. Projeví se klinicky jen u 0,1 až0,4 % pacientů s adenokarcinomem, tvoří jen 1–3 % všech nádorů míchy a asi 8,5 % metastáz celého centrálního nervového systému (CNS) [1–3]. Časná diagnostika míšních metastáz pomocí magnetické rezonance a mikrochirurgická technika resekce mohou částečně zlepšit prognózu a zmenšit neurologický deficit pacientů [3,4]. Cílem chirurgické resekce metastázy je dekomprese funkční tkáně míchy a histologické ověření nádoru. Autoři prezentují kazuistiku pacienta s operovanou krční míšní metastázou adenokarcinomu a s využitím dostupné literatury diskutují přínos operace pro pacienta. Běžně se pro označení míšní metastázy používá zkratka ISCM (Intramedullary Spinal Cord Metastasis).
Kazuistika
Muž ve věku 74 let, nekuřák, bez historie nádorového maligního onemocnění, udával krev ve stolici a váhový úbytek za posledních několik měsíců. Byl proto chystán ke kolonoskopickému vyšetření. Mezitím ale došlo náhle k rozvoji spastické kvadruparézy s prevalencí na pravostranných končetinách, především na pravé horní končetině s postižením svalů ramenního pletence a projevující se neschopností elevace končetiny v rameni. Obě dolní končetiny udržel v Mingazzinim, nebyl schopen chůze a byl popsán jednorázový únik stolice. Následně bylo provedeno akutní vyšetření magnetickou rezonancí (MRI) krční páteře s nálezem intramedulární expanze ve výši C4 s navazující syringomyelickou dutinou zasahující v kraniálním směru po medulla oblongata a v kaudálním směru po Th 4. Expanze byla v T2 a Stir sekvencích hyposignální a po aplikaci kontrastní látky se sytila nepravidelná periferní část formace. Velikost tumoru byla 24 × 12 mm se zřetelným ohraničením oproti zbytku míchy (obr. 1, 2). Pacient byl od začátku léčen kortikoidy (metylprednisolon) a neurologický stav se stabilizoval do té míry, že nedošlo k rozvoji plegie. Po dvou dnech od začátku příznaků bylo indikováno operační odstranění míšní expanze. Z levostranné hemilaminektomie C4, parciální hemilaminektomie C3 a C5 a ze středočárové myelotomie autoři kompletně odstranili zčásti prokrvácený, jinak hnědobéžový, křehký a relativně ohraničený míšní tumor. Druhý den po operaci kontrolní MRI s kontrastem potvrdila radikální odstranění a dekompresi míchy (obr. 3, 4). Operační rána se zhojila bez komplikací a neurologický stav pacienta se mírně upravil, zejména se zvětšil rozsah elevace pravé horní končetiny. Hybnost dolních končetin zůstala zachována beze změny a pacient byl nadále upoután na lůžko.
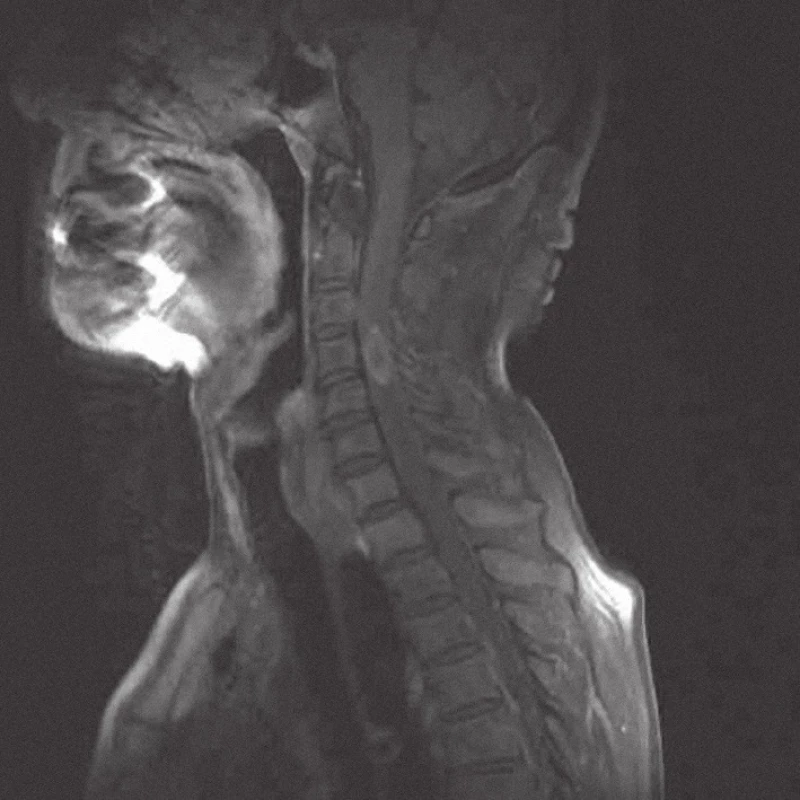
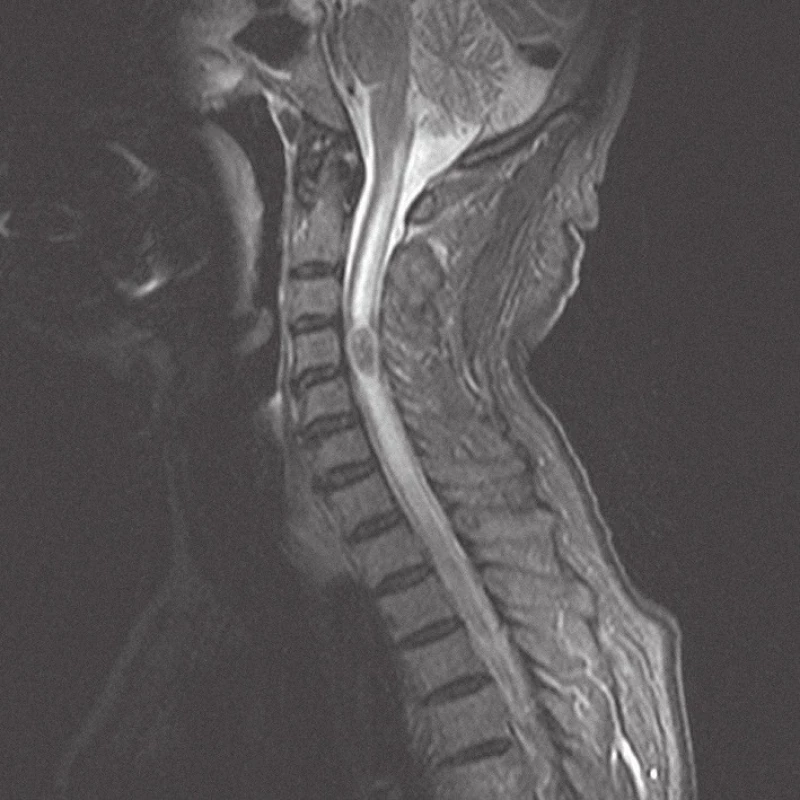
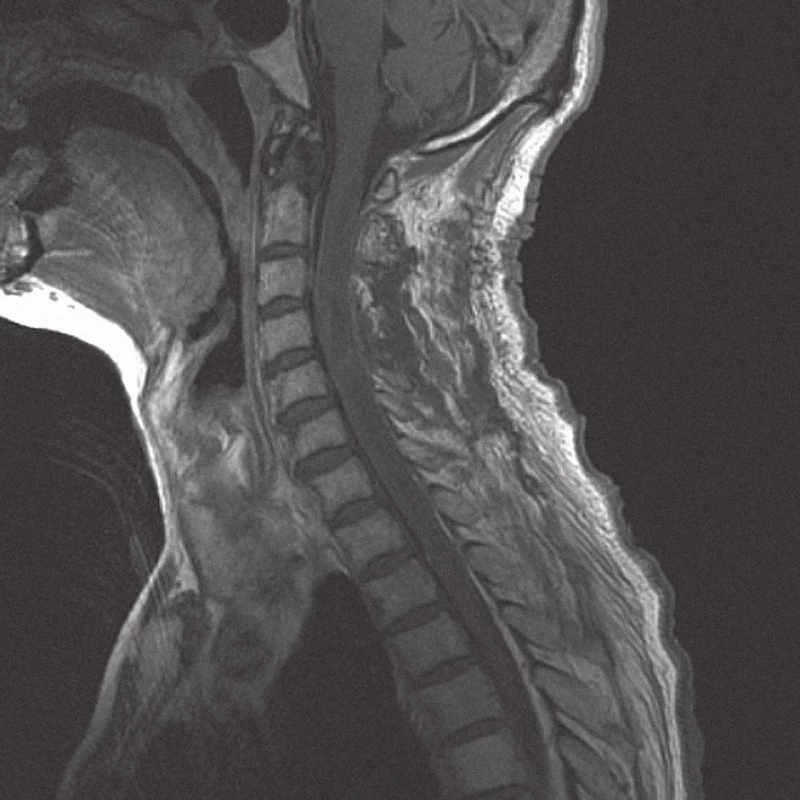
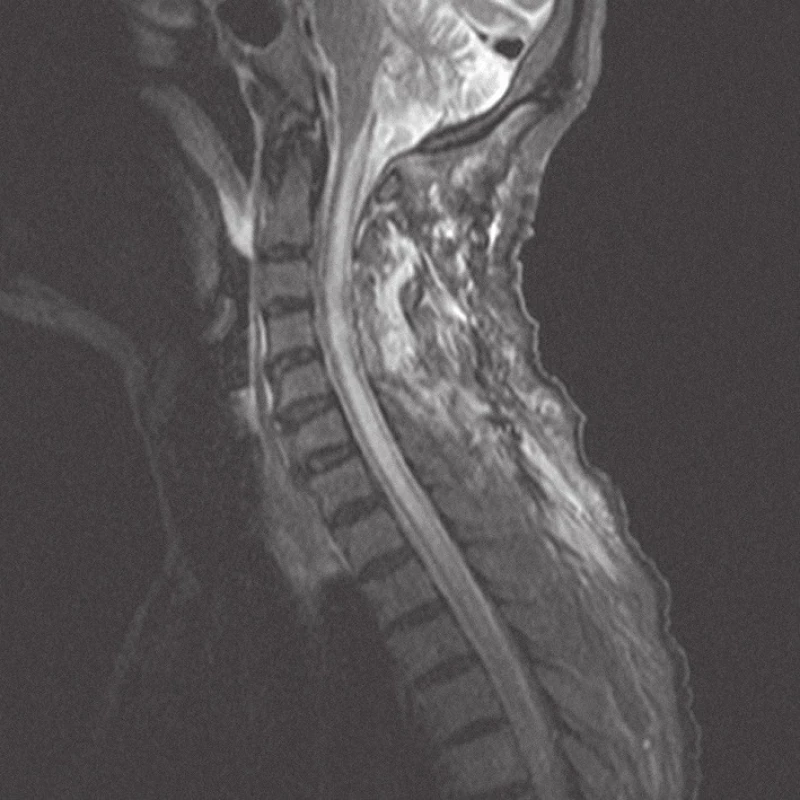
Během hospitalizace byla provedena celotělová PET/CT (pozitronová emisní tomografie/počítačová tomografie), která prokázala mnohočetná ložiska v plicích ve všech plicních polích, v paketu lymfatických uzlin paraesofageálně vpravo a v zesílené stěně colon sigmoideum v síle do 23 mm. Nález v sigmatu byl hodnocen jako pravděpodobný primární tumor a nálezy v lymfatických uzlinách a plicích jako metastázy. Následná kolonoskopie byla technicky obtížná pro nedostatečné vyprázdnění pacienta a tumor colon sigmoideum nemohla potvrdit. Vzhledem ke kachektizaci pacienta nebyla onkologem indikována žádná následná onkologická léčba ani další vyšetření. Pacient byl léčen pouze symptomaticky v zařízení následné péče a zemřel 11 týdnů po operaci, pitva provedena nebyla.
Výsledky tumor markerů
CEA: 4,54 (hodnota zvýšená u nekuřáků).
PSA: 0,75, PSA-volný: 0,19, fPSA/PSA poměr 25,30, CA 19–9: pod 2,5, AFP 2,13 (normální hodnoty).
Výsledek histologického a imunohistochemického vyšetření (obr. 5)
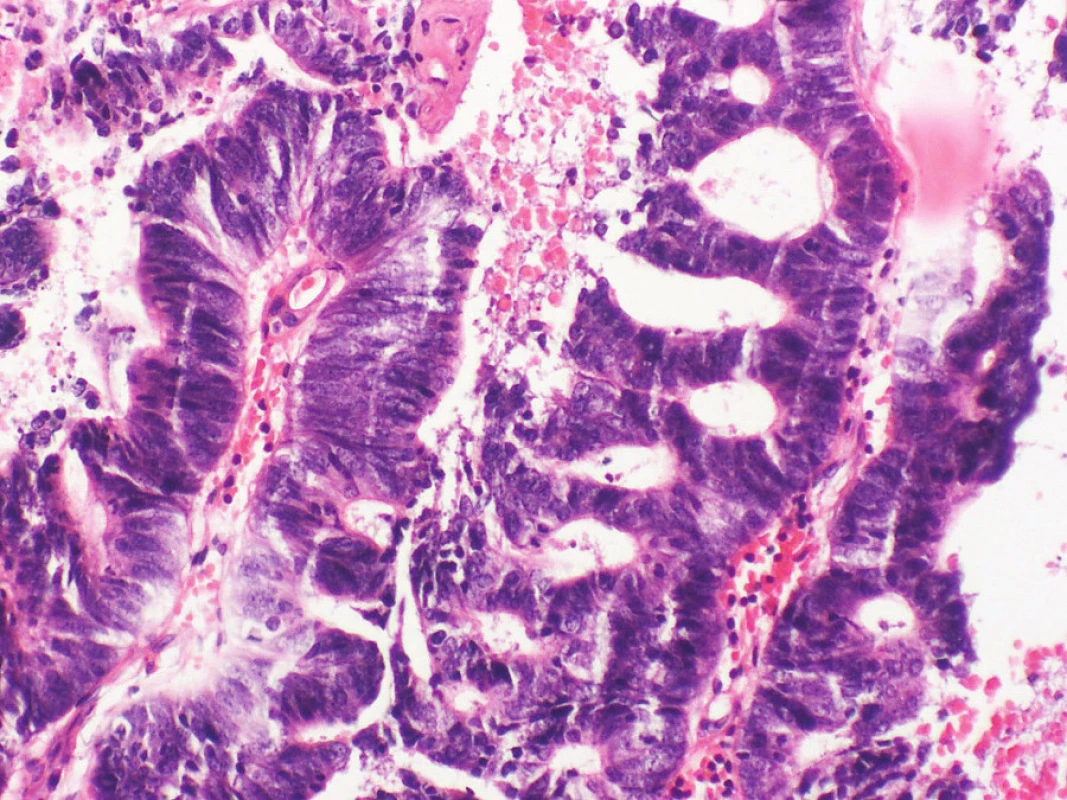
Adenokarcinom metastatický, vzhledem k negativitě CK7, CK20, TTF1 nelze blíže specifikovat orgánovou primaritu.
Výsledek cytogenetických a molekulárně genetických vyšetření
Ke všem vyšetřením byly využity nádorové buňky z parafinového preparátu. Vzhledem ke špatné kvalitě RNA z parafinového bloku nebyla analýza expresního profilu na úrovni mRNA na identifikaci nádorů neznámého primárního původu úspěšná. Z těchto důvodů, s ohledem na nekuřáctví pacienta a plicní ložiska, jsme se pokusili potvrdit/vyloučit plicní původ adenokarcinomu s použitím specifických znaků, aktivačních mutací EGFR1 genu a nepřítomnosti mutace genu KRAS, které se u části nekuřáků s plicní rakovinou vyskytují. Metodou polymerázové řetězové reakce (Polymerase Chain Reaction, PCR) byly testovány aktivující mutace v exonu 19 a 21 v genu EGFR a mutace exonu 1 v genu KRAS. Ve všech případech mutace nebyla nalezena a molekulární vyšetření v tomto případě rovněž nezpřesnilo klinickou diagnózu.
Diskuze
Zatímco metastázy do mozku nachází patolog asi v 20 % nádorových autopsií u pacientů s primární malignitou mimo nervový systém, ISCM jen ve 2 % [5,6]. Klinik diagnostikuje za života pacienta pouze 5 % těchto míšních metastáz [7].
Předpokládá se, že metastázy se do míchy dostanou arteriálním řečištěm a nikoliv venózní nebo lymfatickou cestou [8]. Diskrepance mezi frekvencí metastáz v mozku a v míše může být vysvětlena tak, že mozek přijme jednu třetinu srdečního výdeje přes velké cévy a pod velkým tlakem, zatímco mícha je cévně zásobená spíše z malých a klubkovitých cév pod malým tlakem [1,9]. Navíc medulární arterie odstupují z aorty v pravém úhlu, zatímco mozkové tepny jsou víceméně přímým pokračováním oblouku aorty, a to umožňuje snazší metastazování do mozku [10].
Nejčastějším zdrojem metastáz míchy je bronchogenní karcinom (tvoří 47 %), zejména malobuněčná forma [3,8,11]. Méně častým primárním tumorem metastazujícím do míchy je karcinom prsu, melanom, lymfom a Grawitzův tumor [8,11]. Extrémně vzácné jsou metastázy kolonorektálního adenokarcinomu, které tvoří jen 3 % [12].
Stanovení přesné diagnózy může být obtížné i tehdy, kdy je znám primární nádor, neboť nelze klinicky zcela jasně odlišit míšní metastázu od ostatních příčin myelopatie jako epidurální metastázy nebo paraneoplastické nekrotizující myelopatie [13]. Možnost míšní metastázy bychom měli spíše zvažovat u pacientů s historií maligního nádoru a současně v případech rozvoje hemiparézy nebo hemihypestezie. Právě asymetrie neurologické dysfunkce je typická pro míšní metastázu a Brown-Sequardův syndrom se vyskytuje u 30–34 % těchto pacientů [3,14,15]. Rychlá progrese symptomů zase odliší metastázu od pomaleji se rozvíjejícího primárního tumoru míchy. Ve všech těchto případech je tedy namístě urgentní vyšetření míchy magnetickou rezonancí.
Někteří autoři se domnívají, že radioterapie, chemoterapie ani chirurgická resekce nepřináší pacientovi žádný prospěch [5,16]. Tyto názory jsou ale ojedinělé. V léčbě míšních metastáz mnoho autorů preferuje jen radioterapii [1,8,17,18]. Je třeba ale zdůraznit, že pozitivní efekt radioterapie můžeme očekávat jen u radiosenzitivních metastáz, tedy u malobuněčného karcinomu plic, karcinomu prsu a lymfomu. Jak jsme se již zmínili, právě tyto tři typy nádorů metastazují do míchy nejčastěji. Chemoterapie nemá efekt na délku přežití pacientů ani na zmírnění neurologického deficitu [19], ačkoli některé studie uvádějí, že kombinace chemoterapie a radioterapie prodlužuje přežití pacientů [11,20]. Vzhledem k předpokládanému primárnímu zdroji ISCM v colon sigmoideum byly u našeho pacienta provedeny i testy na možnost použití biologické léčby. Na úrovni DNA jsme neprokázali přítomnost aktivačních mutací EGFR1 genu, často nacházených u plicního adenokarcinomu nekuřáků, což jej zcela nevylučuje, nicméně spíše podporuje kolorektální původ nádoru. S ohledem na nepřítomnost mutací genu KRAS měl pacient vysokou pravděpodobnost terapeutického benefitu z podání EGFR1 inhibitorů. Tato biologická léčba však již nebyla aplikována s ohledem na špatný výkonnostní stav pacienta a omezenou průchodnost monoklonálních protilátek do centrálního nervového systému.
Chirurgické odstranění metastázy míchy bývá indikováno stále častěji, a to zejména u pacientů s radiorezistentním primárním tumorem a při vyloučení leptomeningeální diseminace nádoru [12,21]. V dostupné literatuře je do začátku roku 2008 prezentováno celkem 71 případů chirurgické léčby [9,12,22–40]. Totální resekce byla preferována v 68 % (48 pacientů) a subtotální v 32 % (23 pacientů).
Zlepšení neurologického stavu po operaci nastalo v 56 % (40 pacientů), beze změny zůstal neurologický stav v 35 % (25 pacientů) a zhoršil se v 9 % (6 pacientů). Doba přežití je přibližně dvojnásobná ve srovnání s neoperační terapií. U pacientů konzervativně léčených je v průměru pět měsíců a chirurgicky řešených 9,4 měsíců [17,34].
Závěr
Ve vybraných případech ISCM je doporučeno radikální chirurgické odstranění, a to zvláště u pacientů s potenciálně radiorezistentní metastázou, jak tomu může být u metastázy adenokarcinomu tlustého střeva.
Cílem chirurgické léčby ISCM je dekomprese funkční nervové tkáně a histologické ověření původu nádoru.
MUDr. Lumír Hrabálek, Ph.D.
Neurochirurgická klinika LF UP a FN
I. P. Pavlova 6
775 20 Olomouc
e‑mail: lumir.hrabalek@seznam.cz
Přijato k recenzi: 16. 6. 2008
Přijato do tisku: 27. 8. 2008
Zdroje
1. Edelson RN, Deck MD, Posner JB. Intramedullary spinal cord metastases. Clinical and radiographic findings in nine cases. Neurology 1972; 22(12): 1222–1231.
2. Jellinger K, Kothbauer P, Sunder-Plassmann E, Weiss R. Intramedullary spinal cord metastases. J Neurol 1979; 220(1): 31–41.
3. Schiff D, O’Neill BP. Intramedullary spinal cord metastases: clinical features and treatment outcome. Neurology 1996; 47(4): 906–912.
4. Schijns OE, Kurt E, Wessels P, Luijckx GJ, Beuls EA. Intramedullary spinal cord metastasis as a first manifestation of a renal cell carcinoma: report of a case and review of the literature. Clin Neurol Neurosurg 2000; 102:(4): 249–254.
5. Costigan DA, Winkelman MD. Intramedullary spinal cord metastasis. A clinicopathological study of 13 cases. J Neurosurg 1985; 62(2): 227–233.
6. Chason JL, Walker FB, Landers JW. Metastatic carcinoma in the central nervous system and dorsal root ganglia. Cancer 1963; 16 : 781–787.
7. Okamoto H, Shinkai T, Matsuno Y, Saijo N.Intradural parenchymal involvement in the spinal subarachnoid space associated with primary lung cancer. Cancer 1993; 72(9): 2583–2588.
8. Grem JL, Burgess J, Trump DL. Clinical features and natural history of intramedullary spinal cord metastasis. Cancer 1985; 56(9): 2305–2314.
9. Silva YJ, McSwain B. Intramedullary spinal cord metastasis: the sole clinical manifestation of an adenocarcinoma of the colon. Can J Surg 1967; 10(3): 341–344.
10. Tanghetti B, Fumagalli GL, Giunta F, Marini G, Zorzi F. Intramedullary spinal cord metastases. J Neurosurg Sci 1983; 27(2): 117–124.
11. Connolly ES jr, Winfree CJ, McCormick PC, Cruz M, Stein BM. Intramedullary spinal cord metastasis: report of three cases and review of the literature. Surg Neurol 1996; 46(4): 329–338.
12. Ogino M, Ueda R, Nakatsukasa M, Murase I. Successful removal of solitary intramedullary spinal cord metastasis from colon cancer. Clin Neurol Neurosurg 2002; 104(2): 152–156.
13. Chen YJ, Chang GCh, Chen HT, Yang TY, Kuo BIT, Hsu HCh et al. Surgical results of metastatic spinal cord compression secondary to non‑small cell lung cancer. Spine 2007; 32(15): E413–E418.
14. Dunne JW, Harper CG, Pamphlett R. Intramedullary spinal cord metastases: a clinical and pathological study of nine cases. Q J Med 1986; 61(235): 1003–1020.
15. Guidetti B, Fortuna A. Differential diagnosis of intramedullary and extramedullary tumors. In: Vinken T, Braun G (eds). Handbook of Clinical Neurology. Amsterdam: Elsevier 1975 : 51–75.
16. Hejazi N, Hassler W. Microsurgical treatment of intramedullary spinal cord tumors. Neurol Med Chir (Tokyo) 1998; 38(5): 266–271.
17. Lee SS, Kim MK, Sym SJ, Kim SW, Kim WK, Kim SB et al. Intramedullary spinal cord metastases: a single‑institution experience. J Neurooncol 2007; 84(1): 85–89.
18. Winkelman MD, Adelstein DJ, Karlins NL. Intramedullary spinal cord metastasis. Diagnostic and therapeutic considerations. Arch Neurol 1987; 44(5): 526–531.
19. Holoye P, Libnoch J, Cox J, Kun L, Byhardt R,Almagro U et al. Spinal cord metastasis in small cell carcinoma of the lung. Int J Radiat Oncol Biol Phys 1984; 10(3): 349–356.
20. Potti A, Abdel-Raheem M, Levitt R, Schell DA, Mehdi SA. Intramedullary spinal cord metastases (ISCM) and non‑small cell lung carcinoma (NSCLC): clinical patterns, diagnosis and therapeutic considerations. Lung Cancer 2001; 31(2–3): 319–323.
21. Mut M, Schiff D, Shaffrey ME. Metastasis to nervous system: spinal epidural and intramedullary metastases. J Neurooncol 2005; 75(1): 43–56.
22. Amin R. Intramedullary spinal metastasis from carcinoma of the cervix. Br J Radiol 1999; 72(853): 89–91.
23. Bizzozzero L, Ferrara M, Villa F, Fontana R, Brusamolina R, Collice M. Intramedullary spinal cord metastasis. Case report. J Neurosurg Sci 1994; 38(3): 193–195.
24. de Almeida Holanda MM, de Andrade EM, da Silva JA. Intramedullary spinal cord metastasis from thyroid carcinoma: case report. Arq Neuropsiquiatr 2006; 64(2A): 338–341.
25. Donovan DJ, Freeman JH. Solitary intramedullary spinal cord tumor presenting as the initial manifestation of metastatic renal cell carcinoma: case report. Spine 2006; 31(14): E460–463.
26. Fakih M, Schiff D, Erlich R, Logan TF. Intramedullary spinal cord metastasis (ISCM) in renal cell carcinoma: a series of six cases. Ann Oncol 2001; 12(8): 1173–1177.
27. Fischer G, Brotchi J. Intramedullary spinal cord tumors. Report. French Society of Neurosurgery. 45th annual congress. Neurochirurgie 1994; 40 (Suppl 1): 1–108.
28. Foster OJ, Crockard HA. Cervical syrinx associated with an intramedullary metastasis: case report. J Neurol Neurosurg Psychiatry 1987; 50(5): 637–639.
29. Gasser TG, Pospiech J, Stolke D, Schwechheimer K. Spinal intramedullary metastases. Report of two cases and review of the literature. Neurosurg Rev 2001; 24(2–3): 88–92.
30. Gasser T, Sandalcioglu IE, El Hamalawi B,van de Nes JA, Stolke D, Wiedemayer H. Surgical treatment of intramedullary spinal cord metastases of systemic cancer: functional outcome and prognosis. J Neurooncol 2005; 73(2): 163–168.
31. Gazzeri R, Galarza M, Faiola A, Gazzeri G.Pure intramedullary spinal cord metastasis secondary to gastric cancer. Neurosurg Rev 2006; 29(2): 173–177.
32. Grasso G, Meli F, Patti R, Giambartino F, Florena AM, Iacopino DG. Intramedullary spinal cord tumor presenting as the initial manifestation of metastatic colon cancer: case report and review of the literature. Spinal Cord 2007; 45(12): 793–796.
33. Honma Y, Kawakita K, Nagao S. Intramedullary spinal cord and brain metastases from thyroid carcinoma detected 11 years after initial diagnosis – case report. Neurol Med Chir (Tokyo) 1996; 36(8): 593–597.
34. Kalayci M, Cağavi F, Gül S, Yenidünya S,Açikgöz B. Intramedullary spinal cord metastases: diagnosis and treatment – an illustrated review. Acta Neurochir (Wien) 2004; 146(12): 1347–1354.
35. Li Y, Takayasu M, Takagi T, Yoshimoto M,Mitsui Y, Yoshida J. Intramedullary spinal cord metastasis associated with hemorrage: a case report. No Shinkei Geka 2000; 28(5): 453–457.
36. Marquart C, Weckesser M, Schueller P,Hasselblatt M, Wassmann H, Schröder J. Intramedullary spinal cord metastasis as initial presentation of a systemic cancer – report of a rare case. Zentralbl Neurochir 2007; 68(4): 214–216.
37. Mercier P, Vialle M, George B, Fardoun R,Guy G. Les metastases rachidiennes intradurales des cancers viscéraux. A propos de quatre cas. Neurochirurgie 1984; 30(3): 177–181.
38. Pelissou-Guyotat I, Guyotat J, Szapiro J,Ravon R, Moreau JJ, Vidal J. Métastases spinales intradurales de néoplasies viscérales. A propos de quatre cas. Revue de la litterature. Neurochirurgie 1989; 35(4): 236–241.
39. Raco A, Delfini R, Salvami M, Innocenzi G,Ciappetta P. Intramedullary mestastasis of unknown origin: case report. Neurosurg Rev 1992; 15(2): 135–138.
40. Watanabe M, Nomura T, Toh E, Sato M,Mochida J. Intramedullary spinal cord metastasis: a clinical and imaging study of seven patients. J Spinal Disord Tech 2006; 19(1): 43–47.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2008 Číslo 5
-
Všechny články tohoto čísla
- Neurologické poruchy v rámci kritického stavu
- Matrixové metaloproteinázy v patogenezi roztroušené sklerózy
- Současná diagnostika a léčba oligodendrogliomů
- Význam monitorování mozkové aktivity pomocí integrované amplitudy EEG aktivity u novorozenců s časným asfyktickým syndromem
- Pravo/levorukost a preference druhostranné dolní končetiny. Testování laterality a mozečkové dominance
- Traumatické poranění mozku a zlomeniny obličejového skeletu
- Radiochirurgická léčba kraniofaryngeomů v kombinaci s ostatními stereotaktickými metodami
- Kombinované poranění atlasu a čepovce
- Míšní metastáza adenokarcinomu – kazuistika
- Neurosarkoidóza: zriedkavý prípad sarkoidózy krčnej miechy – kazuistika
-
Komentář k práci Mraček J. Intradurální výhřez bederní meziobratlové ploténky manifestující se syndromem kaudy – kazuistika
Věčné téma: výhřez meziobratlové ploténky, tentokrát intradurální - Intradurální výhřez bederní meziobratlové ploténky manifestující se syndromem kaudy – kazuistika
- Mozková gliomatóza – kazuistika
- Webové okénko
-
Analýza dat v neurologii XI.
Úvod do statistického usuzování – velikost účinku - Recenze
- Ne uromuskulární kongres v Brně
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Neurologické poruchy v rámci kritického stavu
- Intradurální výhřez bederní meziobratlové ploténky manifestující se syndromem kaudy – kazuistika
- Současná diagnostika a léčba oligodendrogliomů
- Traumatické poranění mozku a zlomeniny obličejového skeletu
