Náhrada defektu kalvy u dítěte po úrazu CNS biokompatibilním materiálem na míru – kazuistika
Closure of Calvarial Defect with Custom-made Biocompatible Implant in a Pediatric Patient – a Case Report
Severe head injuries in small children cause serious damage to the brain and bones of the cranium. Only small calvarial bone defects in children up to 1 year of age may heal spontaneously, as the rate of ossification slows down after the first year of life. If the affected area is too large or bone self-repair capacity limited, the patient must undergo cranioplasty. In this article, the authors discuss the issue of calvarial defect reconstruction in very young children. As no tissue bank for long-term storage of autologous bone graft is available in the authors’ institution, they decided to reconstruct posttraumatic calvarial bone defect in a child using customized implant manufactured of biocompatible material. The authors describe their experience with PEEK (polyetheretherketone) implant used in 18-month-old boy. At the present time, 17 months after the procedure, the boy is doing well and is without neurologic and cosmetic sequelae. His psychomotor development is adequate for his age. Following discharge from a hospital, the patient is in a long-term follow-up program in our outpatient clinic.
Key words:
skull defect – cranioplasty – customised implant – PEEK – polyetheretherketone
Autoři:
H. Homolková 1; M. Prchlík 2
Působiště autorů:
Klinika dětské chirurgie a traumatologie 3. LF UK a Thomayerova nemocnice, Praha
Oddělení dětské neurochirurgie
1; Klinika dětské chirurgie a traumatologie 3. LF UK a Thomayerova nemocnice, Praha
Jednotka intenzivní a resuscitační péče
2
Vyšlo v časopise:
Cesk Slov Neurol N 2012; 75/108(5): 617-620
Kategorie:
Kazuistika
Souhrn
Těžké úrazy hlavy u malých dětí působí závažná poranění mozku i kostí krania. Spontánní vyhojení kostního defektu je možné jen u malých ploch u dětí do jednoho roku věku. Osifikace totiž po prvním roce života klesá. Pokud je defekt příliš velký nebo osifikační potenciál malý, musí být defekt uzavřen kranioplastikou. Autoři předkládají složitost problematiky reparace defektů krania u velmi malých dětí. Protože na pracovišti autorů nelze uchovávat autologní štěpy k další reimplantaci, rozhodli se použít k uzavření poúrazového defektu krania u malého dítěte biokompatibilního implantátu vyrobeného na míru. V současné době je chlapec 17 měsíců po rekonstrukční operaci lbi, zcela bez neurologického postižení, bez kosmetických deformit a jeho psychomotorický vývoj odpovídá věku. Chlapec zůstává nadále dlouhodobě v našem sledování.
Klíčová slova:
kostní defekt – kranioplastika – implantát na míru – PEEK – polyéteréterketon
Úvod
Etiologie defektů kalvy u dětí je různá. Může se jednat o vrozené defekty, jako např. aplasia cutis, foramina parietalia, cleidokraniální dysplazie, nebo získané – trauma, pooperační infekce, tumor [1]. Spontánní vyhojení kostního defektu je možné jen u velmi malých ploch u malých dětí do jednoho roku věku. Osifikace totiž po prvním roce života klesá [2]. Osteogenetický potenciál krania je nepřímo úměrný věku [2–5]. Pokud je defekt příliš velký nebo osifikační potenciál malý, musí být defekt uzavřen kranioplastikou. Uzavření kostních defektů kalvy je vhodné nejenom z kosmetického, ale i z funkčního hlediska.
U starších dětí a dospělých lze užít vlastní kost z jiného místa kalvy, kostní ploténku vlastní, odstraněnou např. pro úraz, žebro, syntetický materiál, kostní náhražky, osteoinduktivní materiál.
U malých dětí je použití autologní kosti limitováno jejím nedostatkem. Metoda split bone není rovněž použitelná u dětí do čtyř let věku díky malé tloušťce diploického prostoru kosti a nemožnosti rozdělit kostní ploténku na vnitřní a vnější laminu. Diploický prostor se vytváří až po čtvrtém roce věku [5]. Získání extrakraniální autologní kosti zatěžuje dítě prodloužením ane-stezie, další operační ránou a je spojeno s prokazatelně vyšší morbiditou.
Autoři prezentují kazuistiku chlapce, jehož defekt lbi po dekompresní kraniektomii pro těžké kraniocerebrální poranění byl pro nedostatek vlastní kosti reparován biokompatibilním implantátem na míru. V diskuzi jsou rozebrány další možnosti reparace kostních defektů lbi v souladu s literaturou.
Kazuistika
Roční chlapec byl v lednu 2010 v kočárku zraněn tajícím sněhem a ledem, padajícími ze střechy domu. Ihned po úrazu byl chlapec v bezvědomí, GCS 3. Na místě byl zajištěn lékařem RZP a intubován. Byl přijat na JIRP s mnohočetnými a rozsáhlými zlomeninami kalvy, s kontuzemi mozku a posttraumatickým edémem. Ihned po příjmu bylo provedeno CT vyšetření s nálezem kontuzního ložiska vpravo parietálně až temporálně, další drobná kontuzní ložiska patrna bilaterálně parietálně až téměř na konvexitě mozku. Čerstvá krev byla patrna podél falxu a tentoria. Středové struktury bez jasného přetlaku, komorový systém bez dilatace a komprese, III. a IV. komora diferencovatelná. Četné fraktury neurokrania – fisura okcipitoparietálně vpravo i vlevo – vpravo částečně vícefragmentová. Rozestup fragmentů okcipitálně vpravo až 7 mm. Fraktura frontální kosti vpravo přecházela na strop očnice a její mediální i laterální stěnu.
Prvotní nález nebyl indikací k urgentní neurochirurgické intervenci (obr. 1, 2).

Pacient byl invazivně zajištěn včetně monitorování nitrolebního tlaku a jugulární oxymetrie. Od druhého dne byla monitorována mozková perfuze. Od 5. dne došlo k pozvolnému vzestupu nitrolebního tlaku až na hodnotu 25 mmHg, přičemž k poklesu nedošlo ani po podání masivní antiedematózní léčby. Možnosti konzervativní léčby byly vyčerpány, proto byla indikována neurochirurgická intervence – dekompresivní kraniektomie a ošetření kontuzně změněné mozkové tkáně (obr. 3).

V dalším průběhu byl pacient v dobrém klinickém stavu, neurologicky bez lateralizace hybnosti. V 46. den hospitalizace byl přeložen na plném enterálním příjmu, v dobrém sociálním kontaktu na oddělení dětské neurologie k rehabilitaci.
Uzávěr defektu krania byl původně plánován dva měsíce po překladu na neurologické oddělení. Pro opakované zánětlivé onemocnění ledvin a otitidu musel být zákrok vždy odložen. K uzávěru defektu krania nakonec došlo téměř šest měsíců po úrazu lbi. Vlastní kost odebranou během dekompresní kraniotomie nebylo možné použít, protože v našem zdravotnickém zařízení nelze uchovávat autologní kostní štěp k pozdější reimplantaci. Použít metodu split bone z kostní ploténky odebrané jinde na kalvě nebylo rovněž možné, tloušťka kalvy u našeho pacienta byla necelé 3 mm, diploický prostor se vytváří až po 4. roce věku.
Rozhodli jsme se použít biokompatibilní syntetický implantát na míru. Rozhodování, zda provést plastiku lbi vlastní kostí nebo implantátem a který implantát zvolit, je detailně rozebráno v diskuzi.
K vyhotovení přesného implantátu bylo nejprve nutno provést CT vyšetření, jednotlivé skeny po 1 mm. Následně je vytvořen 3D model lbi a podle tvaru a velikosti defektu je pak vyhotoven implantát přesně na míru. Vzhledem k četným odkladům kranioplastiky pro zánětlivá onemocnění jsme mohli přistoupit k operaci šest měsíců po úrazu. Implantát perfektně odpovídal tvaru defektu, museli jsme provést jen drobné korekce – snesení novotvořené nekvalitní kosti v apexu defektu. Implantát jsme k okolní kosti fixovali dlažkami a šroubky o délce 3 mm. Průběh operace i hospitalizace byl bez pozoruhodností. Nezaznamenali jsme žádné obtíže s hojením rány. V současné době je chlapec 17 měsíců po rekonstrukční operaci lbi, zcela bez neurologického postižení, psychomotorický vývoj odpovídá věku. Doposud neměl žádné pooperační komplikace. Implantát je fixován in situ v původní poloze, nedošlo k jeho dislokaci. Nezaznamenali jsme ani růstové deformity při přirozeném růstu lbi (obr. 4–6).

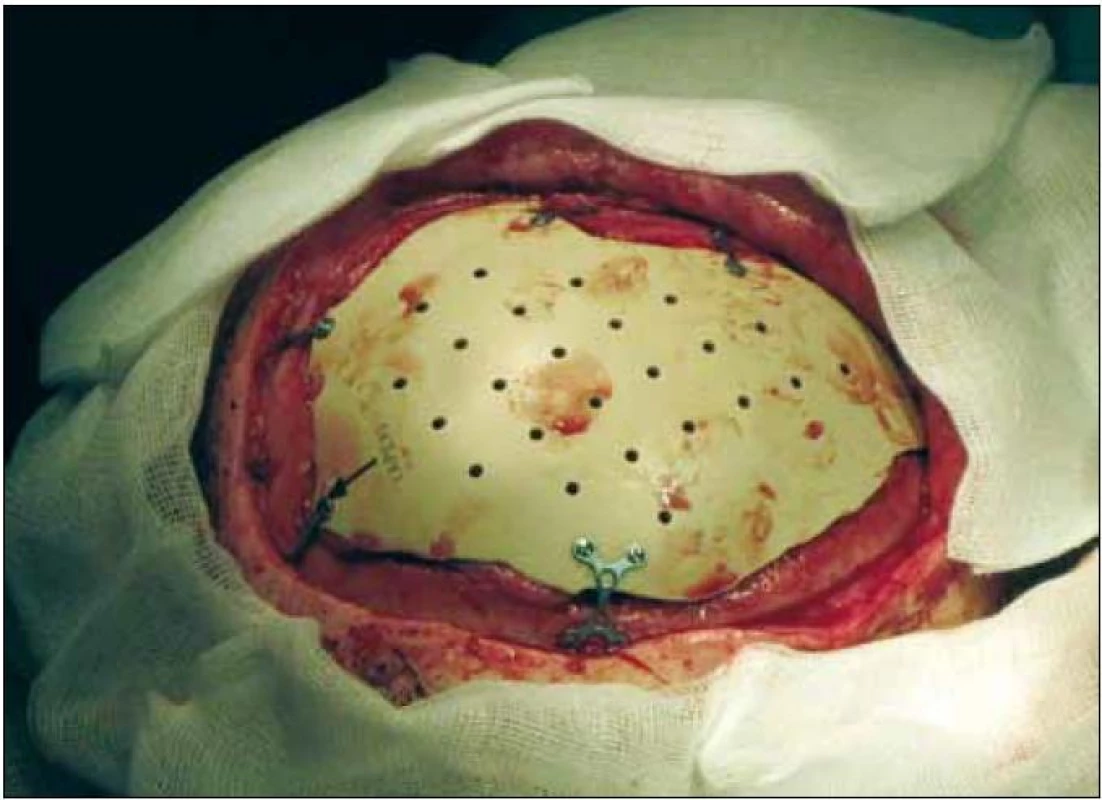

Diskuze
Cílem rekonstrukční operace lbi je dosažení dobrého estetického efektu a také obnovení krytu CNS.
Kranioplastika velkých defektů lebky vždy přináší určité problémy – kosmetické defekty, infekce, nepřihojení implantátu, uvolnění fixace a posunutí implantátu, epidurální efuze pod implantátem, resorpce vlastní kosti. Ani v literatuře neexistuje jednotná shoda v používaných metodách a materiálech. Oliveira et al (2007) [6] doporučují u velkých defektů kalvy použití biokeramických implantátů. Greene at al (2008) [1] na souboru 38 dětí ve věku od 3 do 20 let použili kostní drť vytěženou odvrtáváním nejčastěji parietální kosti. Tyto částečky pak navršili ve 3–4 mm silné vrstvě na tvrdou plenu a překryli tekutým tkáňovým lepidlem. Goh et al (2009) [7] doporučují užití na míru vyrobených metyl-metakrylátových implantátů a zároveň poukazují na četná selhání autologních štěpů, ať už z důvodu infekce nebo resorpce. Chao et al (2009) [8] se na souboru 11 pacientů přiklánějí k použití demineralizované kostní matrix vložené sendvičově mezi dvěma resorbovatelnými síťkami. Nicméně většina autorů se nakonec shoduje, že zlatým standardem je kranioplastika vlastní kostí [9].
Procento selhání štěpu z vlastní kosti koreluje s velikostí defektu. U defektů větších než 75 cm2 dochází k resorpci kostní ploténky až v 60 % případů.
U defektů menších než 75 cm2 je procento selhání štěpu minimální [10]. Zdravotnické zařízení musí mít možnosti zamražení kostní ploténky a její uchování lege artis až do doby implantace. V některých případech lze kostní ploténku uchovat v podkoží břicha. U malých dětí není tento postup vhodný z důvodu malé plochy stěny břišní, tenkého podkoží a malého množství podkožního tuku. Může dojít i k resorpci kosti.
Plastika defektu kalvy titanovými síťkami je vhodná u větších dětí. Při ní je třeba vymodelovat určitou strukturu, například část nadočnicového oblouku, a překrýt malý přiléhající defekt kalvy. I tak může působit estetické deformity při růstu krania, artefakty na CT i MR.
U velkých defektů kalvy, které zasahují několik růstovým zón, je nejvhodnější užití hydroxyapatitových kostních implantátů, zhotovených na míru. Hydroxyapatit se chová jako kostní materiál, dá se říci, že roste spolu s nositelem. Nevýhodou je vysoká cena, zatím není hrazen zdravotními pojišťovnami.
U našeho pacienta byla celková plocha kostního defektu cca 85 cm2, s maximem parietálně, a asi 1/3 defektu zasahovala temporookcipitálně.
Na našem pracovišti jsme doposud rutinně využívali metylmetakrylát, který jsme přizpůsobovali velikosti a tvaru defektu peroperačně. Referovaný pacient je naším nejmladším pacientem, jenž podstoupil dekompresivní kraniektomii pro úraz CNS. Použít na míru vyrobený implantát jsme se rozhodli kvůli věku pacienta a nepravidelnému tvaru defektu, který by se obtížně modeloval v průběhu operace na sále.
V tomto případě jsme zvolili použít biokompatibilní implantát vyrobený na míru, polyéteréterketon. Cena PEEK implantátu činí asi čtvrtinu ceny ve srovnání s hydroxyapatitem, lze vyžádat souhlas revizního lékaře a pak je implantát zcela hrazen zdravotní pojišťovnou.
PEEK polymer je semikrystalický plast odolávající vysokým teplotám, není toxický, je rezistentní na působení různých chemických látek [11]. Nepoškodí jej ani ionizační záření, je biologicky bezpečný a není cytotoxický [12]. Protože standardní tloušťka implantátu je od výrobce 4 mm, musela být tloušťka implantátu uzpůsobena tenké kosti našeho nemocného. Maximální ztenčení, při kterém výrobce nese garanci, je na 3 mm. Vlastní kost našeho nemocného měla sílu asi 2 mm. Milimetrový rozdíl v tloušťce kosti nepůsobil problémy. K fixaci jsme užili 3 mm dlouhé šrouby. Okraje vlastní kosti byly podloženy ztluštělou tkání tvrdé pleny a přerůstajícím periostem, hroty šroubů zůstaly v této tkání a nepůsobily dráždění zdravé tvrdé pleny. S růstem kalvy a jejím zesílením dojde k eliminaci kontaktu hrotu s měkkými tkáněmi. Deformit kalvy v důsledku růstu se neobáváme vzhledem k lokalizaci a velikosti defektu.
Závěr
Podle naší zkušenosti použití implantátu vyrobeného na míru významně zkracuje operační čas, umožňuje dokonale obnovit kraniální kontury, zamezit kosmetickým deformitám [13].
Neexistuje a ani nemůže existovat standard pro použití toho či onoho materiálu k léčbě kostních defektů kalvy u dětí. Každý nemocný musí být posuzován individuálně. Je nutno zvažovat velikost defektu, lokalizaci defektu, přesah defektu přes střední čáru, předchozí kranioplastiky nebo infekční komplikace a mnoho dalších faktorů, jako jsou věk, hmotnost, celkový klinický stav nemocného. V současné době je chlapec 17 měsíců po rekonstrukční operaci lbi, zcela bez neurologického postižení, psychomotorický vývoj odpovídá věku. Doposud neměl žádné pooperační komplikace. Implantát nepůsobí kosmetické deformity při růstu krania. Chlapec zůstává nadále v našem dlouhodobém sledování.
MUDr. Helena Homolková
Klinika dětské chirurgie a traumatologie
3. LF UK a Thomayerova nemocnice
Vídeňská 800
140 00 Praha 4
e-mail: helena.homolkova@ftn.cz
Přijato k recenzi: 30. 1. 2012
Přijato do tisku: 21. 2. 2012
Zdroje
1. Greene AK, Mulliken JB, Proctor MR, Rogers GF. Pediatric cranioplasty using particulate calvarial bone graft. Plast Reconstr Surg 2008; 122(2): 563–571.
2. Greenwald JA, Mehara BJ, Spector JA, Chin GS, Steinbrech DS, Saadeh PB et al. Biomolecular mechanisms of calvarial bone induction: immature versus mature dura mater. Plast Reconstr Surg 2000; 105(4): 1382–1392.
3. Cowan CM, Quatro N, Warren SM, Salim A, Longaker MT. Age-related changes in the biomolecular mechanisms of calvarilal osteoblast biology affect fibroblast growth factor-2 signaling and osteogenesis. J Biol Chem 2003; 278(34): 32005–32013.
4. Gosain AK, Santoro TD, Song LS, Capel CC, Sudhakar PV, Matloub HS. Osteogenesis in calvarial defects: contribution of the dura,the pericranium,and the sorrounding bone in adult versus infant animals. Plast Reconstr Surg 2003; 112(2): 515–527.
5. Koenig WJ, Donovan JM, Pensler JM. Cranial bone grafting in children. Plast Reconstr Surg 1995; 95(1): 1–4.
6. de Oliveira RS, Brigato R, Madureira JFG, Cruz AA, Mellho V, Filho FV et al. Reconstruction of a large complex skull defect in a child: a case report and literature review. Child Nerv Syst 2007; 23(10): 1097–1102.
7. Goh RC, Chang CN, Lin CL, Lo LJ. Customised fabricated implants after previous failed cranioplasty. J Plast Recontr Aesthetic Surg 2009; 63(9): 1479–1484.
8. Chao MT, Jiang S, Smith D, De Cesare GE, Cooper GM, Pollack IF et al. Demineralized bone matrix and resorbable mesh bilaminate cranioplasty: a novel method for reconstruction of large-scale defects in the pediatric calvaria. Plast Reconstr Surg 2009; 123(3): 976–982.
9. Brevi BC, Magri AS, Toma L, Sesenna E. Cranioplasty for repair of a large bone defect with autologous and homologous bone in children. J Ped Surg 2010; 45(4): E17–E20.
10. Grant GA, Jolley M, Ellenbogen RG, Roberts TS, Gruss JR, Loeser JD. Failure of autologous bone-assisted cranioplasty following decompressieve craniectomy in children and adolescents. J Neurosurg 2004; 100 (Suppl 2): 163–168.
11. Horák Z, Pokorný D, Fulín P, Šlouf M, Jahoda D, Sosna A. Polyetheretherketon (PEEK) – I. část: Perspektivní materiál pro ortopedickou a traumatologickou praxi. Acta Chir Ortop Traum Čech 2010; 77 : 463–469.
12. Pokorný D, Fulín P, Šlouf M, Jahoda D, Landor I, Sosna A. Polyetheretherketon (PEEK) – II. část: Poznatky o využití v klinické praxi. Acta Chir Ortop Traum Čech 2010; 77 : 470–478.
13. Josan VA, Sgouros S, Walsh AR, Dover MS, Nishikawa H, Hockley AD. Cranioplasty in children. Childs Nerv Syst 2005; 21(3): 200–204.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2012 Číslo 5
-
Všechny články tohoto čísla
- Vliv malých dávek vína či jiných alkoholických nápojů na lidské zdraví a délku života
- Emoční paměť – patofyziologie a klinické souvislosti
- Endovaskulární léčba intrakraniálních aneuryzmat – metodika, indikace, komplikace
- Validita a prediktivní hodnota skríningových testů u prediabetické a časné diabetické polyneuropatie
- Komentář k práci Š. Buršové et al
- Incidence a rizikové faktory pooperačního deliria
- Bezpečnost a účinnost intravenózní trombolytické terapie mozkového infarktu u pacientů nad 80 let věku
- Likvorový triplet (tau proteiny a beta-amyloid) v diagnostice Alzheimerovy-Fischerovy nemoci
- Zhoršení kognitivních funkcí a snížení perfuze v kontralaterálním frontálním laloku u pacientů s lézí mozečku
- Baha jako řešení jednostranné hluchoty po operaci vestibulárního schwannomu
- Sekvestrace MBNL1 proteinu mutovaným ZNF9 mRNA v lymfocytech pacientů s myotonickou dystrofií 2. typu
- Lze detekovat intrakraniální venózní reflux z transkondylárního přístupu? Výsledky studie s Fusion Imaging
- Náhrada defektu kalvy u dítěte po úrazu CNS biokompatibilním materiálem na míru – kazuistika
- Motorické stereotypie v dětském věku – kazuistiky
- Léčba spinálních paragangliomů – kazuistiky
- Amyotrofická laterální skleróza v zařízení paliativní hospicové péče – kazuistika
- Idiopatická stenóza akveduktu a porucha vývoje řeči u dětí s neurofibromatosis von Recklinghausen typ 1 – dvě kazuistiky
- Neurologické komplikace spojené s asistovanou reprodukcí – kazuistika
- Webové okénko
-
Analýza dat v neurologii
XXXV. Rozlišujme poměr šancí a relativní riziko -
8. olomoucké neuroimunologické sympozium s mezinárodní účastí
Olomouc, 20.–21. 9. 2012
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Motorické stereotypie v dětském věku – kazuistiky
- Emoční paměť – patofyziologie a klinické souvislosti
- Neurologické komplikace spojené s asistovanou reprodukcí – kazuistika
- Likvorový triplet (tau proteiny a beta-amyloid) v diagnostice Alzheimerovy-Fischerovy nemoci
