Liečba adrenokortikotropným hormónom u pacienta s epileptickou encefalopatiou spojenou s elektrickým status epilepticus v pomalom spánku – kazuistika
Landau - Kleffner Syndrome and Long‑term Adrenocorticotropic Hormone Therapy – a Case Report
The electrical status epilepticus in slow sleep (ESES) is characterised by specific EEG pattern of paroxysmal activity significantly activated during slow sleep. There are more clinical variants associated with an EEG pattern of ESES (for example Landau-Kleffner syndrome, continuous spike and wave syndrome – CSWS, benign childhood epilepsy with centro-temporal spikes, atypical benign partial epilepsy of childhood, myoclonic-astatic epilepsy). Therapy of ESES syndrome is not limited just to seizure control but it should be focused on controlling neuropsychological outcome through improved continuous epileptiform activity. Even though the epileptic seizures and the EEG pattern of ESES are age-related, many children have persisting cognitive and language disturbances. Early diagnosis and effective treatment are necessary for better outcome in these patients. In our case report we present the good effect of long-term adrenocorticotropic hormone therapy.
Key words:
electrical status epilepticus in slow wave sleep – cognitive deterioration – adrenocorticotropic hormone
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
L. Švecová; P. Sýkora; M. Kolníková
Působiště autorů:
Klinika detskej neurológie LF UK a DFNsP Bratislava
Vyšlo v časopise:
Cesk Slov Neurol N 2015; 78/111(1): 93-97
Kategorie:
Kazuistika
doi:
https://doi.org/10.14735/amcsnn201593
Souhrn
Elektrický status epilepticus v pomalom spánku (ESES) je charakterizovaný špecifickým EEG obrazom, ktorý zaznamenáva signifikantnú aktiváciu epileptiformných zmien v spánku. Je pozorovaný u viacerých epileptických syndrómov (Landau ‑ Kleffnerov syndróm, syndróm kontinuálnych hrotov a vĺn v pomalom spánku – CSWS, benígna detská epilepsia s centro‑temporálnymi hrotmi, atypická benígna parciálna epilepsia detského veku, myoklonicko‑astatická epilepsia a iné). Liečba ESES syndrómu sa sústredí nielen na vymiznutie záchvatov, ale aj na elimináciu epileptiformných zmien, ktoré sú zodpovedné za neuropsychologické poruchy. Aj napriek tomu, že epileptické záchvaty ako aj nález ESES vekom vymiznú, u mnohých detí pretrvávajú rôzne závažné poruchy kognície a reči. Skoré rozpoznanie a efektívna liečba sú potrebné pre zlepšenie dlhodobej prognózy tohto syndrómu. V našej kazuistike poukazujeme na dobrý efekt dlhodobej liečby adrenokortikotropným hormónom.
Kľúčové slová:
elektrický status epilepticus v pomalom spánku – poruchy kognície – adrenokortikotropný hormón
Úvod
Encefalopatia s elektrickým status epilepticus v spánku (ESES) je epileptická encefalopatia detského veku s heterogénnou klinickou manifestáciou (kognitívne, motorické a behaviorálne poruchy v rôznych asociáciách s rôznymi typmi záchvatov). Tieto poruchy sú spojené so špecifickým elektroencefalografickým obrazom, charakterizovaným paroxyzmálnou aktivitou signifikantne aktivovanou počas spánku, ktorá pozostáva z kontinuálnych alebo temer kontinuálnych bilaterálne synchrónnych výbojov hrotov a vĺn počas pomalého spánku. Presná incidencia ESES je neznáma, avšak zdá sa byť zriedkavým, ale pravdepodobne často nerozpoznaným ochorením.
Existuje viacero epileptických syndrómov, u ktorých dochádza k výraznej akcentácii epileptiformných zmien až do obrazu ESES, ako napr. syndróm kontinuálnych hrotov a vĺn v pomalom spánku (CSWS), kde u 100 % detí nachádzame ESES. Záchvaty sú rôzneho charakteru (najčastejšie generalizované tonicko‑klonické, typické absencie, atypické absencie a jednoduché a parciálne komplexné záchvaty) a vyskytujú sa asi u 80 % detí. Najvyšší výskyt CSWS je okolo 4 – 8 rokov. Prognóza je horšia pri včasnejšom začiatku ochorenia.
Landau ‑ Kleffnerov syndróm (LKS) je zriedkavý epileptický syndróm, ktorý sa objavuje u detí medzi 3 – 8 rokom života. Je charakterizovaný získanou afáziou, EEG obrazom ESES, záchvatmi (u 70 – 80 % detí), neuropsychologickými zmenami a poruchami správania. V natívnom EEG sú multifokálne alebo generalizované zmeny, často posterotemporálne lokalizované, v spánku dochádza k výraznej aktivácii zmien až s obrazom ESES. Hlavným znakom syndrómu je získaná afázia, ktorá sa objavuje u dieťaťa s premorbídne normálnym vývojom reči. Začína ako sluchová agnózia, ktorá neskôr prejde do expresívnej poruchy reči. Chlapci sú postihnutí dvakrát častejšie ako dievčatá.
Benígna detská epilepsia s centro‑temporálnymi hrotmi (rolandická epilepsia) je najčastejšia benígna epilepsia detského veku, ktoré vzniká medzi 1 – 14 rokom života (s maximom okolo 8 – 9 roku). U chlapcov sa vyskytuje 1,5 ‑ krát častejšie ako u dievčat. K remisii ochorenia dochádza 2 – 4 roky od vzniku ochorenia a pred 16. rokom života. Celkový počet záchvatov je nízky. Okolo 10 – 20 % detí môže mať časté záchvaty, avšak tieto vekom vymiznú. Prognóza je konštantne veľmi dobrá, s rizikom vzniku málo frekventných generalizovaných záchvatov v dospelosti nižším ako 2 %.
Atypická benígna parciálna epilepsia detského veku je zriedkavé ochorenie (cca 1 na 130 prípadov rolandickej epilepsie). Vek vzniku ochorenia je medzi 2 – 6 rokom života. Hlavným bodom v diferenciálnej diagnostike je výskyt nočných fokálnych záchvatov podobných rolandickým záchvatom, ktoré sú často iniciálnym typom záchvatov. U niektorých pacientov sa ďalej vyskytnú generalizované tonicko‑klonické záchvaty, krátke absencie a občasné zášklby. Dlhodobá prognóza sa zdá byť dobrá s úplným vymiznutím záchvatov, bez ťažkých behaviorálnych porúch a porúch kognície.
Získaný operkulárny syndróm je zriedkavý epileptický syndróm, ktorý sa objavuje vo veku 4 – 8 rokov. Klinicky je charakterizovaný oro‑facio‑linguálnymi deficitmi (ťažká motorická dysfunkcia, slintanie, dyzartria, slabosť svalstva tváre a jazyka). Záchvaty sú väčšinou fokálne motorické, občas rolandické, parciálne komplexné alebo atypické absencie. V EEG nachádzame centrotemporálne bilaterálne alebo temporálne hroty, spánok je charakterizovaný komplexami hrotov a vĺn so sekundárnou bilaterálnou synchróniou až do obrazu ESES.
Myoklonicko‑astatická epilepsia (Dooseho syndróm) je generalizovaná idiopatická epilepsia charakterizovaná vývojom myoklonických a/ alebo myoklonicko‑astatických záchvatov. Vzniká medzi 2 – 5 rokom života. V EEG sú prítomné pravidelné alebo nepravidelné bilaterálne synchrónne výboje hrotov a vĺn alebo viacerých hrotov o frekvencii 2 – 3 Hz. Pred objavením záchvatov sa 84 % detí vyvíja normálne. Chlapci sú postihnutí častejšie ako dievčatá. Postupom ochorenia sa môžu pridružiť ďalšie neurologické abnormity ako ataxia, dyzartria, porucha vývoja reči. Prognóza je nepriaznivá, ak sa v úvode ochorenia objavia generalizované tonicko‑klonické, tonické alebo klonické záchvaty.
Etiológia a patofyziológia
Etiológia je vo väčšine prípadov neobjasnená. Väčšina detí sa pred objavením ochorenia vyvíja normálne. Asi v jednej tretine prípadov odkrýva osobná anamnéza napr. encefalopatiu, pre ‑ alebo perinatálne poruchy a kongenitálnu hemiparézu, tetraparézu, psychomotorickú retardáciu, retardáciu reči a konsangvinitu. V neurozobrazovacích vyšetreniach často nachádzame atrofiu a poruchy migrácie kortexu [1]. Z dôvodu istého efektu kortikosteroidov a imunoglobulínov v liečbe niektorých prípadov idiopatického CSWS a LKS sa uvažuje aj o autoimúnnom podklade ochorenia [2].
Patofyziológia ESES je mechanizmus generujúci ESES prisudzovaný sekundárnej bilaterálnej synchrónii. De Negri [3] predpokladá, že epileptiformné zmeny môžu byť primárne spôsobené aktiváciou retikulo ‑ thalamo ‑ kortikálneho systému so sekundárnou bilaterálnou synchronizáciou cez korpus kalosum. Táto teória koreluje so signifikantnou aktiváciou epileptiformnej aktivity počas spánku.
Vznik neuropsychologického poškodenia je prisudzovaný efektu ESES, čomu nasvedčuje fakt, že kognitívne a motorické poškodenie u CSWS je závislé na dĺžke trvania a závažnosti ESES. Trvanie ESES koreluje s výsledným neuropsychologickým statusom. Závažnosť záchvatov nepredikuje mieru kognitívnej deteriorácie.
Elektroencefalografia
EEG je už v bdelom stave väčšinou patologické, epileptiformné zmeny sú fokálne, multifokálne alebo difúzne, často predominantne lokalizované frontálne alebo frontocentrálne. Spánok, najmä začiatok spánku, aktivuje EEG nález, znásobujú sa výboje, majú tendenciu ku generalizácii a bilaterálnej synchrónii. Počas REM fázy spánku sa paroxyzmálna aktivita stáva fragmentovanou, menej kontinuálnou. Narušenie organizácie spánkových štádií má výrazný podiel na vzniku kognitívnych zmien u pacientov.
Percento epileptiformných zmien počas spánku je vyjadrené indexom hrotov a vĺn (Spike ‑ Wave Index; SWI), ktorý je súčtom všetkých komplexov hrotu a vlny v minútach vynásobených 100 a vydelených celkovým trvaním NREM spánku v minútach.
Longitudinálny spánkový EEG záznam zaznamenáva v priebehu rokov progresívne zlepšenie smerom k normalizácii priemerne okolo 11 roku života. Zmeny počas spánkového EEG sa skracujú, sú menej frekventné a viac fragmentované. Fyziologický obraz spánku sa stane rozpoznateľným. Dlho po klinickej úprave môžu pretrvávať zriedkavé fokálne komplexy ostrých pomalých vĺn najmä v spánkovom EEG. Normalizácia môže trvať viac ako 15 rokov. Vo všetkých prípadoch sú organizácia spánku a spánkové štádiá po vymiznutí ESES normálne.
Liečba
Pri voľbe terapie treba brať do úvahy jednak liečbu epileptických záchvatov, jednak liečbu ESES. Záchvaty nie sú hlavným problémom, keďže ich výsledná prognóza je väčšinou priaznivá. Predpokladá sa, že epileptiformné zmeny sú zodpovedné za vznik porúch reči, behaviorálnych a iných neuropsychologických zmien, a preto cieľom farmakologickej liečby je ich potlačenie. Liečba ESES je úplne empirická a väčšinou len s dočasným efektom.
Možnosti liečby ESES zahŕňajú použitie niektorých „starých“ antiepileptík ako kyselina valproová [4], etosuximid [4] a benzodiazepíny [5] a „nových“ AED ako levetiracetam [6]. Medzi ďalšie antiepileptiká uvádzané v malých súboroch pacientov ako efektívne patrí sultiam [7] a lamotrigin [8].
Viaceré štúdie preukázali, že niektoré AED ako fenobarbital, fenytoín, primidon a karbamazepín môžu u pacientov s generalizovanou aktivitou v spánku a kognitívnou deterioráciou zhoršovať neuropsychologické zmeny a EEG nález a preto sú u týchto detí jednoznačne kontraindikované.
Vzhľadom na nedostatočný efekt monoterapie sú pacienti často od začiatku liečený polyterapiou. Nekonvenčné terapeutické možnosti zahŕňajúce intravenózne imunoglobulíny [9], ketogénnu dietu [10], stimuláciu n. vagus [11] a epileptochirurgiu mnohopočetnými subpiálnymi transekciami [12] preukázali efektivitu v malých súboroch pacientov.
Buzatu et al [13] vo svojej práci hodnotili efektivitu kortikosteroidov u epileptických syndrómov s CSWS (44 pacientov). Kortikosteroidy boli podávané vo vysokých dávkach dlhšie ako 1 rok. Dobrý úvodný efekt jednak v zmysle vymiznutia EEG zmien, jednak klinického a neuropsychologického zlepšenia bol zaznamenaný u 77 % pacientov.
Viacero štúdií preukázalo, že prednison, metylprednisolon a adrenokortikotropný hormón sú efektívne v zlepšovaní EEG zmien aj neuropsychologických funkcií [14 – 15]. Aj keď veľa autorov súhlasí s podávaním vysokých dávok steroidov na dosť dlhé obdobie, neboli realizované žiadne randomizované štúdie, ktoré by dali podklad pre odporúčania o dávkovaní a dĺžke trvania terapie. Avšak Lerman et al [16] predpokladajú, že čím skôr sa začne s liečbou steroidmi, tým kratšia je potrebná doba liečby a je lepšia prognóza. Postupné znižovanie dávky steroidov môže byť spojené s relapsom ESES a neuropsychologickou deterioráciou, čo vyžaduje predĺženie liečby u mnohých detí [4,16].
Kazuistika
Jedná sa o 5,5 ‑ ročného chlapca s pozitívnou pre ‑ aj perinatálnou anamnézou. Je to dieťa z druhej rizikovej gravidity, pre predčasné odlučovanie placenty pôrod cisárskym rezom v 32. gestačnom týždni. Dieťa sa narodilo s nízkou pôrodnou hmotnosťou (2 100 g) a s nízkym Apgarovej skóre (7/ 8/ 7). Po narodení bolo dieťa preložené na jednotku intenzívnej starostlivosti ako prematúrny novorodenec s včasným asfyktickým syndrómom a dychovou tiesňou. Pre anémiu opakovane hemotransfundované. Po dvoch mesiacoch bolo dieťa prepustené a následný psychomotorický vývoj bol v norme (samostatná chôdza okolo 1. roku, reč do 2,5 roku bez porúch vývoja).
Od dvoch rokov je dieťa v sledovaní neurológa pre myoklonicko‑astatické záchvaty s pádom. Na EEG bol nález paroxyzmálnej aktivity centrotemporálne vľavo so sekundárnou generalizáciou. Bola nasadená liečba nitrazepamom s dobrým efektom. Po roku došlo k recidíve záchvatov. Po dobu šiestich mesiacov bola opakovane menená antiepileptická liečba – vystriedané antiepileptiká nitrazepam, valproát, topiramát a klobazam boli bez výraznejšieho efektu. V tomto období (vo veku 3,5 roka) sa pridružili poruchy reči v oblasti percepčnej aj expresívnej. V psychologickom vyšetrení boli intelektové výkony v rámci širšieho populačného priemeru, zaostávanie v oblasti reči, sociálneho vývinu a percepcie. V spánkovom EEG boli prítomné dve nezávislé ohniská v temporálnych zvodoch obojstranne s generalizáciou (obr. 1).
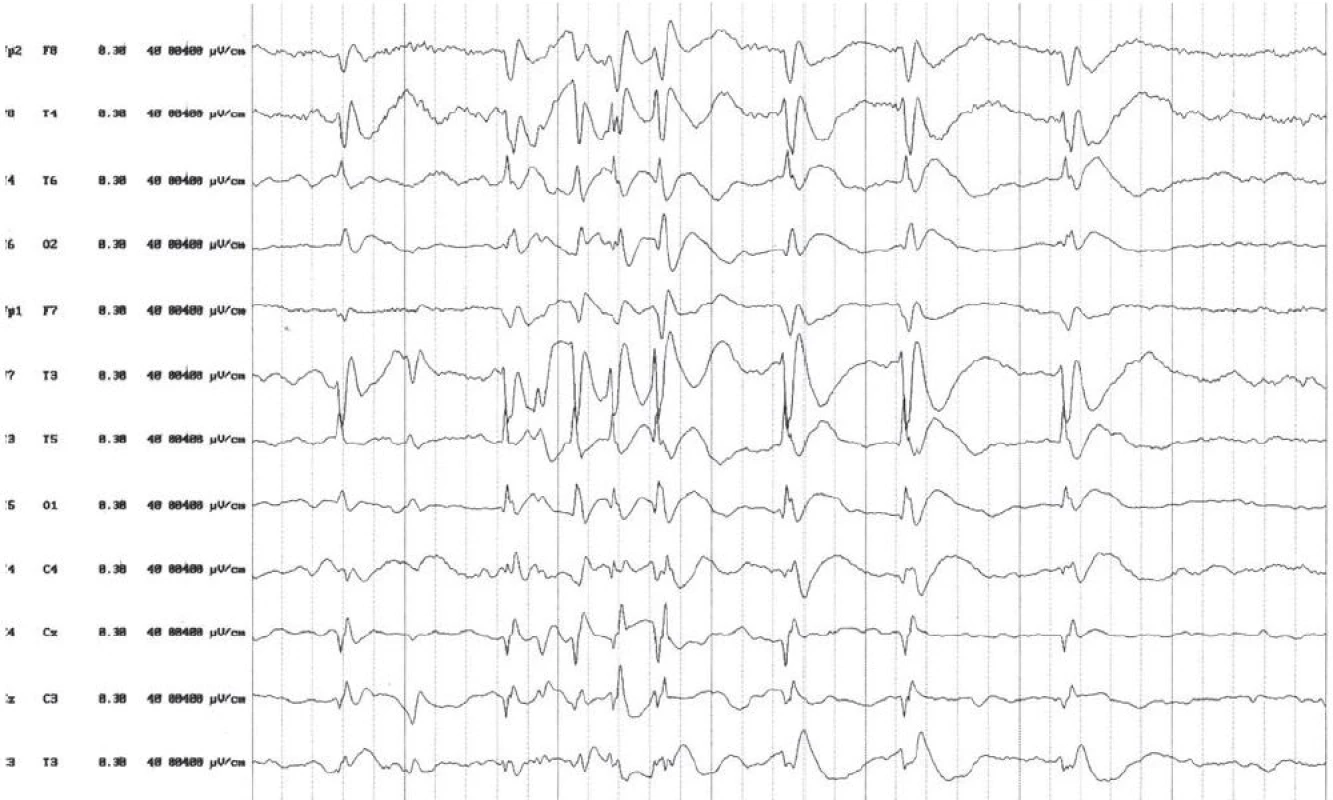
Vzhľadom na objavenie poruchy reči bola zvažovaná diagnóza LKS. Avšak pre toto ochorenie je typický trochu neskorší začiatok a fatická porucha väčšinou predchádza vzniku záchvatov. V rámci diferenciálnej diagnostiky prichádza do úvahy atypická benígna parciálna epilepsia alebo myoklonicko‑astatická epilepsia, u ktorej je však výskyt ESES relatívne zriedkavý.
V liečbe bola nasadená päťdňová pulzná liečba adrenokortikotropným hormónom (ACTH) s následnými dvoma pulzami po týždni s veľmi dobrým efektom. Dieťa bolo tri dni od začatia liečby bez záchvatov. Dva týždne po preliečení ACTH došlo k relapsu záchvatov. O dva mesiace bola započatá kortikoidná liečba dexametasonom v úvodnej dávke 1,5 mg denne. Po troch dňoch u dieťaťa záchvaty vymizli. Opakované zníženie dávky kortikoidov (na 0,5 mg denne) viedlo k relapsu záchvatov. Pre nedostatočnú kompenzáciu (početné záchvaty charakteru astatických, zvýraznenie poruchy expresívnej zložky reči) sme sa po 11-mesačnej kortikoidnej liečbe a po pozitívnej predošlej skúsenosti s ACTH rozhodli pre zmenu liečby. Dieťa sme nastavili na monoterapiu ACTH v dávke 1 mg týždenne s dobrým efektom. Záchvaty sa plne kompenzovali, došlo k zlepšeniu percepčnej aj expresívnej zložky reči a postupne k úprave ad integrum. Zlepšil sa taktiež nález na EEG, pretrváva paroxyzmálna aktivita temporálne vľavo s minimálnym prenosom vpravo (obr. 2). Pri kontrolnej hospitalizácii neboli u dieťaťa zistené nežiadúce účinky dlhodobej liečby ACTH.

Vzhľadom k pravidelnému podávaniu ACTH jedenkrát týždenne po dobu deviatich mesiacov sme zisťovali vplyv liečby na endogénnu tvorbu kortizolu. Kortizolový profil na 5. a 6. deň, t.j. tesne pred podaním ACTH, poukazuje na zachovanú endogénnu tvorbu kortizolu, hodnoty voľného kortizolu sú vo fyziologickom rozmedzí pre daný vek. Po podaní ACTH dochádza k výraznému vzostupu plazmatickej hladiny kortizolu, čomu zodpovedá až 30 ‑ násobné zvýšenie hladiny kortizolu v 24 ‑ hod zbere moču (hladina voľného kortizolu v moči na piaty deň po podaní ACTH bola 21,2 nmol/ 24 hod., po podaní ACTH stúpla na 2 543,3 nmol/ 24 hod).
Záver
Skupina epileptických encefalopatií s výraznou akcentáciou epileptiformnej aktivity v spánku až do obrazu ESES patria medzi závažné ochorenia s neistou prognózou. Aj napriek tomu, že epileptické záchvaty ako aj elektroencefalografický obraz ESES vekom vymiznú, u mnohých detí pretrvávajú rôzne závažné poruchy kognície a reči. Skoré rozpoznanie a efektívna liečba sú potrebné pre zlepšenie dlhodobej prognózy tejto skupiny epileptických syndrómov. ACTH a kortikoidy sú liekmi voľby, dĺžka ich podávania je v literatúre uvádzaná rádovo v týždňoch. Táto kazuistika svedčí o tom, že dlhodobá monoterapia ACTH (bez prídavnej antiepileptickej liečby) môže viesť k remisii záchvatov, zlepšeniu fatických funkcií a EEG nálezu. Sledovanie diurnálneho rytmu kortizolu svedčí o tom, že liečba má pulzný charakter a ani po dlhodobom podávaní nemusí mať nežiaduce účinky.
Zoznam použitých skratiek
ACTH adrenokortikotropný hormón
AED antiepileptikum (Antiepileptic Drug)
EEG elektroecenfalografia
ESES elektrický status epilepticus v pomalom spánku
LKS Landau ‑ Kleffnerov syndróm
CSWS syndróm kontinuálnych hrotov a vĺn v pomalom spánku
MUDr. Lucia Švecová
Klinika detskej neurológie
LF UK a DFNsP
Limbova 1
833 40 Bratislava
e-mail: lsabolova@gmail.com
Prijato k recenzii: 23. 6. 2014
Prijato do tlače: 24. 11. 2014
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Zdroje
1. Tassinari CA, Rubboli G, Volpi L, Meletti S, d’Orsi G, Franca M et al. Encephalopathy with electrical status epilepticus during slow sleep or ESES syndrome including the acquired aphasia. Clin Neurophysiol 2000; 111(Suppl 2): S94 – S102.
2. Scholtes FB, Hendriks MP, Renier WO. Cognitive deterioration and electrical status epilepticus during slow sleep. Epilepsy Behav 2005; 6(2): 167 – 173.
3. De Negri M. Electrical status epilepticus during sleep (ESES). Different clinical syndromes: towards a unifying view? Brain Dev 1997; 19(7): 447 – 451.
4. Inutsuka M, Kobayashi K, Oka M, Hattori J, Ohtsuka Y. Treatment of epilepsy with electrical status epilepticus during slow wave sleep and its related disorders. Brain Dev 2006; 28(5): 281 – 286.
5. Francois D, Roberts J, Hess S, Probst L, Eksioglu Y. Medical management with Diazepam for electrical status epilepticus during slow wave sleep in children. Pediatr Neurol 2014; 50(3): 238 – 242. doi: 10.1016/ j.pediatrneurol.2013.11.002.
6. Chen XQ, Yhang WN, Yang ZX, Zhao M., Cai FC, Huang SP et al. Efficacy of levetiracetam in electrical status epilepticus during sleep of children: a multicenter experience. Pediatr Neurol 2014; 50(3): 234 – 239. doi: 10.1016/ j.pediatrneurol.2013.10.015.
7. Kramer U, Sagi L, Golberg ‑ Stern H, Zelnik N, Nissenkorn A, Ben ‑ Zeev B. Clinical spectrum and medical treatment of children wth electrical status epilepticus is sleep (ESES). Epilepsia 2009; 50(6): 1517 – 1524. doi: 10.1111/ j.1528 – 1167.2008.01891.x.
8. Guerrini R, Genton P, Bureau, Parmeggiani A, Salas ‑ Puig X, Santucci M et al. Multilobar polymicrogyria, intractable drop attacks seizures, and sleep‑related electrical status eppilepticus. Neurology 1998; 51(2): 504 – 512.
9. Mikati MA, Saab R, Fayad MN, Choueiri RN. Efficacy of intravenous immunoglobulin in Landau ‑ Kleffner syndrome. Pediatr Neurol 2002; 26(4): 298 – 300.
10. Nikanorova M, Miranda M.J, Atkins M, Sahlholdt L. Ketogenic diet in treatment of refractory continuous spikes and waves during slow sleep. Epilepsia 2009; 50(5): 1127 – 1130. doi: 10.1111/ j.1528 – 1167.2008.01958.x.
11. Park ID. The effects of vagus nerve stimulation on patients with intractable seizures and either Landau ‑ Kleffner syndrome or autism. Epilepsy Behav 2003; 4(3): 286 – 290.
12. Loddenkemper T, Comso G, Kotagal P, Haut J, Klaas P, Gupta A et al. Epilepsy surgery in children with electrical status epilepticus in sleep. Neurosurgery 2009; 64(2): 327 – 337. doi: 10.1227/ 01.NEU.0000336767.14252.76.
13. Buzatu M, Bulteau C, Altuzarra C, Dulac O, Van Bogeart P. Corticosteroids as treatment of epileptic syndromes with continuous spike ‑ waves during slow sleep. Epilepsia 2009; 50 (Suppl 7): 58 – 72. doi: 10.1111/ j.1528 – 1167.2009.02224.x.
14. Tsuru T, Mori M, Mizuguchi M, Momoi MY. Effects of high‑dose intravenous corticosteroid therapy in Landau ‑ Kleffner syndrome. Pediatr Neurol 2000; 22(2): 145 – 147.
15. Smith MC, Hoeppner TJ. Epileptic encephalopathy of late childhood: Landau ‑ Kleffner syndrome and the syndrome of continuous spikes and waves during slow ‑ wave sleep. J Clin Neurophysiol 2003; 20(6): 462 – 472.
16. Lerman P, Lerman ‑ Sagie T, Kivity S. Effect of early corticosteroid therapy for Landau ‑ Kleffner syndrome. Dev Med Child Neurol 1991; 33(3): 257 – 260.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2015 Číslo 1
-
Všechny články tohoto čísla
-
Analýza dat v neurologii
XLIX. Vzájemná srovnatelnost a aproximace odhadů relativního rizika a poměru šancí - Recenze knih
- Zpráva z 8. plenárního setkání Evropské společnosti pro Huntingtonovu nemoc
- Erratum
- Zpráva z 15. kongresu Evropské asociace neurochirurgických společností, Praha, 12.– 17. říjen 2014. www.eans2014.com
- Abstrakta přednášek, které odezněly na VII. neuromuskulárním kongresu Brno, 15.– 16. květen 2014
- Asymptomatická spondylogenní komprese krční míchy
- Protokol diagnostiky a léčby hyponatremie a hypernatremie v neurointenzivní péči
- Interindividuální variabilita provádění Sémontova repozičního manévru
-
Komentář k článku autorů Stehlíková et al.
Interindividuální variabilita provádění Sémontova repozičního manévru - Validace české verze Neuropathic Pain Symptom Inventory (NPSIcz)
- Mini‑Mental State Examination – česká normativní studie
- Editorial
- Projekt ncRNAPain
- Algoritmus operací mnohočetného myelomu a solitárního plazmocytomu páteře
- Autoimunitní encefalitidy
- Neuromyelitis optica a poruchy jejího širšího spektra – retrospektivní analýza klinických a paraklinických nálezů
- Normální hodnoty Nového testu libosti pachů u zdravé populace
- Neurostimulace, neuromodulace a neurotizace v terapii neurogenního močového měchýře
- Chirurgicky obtížně řešitelné meningeomy
- Liečba adrenokortikotropným hormónom u pacienta s epileptickou encefalopatiou spojenou s elektrickým status epilepticus v pomalom spánku – kazuistika
- Doc. MUDr. Eugen Eiben, CSc., má 75 rokov
- Webové okénko
-
Analýza dat v neurologii
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Protokol diagnostiky a léčby hyponatremie a hypernatremie v neurointenzivní péči
- Mini‑Mental State Examination – česká normativní studie
- Autoimunitní encefalitidy
- Asymptomatická spondylogenní komprese krční míchy
