Klinický standard pro diagnostiku a léčbu pacientů s ischemickou cévní mozkovou příhodou a s tranzitorní ischemickou atakou – verze 2016
Clinical Guideline for the Diagnostics and Treatment of Patients with Ischemic Stroke and Transitory Ischemic Attack – Version 2016
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
O. Škoda; R. Herzig; R. Mikulík; J. Neumann; D. Václavík; M. Bar; D. Šaňák; A. Tomek; D. Školoudík
Působiště autorů:
Cerebrovaskulární sekce České neurologické společnosti ČLS JEP
Vyšlo v časopise:
Cesk Slov Neurol N 2016; 79/112(3): 351-363
Kategorie:
Doporučené postupy
doi:
https://doi.org/10.14735/amcsnn2016351
Souhrn
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Předchozí Klinický standard (KS) byl vypracován v roce 2011 jako interdisciplinární odborný dokument zveřejněný v sadě KS Národního referenčního centra ČR. Vzhledem k významnému odbornému vývoji v oblasti diagnostiky, léčby i prevence cévních mozkových příhod (CMP) nastala naléhavá potřeba jej aktualizovat. Současný KS – verze 2015 – byl upraven na základě všech dostupných vědeckých důkazů, mezinárodních doporučení i klinických dat, jež jsou v současnosti k dispozici. Zároveň tento dokument zohledňuje stav péče o pacienty s akutní CMP v síti vysoce specializovaných center v ČR, vč. organizačních principů. Standard nenahrazuje platné legislativní předpisy, ale jako konsenzuální doporučení výboru Cerebrovaskulární sekce České neurologické společnosti shrnuje současné optimální odborné postupy v diagnostice a léčbě CMP.
Základní informace o KS
Zdůvodnění vývoje KS
Ischemická CMP je závažné cévní onemocnění, které je 2.–3. nejčastější příčinou úmrtí v rozvinutých zemích a nejčastější příčinou dlouhodobé invalidity. Zlepšující se možnosti terapeutického ovlivnění zejména v časných fázích vyžadují zavádění a kontrolu adekvátních postupů, které je vhodné standardizovat. Existuje literárně podložený předpoklad, že dodržování vhodně navrženého standardu zvyšuje kvalitu péče v akutním stavu, vyjádřenou především výsledkovými ukazateli a kvalitu dlouhodobých výsledků vyjádřených lepším funkčním stavem a nižší závislostí pacientů na ošetřovatelské podpoře.
Cílem KS je:
- docílení co nejnižší úmrtnosti a co nejnižších důsledků onemocnění;
- podpora včasného rozhodování o efektivní léčbě, minimalizace chybných rozhodnutí;
- zvýšení efektivity vynaložených nákladů, zejména zajištěním vysoce odborné péče v rámci iktového programu.
Způsob ověřování KS v praxi
Zatím není v běžné praxi prováděno systematické ověřování. Audit personálních, materiálních a organizačních předpokladů nemocnic hlásících se do sítě Komplexních cerebrovaskulárních a iktových center proběhl poprvé v roce 2010 podle požadavků Věstníku MZ ČR č. 2/2010. Druhé kolo se uskutečnilo v roce 2012 dle Věstníků MZ ČR 3 a 4/ 2012. Ve Věstníku č. 10/2012 byla vydána Triáž pacientů s akutní CMP v přednemocniční a nemocniční péči s rozdělením spádových oblastí jednotlivých center a byly definovány Ukazatele kvality a výkonnosti Komplexních cerebrovaskulárních a iktových center, které jsou každoročně vyhodnocovány. V roce 2015 byla vyhlášena Ministerstvem zdravotnictví ČR ve Věstníku č. 4/2015 nová výzva k akreditaci Center vysoce specializované cerebrovaskulární péče a Center vysoce specializované péče o pacienty s iktem.
Způsob vývoje KS
KS byl vytvořen členy Cerebrovaskulární sekce ČNS JEP ve spolupráci s dalšími odborníky na základě inspirace sady standardů vyvinutých organizací European Stroke Organization (ESO) vydaných pod názvem Standardy pro diagnostiku a léčbu mozkových příhod, verze 2003, 2008, 2009 a konsenzu z roku 2015 [39,40] s přizpůsobením pro specifické podmínky péče v České republice.
Vědecké ověření KS
Tým autorů při vývoji KS považoval za dostatečné převzetí vědeckých důkazů, které vycházejí z Recommendation for stroke therapy (ESO) 2008, 2009 a konsenzu z roku 2015 [39,40], dále z doporučení American Heart Association [41,42], aktuálních odborných doporučení Cerebrovaskulární sekce ČNS [59] a z vlastních prací členů autorského týmu [51,55,56,61,68,76,81–84].
Klasifikace vydaných doporučení
Ke klasifikaci vydaných doporučení terapeutických intervencí byl použit systém doporučený EFNS Task Force [19] s modifikací dle SIGN.
Vymezení KS
Vymezení klinického stavu
Obory, kterých se KS týká
Hlavní obory: 209 – neurologie.
Ostatní obory: 001 – všeobecný praktický lékař, 101 – vnitřní lékařství – interna, 102 – angiologie, 107 – kardiologie, 201 – rehabilitační a fyzikální medicína, 504 – cévní chirurgie, 506 – neurochirurgie, 708 – anesteziologie, resuscitace a intenzivní medicína, 809 – radiologie a zobrazovací metody, 903 – klinická logopedie.
Oblasti péče, kterých se KS týká
Akutní lůžková standardní a intenzivní, ambulantní, následná lůžková a následná ambulantní, Centra.
Skupina pacientů, kterých se KS týká
Pacienti s ischemickou CMP, event. s tranzitorní ischemickou atakou.
Vymezující klinické klasifikace
Kódy a názvy výkonů uvedených v následujících tabulkách jsou v souladu s platnými verzemi MKN-10 a Seznamu výkonů.
Diagnózy (tab. 1)
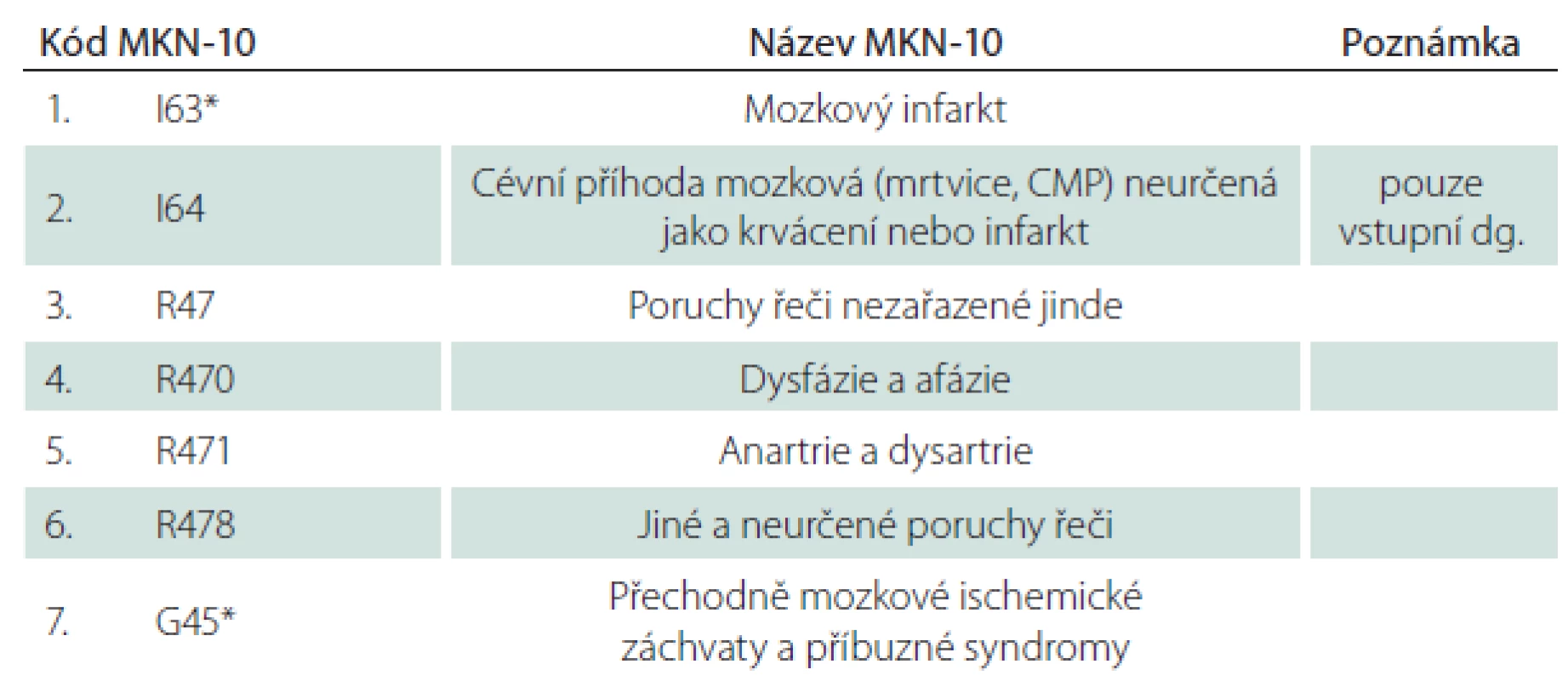
Ostatní klinické klasifikace
Výkony
V rámci diagnostického postupu je požadováno včasné provedení CT mozku (alternativně MR mozku), další diagnostické metody jsou doplňkové – jde o duplexní sonografii tepen, transkraniální sonografii, CT či MR angiografii, perfuzní vyšetření, případně digitální subtrakční angiografii atd. Z terapeutických výkonů jsou v časné fázi indikovány především výkony rekanalizační, z nichž je standardním postupem prvé volby systémová trombolýza. Trombolýzu lze identifikovat podle vykázaných ZULP. Ostatní terapeutické výkony jsou určeny pouze pro vybrané pacienty dle klinického stavu a dalších okolností – zahrnují např. mechanické postupy rekanalizace, intraarteriální trombolýzu, karotickou endarterektomii či neurochirurgické zákroky jako dekompresní kraniektomii apod. (tab. 2).
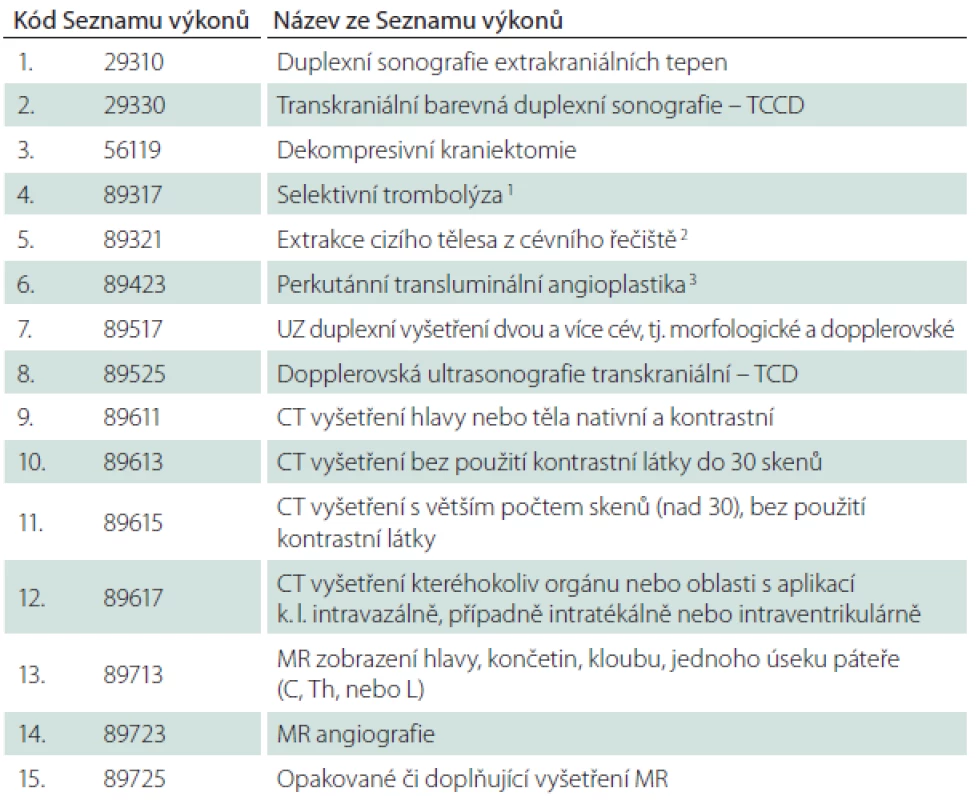
Materiál (tab. 3)
Negativní klinické vymezení
KS se podrobně nezabývá problematikou rehabilitace a ošetřovatelské péče, které jsou nezbytnou součástí péče o pacienty s touto diagnózou. Předmětem KS také není léčba dysfagie, dysartrie, dysfonie atd.
Jiné používané klasifikace
NIHSS – National Institute of Health Stroke Scale, Rankin Scale (disability), Bartel Index.
Klíčová slova
Iktus, CMP, mozkový infarkt, prevence, akutní léčba iktu, iktová jednotka, rehabilitace.
Vymezení procesu péče
Hlavní proces péče je ta část procesu, kterou KS popisuje ve všech podrobnostech. Probíhají v něm klíčové aktivity, jež mají vliv na výsledek, dále je v něm spotřebována podstatná část zdrojů a vztahují se k němu významné statistiky a ukazatele (tab. 4).
Konečný stav pacienta je zhodnocen pomocí popisu objektivního neurologického nálezu. Dále lze použít následující validizované škály: Modifikovaná Rankinova škála (soběstačnost), Index Barthelové (hodnocení aktivit denního života), škála NIHSS (tíže neurologického deficitu).

Kvalifikační a technické požadavky na poskytovatele
Kvalifikace instituce poskytovatele a jejích oddělení
Péče o pacienty s CMP probíhá na pracovištích splňujících podmínky a požadavky dle platné legislativy, předpisů MZ ČR a ČLK.
Přednemocniční péče
Přednemocniční péči poskytuje zdravotnická záchranná služba (ZZS) (územní, lokální) s určeným cílovým nemocničním zařízením, které má stanovené technické a personální předpoklady poskytnout adekvátní nemocniční péči pacientům s akutní CMP (Centra vysoce specializované cerebrovaskulární péče a Centra vysoce specializované péče o pacienta s iktem). Postupuje přitom podle Triáže vydané Věstníkem MZ ČR č. 10/2012, v aktuálním znění.
Nemocniční péče
V akutní fázi probíhá péče optimálně na JIP odbornosti 2I9 vybavené pro ošetřovací den intenzivní péče minimálně na části lůžek 00055, optimálně 00053, na zbylých lůžkách 00057 podle vyhlášky MZ ČR č. 101/2002 Sb., jejímiž variantami jsou:
a) samostatná iktová jednotka,
b) iktová lůžka jako součást širší neurologické JIP,
c) iktová lůžka v rámci víceoborové JIP.
Uvedená lůžka iktové jednotky jsou součástí Centra vysoce specializované péče o pacienta s iktem, nebo Centra vysoce specializované cerebrovaskulární péče, které zajišťuje komplexní diagnostickou, léčebnou a časnou rehabilitační péči o pacienty s akutní fází CMP. Centrum vysoce specializované cerebrovaskulární péče poskytuje kromě systémové trombolýzy pro vlastní spádovou oblast a pro spolupracující Centra vysoce specializované péče o pacienta s iktem také intraarteriální trombolýzu vč. dalších endovaskulárních (mechanických) metod (vč. angioplastiky/stentování) a též možnost neurochirurgických a cévně chirurgických výkonů. Zajišťuje také diagnostiku vzácných a nejasných příčin akutní CMP, zejména u mladých jedinců.
V případě potřeby resuscitační péče je tato realizována zpravidla na oddělení ARO. Na JIP odbornosti 2I9 může být takový charakter péče poskytnut jen v těch případech, jsou-li splněna technická a personální kritéria pro ošetřovací den resuscitační péče daná vyhláškou MZ ČR č. 134/1998 Sb., v platném znění.
V akutní fázi může být péče v indikovaných případech (jako je neurochirurgický zákrok, významná interní komorbidita atd.) poskytnuta i na jiné JIP zabývající se péčí o pacienty s CMP (interní, neurochirurgická atd.) a vybavené minimálně pro OD typu 00055.
Hospitalizace na iktových jednotkách snižuje mortalitu a morbiditu oproti hospitalizaci pacientů s CMP na standardních lůžkách. Cílem je tudíž hospitalizovat co nejvíce pacientů na specializovaných iktových jednotkách v rámci Center vysoce specializované péče o pacienta s iktem a Center vysoce specializované cerebrovaskulární péče. Dosažení rekanalizace mozkových tepen v terapeutickém časovém okně je vědecky prokázaný faktor zlepšující výsledný stav pacientů s akutní ischemickou CMP. Proto je nutné, aby byli hospitalizováni v centru vysoce specializované péče, které je schopno poskytnout potřebný typ rekanalizační léčby. Překlad pacienta mezi Centry vysoce specializované péče o pacienta s iktem a Centry vysoce specializované cerebrovaskulární péče probíhá rovněž podle aktuálního znění Triáže.
Z iktové jednotky má být pacient přeložen na lůžka se zvýšenou ošetřovatelskou péčí, kde je prováděna další léčba a především časná intenzivní rehabilitace.
Pacienty přijaté s časovým odstupem více než 24 hod od vzniku mozkového infarktu (MI) lze také hospitalizovat na standardním neurologickém oddělení, event. i na jiném nemocničním oddělení (interním, geriatrickém) zabývajícím se péčí o pacienty s CMP, s 24hod konziliární neurologickou službou a nepřetržitou dostupností komplementu. Hospitalizace na specializované iktové jednotce je i v těchto případech nicméně preferována.
Po stabilizaci zdravotního stavu může být pacient doléčen na standardním lůžku neurologického, interního, neurochirurgického, geriatrického nebo rehabilitačního oddělení.
Následná péče
Optimálně v domácím prostředí, s podílem praktického lékaře, odborných lékařů (oboru neurologie a fyzioterapie, event. interního lékařství), odborných vysokoškolských pracovníků (psychologa, logopeda), nelékařských zdravotnických pracovníků (všeobecné sestry domácí péče, fyzioterapeut, ergoterapeut) a sociálních institucí (pečovatelská služba apod.).
V případě trvající potřeby chronické hospitalizace lůžko následné péče rehabilitačního typu, léčebny pro dlouhodobě nemocné (LDN) nebo oddělení chronické intenzivní péče.
Technické požadavky
Přednemocniční péče
Vozidlo ZZS s předepsanou výbavou dle vyhlášky MZ ČR č. 434/1992 Sb., v platném znění.
Nemocniční péče
Vybavení standardního pracoviště JIP dle vyhlášky MZ ČR č. 134/1998 Sb., v platném znění, způsobilého pro poskytování ošetřovacích dnů intenzivní péče na části lůžek minimálně 00055, optimálně 00053, na zbytku lůžek 00057, které je klíčovou součástí Center vysoce specializované péče o pacienta s iktem a Center vysoce specializované cerebrovaskulární péče. Bližší podmínky pro personální, technické a organizační vybavení Center vysoce specializované péče o pacienta s iktem a Center vysoce specializované cerebrovaskulární péče stanoví Věstník MZ ČR č. 2/2010, dále Věstník MZ ČR č. 4/2015.
Je nezbytná nepřetržitá dostupnost laboratorního komplementu (biochemie, hematologie, event. nukleární medicíny), RTG a CT nebo MR, vč. možnosti cévního vyšetření pomocí CT nebo MR angiografie, kardiologa a internisty. Nejpozději do 24 hod je nezbytná dostupnost sonografického vyšetření extrakraniálních tepen, optimálně i transkraniální sonografie a katetrizační angiografie. Pro Centrum vysoce specializované cerebrovaskulární péče je nutná nepřetržitá dostupnost angiografie, neuroradiologických, neurochirurgických a cévně chirurgických intervencí, nepřetržitá dostupnost neurosonologického vyšetření.
Součástí uvedených center je i lůžková část zvýšené ošetřovatelské péče způsobilá pro poskytování péče o pacienty s převažující hodnotou kategorie 4, s odpovídajícím technickým a personálním vybavením, kde se pokračuje v léčbě, v časné komplexní rehabilitační péči a v diagnostice subtypu CMP.
Standardní lůžkové neurologické oddělení je vybaveno v souladu s požadavky vyhlášky MZ ČR č. 134/1998 Sb., v platném znění, pro poskytování ošetřovacího dne 00001. Vhodná je dostupnost medicinálních plynů (kyslík), lineárních dávkovačů nebo infuzních pump, EKG a oxymetrů.
Centra přispívají do aktuálních registrů, protože registry slouží jako nástroje zlepšování kvality péče.
Následná péče
V případě pobytu na lůžku následné péče jsou potřebné prostředky zdravotnické techniky a pomůcky v majetku zdravotnického zařízení a v souladu se zákonem č. 48/1997 Sb. pacientovi poskytovány po dobu hospitalizace.
V případě domácí péče, kromě standardního vybavení ordinací příslušných lékařů a zdravotnických pracovníků, je nutno vybavit pacienta pomůckami a zdravotnickou technikou, které jsou nezbytné pro vykonávání jeho základních potřeb, zajištění soběstačnosti, pohyblivosti, případně k zabránění komplikací (hůl, toaletní křeslo, vozík, chodítko, nástavec na WC, antidekubitální matrace, polohovací lůžko atd.).
Personální kvalifikační požadavky
Přednemocniční péče
Tým ZZS (lékař ZZS, zdravotnický záchranář, řidič vozidla ZZS).
Nemocniční péče
Vedoucím Centra vysoce specializované péče o pacienta s iktem nebo Centra vysoce specializované cerebrovaskulární péče je lékař se specializovanou způsobilostí v oboru neurologie (dále neurolog) a s kurzem intenzivní medicíny v oboru neurologie získaném na akreditovaném pracovišti a s erudicí v diagnostice a léčbě CMP. Bližší podmínky pro personální, technické a organizační vybavení Center vysoce specializované péče o pacienta s iktem a Center vysoce specializované cerebrovaskulární péče stanoví Věstník MZ ČR č. 2/2010 a Věstník MZ ČR č. 4/2015.
Ústavní pohotovostní služba (ÚPS) musí být zajištěna také neurologem.
Dalšími členy týmu jsou neurologové pracující na JIP (vhodný je i kurz intenzivní péče v neurologii a kurz neurosonologie) a specializované všeobecné sestry, v počtech dle vyhlášky MZ ČR č. 493/2005 Sb., v platném znění.
Součástí týmu je do 24 hod dostupný neurosonografista, radiolog a internista (kardiolog), v případě Centra vysoce specializované cerebrovaskulární péče i neurochirurg, cévní chirurg, lékař se způsobilostí provádět endovaskulární neurointervence.
V pracovní dny musí být 8 hod denně dostupný logoped, rehabilitační lékař, klinický psycholog a sociální pracovník.
Nelékařští zdravotničtí pracovníci se způsobilostí dle zákona č. 96/2004 Sb. a vyhlášky č. 424/2004 Sb. jsou zajištěni v počtech a se vzděláním dle vyhlášky MZ ČR č. 134/ 1998 Sb., v platném znění. Na lůžkové části se zvýšenou ošetřovatelskou péči jsou tito pracovníci požadováni v počtu 1–2/1 lůžko.
Významnou součástí týmu nelékařských pracovníků jsou rehabilitační pracovníci (podle koncepce oboru Rehabilitace a fyzikální medicíny je zapotřebí na iktové jednotce: 1 fyzioterapeut/5 lůžek, 1 ergoterapeut/10 lůžek a 1 klinický logoped se specializovanou průpravou v klinické logopedii/10 lůžek a na lůžkové části zvýšené ošetřovatelské péče: 1 fyzioterapeut/3 lůžka, 1 klinický logoped se specializovanou průpravou v klinické logopedii/10 lůžek a 1 ergoterapeut/10 lůžek).
Následná péče
V ústavních rehabilitačních zařízeních je pacient v péči rehabilitačních lékařů.
V zařízeních následné péče koordinuje péči o pacienta ošetřující lékař, zpravidla geriatr, internista, rehabilitační lékař apod.
V domácích podmínkách koordinuje následnou péči o pacienta registrující praktický lékař ve spolupráci s lékařem ve specializované cerebrovaskulární poradně nebo v odborné ambulanci, která tyto pacienty dispenzarizuje. Na odborné péči se podílí neurolog, internista, event. kardiolog, psychiatr, psycholog, rehabilitační lékař, logoped, neurochirurg, intervenční radiolog. Nelékařští zdravotničtí pracovníci jsou zastoupeni rehabilitačními pracovníky a všeobecnými sestrami domácí péče. U nesoběstačných pacientů je žádoucí rovněž péče pracovníků sociální péče – pečovatelské služby.
Doporučení (tab. 5)

Popis nemoci a její začátek
Definice nemoci
Definice onemocnění
Skupinu ischemických CMP tvoří MI (dokončená ischemická CMP) a tranzitorní ischemická ataka (TIA). MI je podle kritérií Světové zdravotnické organizace definován jako rychle se rozvíjející klinické známky ložiskového mozkového postižení trvající déle než 24 hod nebo vedoucí ke smrti, bez přítomnosti jiných zřejmých příčin než cerebrovaskulárního onemocnění. Proto každý pacient se známkami ložiskového mozkového postižení je po tuto dobu pokládán za pacienta s diagnózou MI až do uplynutí prvních 24 hod, kdy je diagnóza potvrzena, nebo do okamžiku kompletního odeznění neurologického postižení v prvních 24 hod – v takovém případě se může jednat o TIA, jež je v současnosti z diagnostického hlediska považována za součást skupiny ischemických CMP, se shodnými požadavky na akutní management i sekundární prevenci. MI je nejčastěji způsoben uzávěrem mozkové tepny trombem či embolem.
Patofyziologie
MI je způsoben uzávěrem nebo zúžením mozkových cév s výrazným snížením průtoku krve, které vede k ischemizaci části mozkové tkáně. Zdaleka nejčastějším mechanizmem je zúžení nebo úplný uzávěr intrakraniální tepny většinou v důsledku embolizace z proximálně uloženého zdroje (krční tepny, aortální oblouk, srdce). Jindy může jít o uzávěr perforujících arteriol při jejich mikroangiopatii. Méně často jde o uzávěr krční tepny, intrakraniální postižení velkých tepen, intrakraniální žilní trombózu nebo případně kombinaci více faktorů (zejména hypotenze, arytmie srdeční), na základě kterých vznikají hemodynamicky podmíněné infarkty.
V nepříznivém případě je konečným stavem nekróza a apoptóza mozkových buněk v oblasti ischemie (těžké hypoperfuze).
Rizika, příčiny a prevence onemocnění
Rizika a příčiny onemocnění
MI je z hlediska příčiny heterogenní onemocnění.
Nejčastější příčiny jsou:
- ateroskleróza s postižením krčních a méně často intrakraniálních tepen,
- embolizace z kardiálního nebo jiného centrálního zdroje,
- mikroangiopatie postihující perforující arterioly s následnými lakunárními infarkty.
Méně časté příčiny jsou:
- disekce krční tepny,
- trombofilní stavy,
- intrakraniální žilní trombóza,
- paradoxní embolizace (nejčastěji otevřeným foramen ovale),
- vaskulitidy a vaskulopatie,
- vasospazmy při subarachnoidálním krvácení,
- infekce,
- genetická a další onemocnění.
Prevence vzniku onemocnění (primární prevence)
Prevence cerebrovaskulárních onemocnění je jedna z priorit zdravotní politiky státu. Nezbytné je zajištění dostatečné informovanosti veřejnosti o příznacích CMP a nutnosti okamžitého přivolání RZP při vzniku příznaků. Primární prevence zahrnuje:
a) Režimová a léčebná opatření k eliminaci vaskulárních rizikových faktorů
Tlak krve (TK) má být kontrolován pravidelně. U pacientů s vysokým TK je doporučena úprava životního stylu a individualizovaná farmakoterapie s cílem dosažení normální hodnoty TK 120/80 mm Hg. U pacientů se zvýšeným TK (v rozmezí 120–139/80–90 mm Hg) a se srdečním selháním, infarktem myokardu (IM), diabetem mellitem (DM) nebo chronickým renálním selháním je indikována antihypertenzní medikace.
Glykemie má být kontrolována pravidelně. U pacientů s DM jsou doporučeny úprava životního stylu a individualizovaná farmakoterapie. TK má být u diabetiků ovlivňován intenzivně s cílem dosažení hodnoty TK pod 130/80 mm Hg. Léčba má, pokud možno, zahrnovat inhibitory angiotenzin-konvertujícího enzymu nebo antagonisty angiotenzinových receptorů.
Hladina cholesterolu v krvi má být kontrolována pravidelně. Je doporučeno, aby hypercholesterolemie (s hladinou LDL-cholesterolu > 3,9 mmol/l) byla ovlivněna úpravou životního stylu a statinem. Statin je indikován také u pacientů s asymptomatickou karotickou stenózou.
Je doporučeno nekouřit.
Je doporučeno vyvarovat se nadměrné konzumace alkoholu.
Je doporučena pravidelná fyzická aktivita.
Je doporučena dieta s omezením soli a nasycených tuků, bohatá na ovoce, zeleninu a vlákninu.
Jedincům s vyšší hodnotou body mass indexu (BMI) je doporučena redukční dieta.
Nejsou doporučeny doplňky vitaminů – antioxidantů.
V primární prevenci iktu není doporučena hormonální substituční terapie.
b) Specifické medikamentózní postupy – antitrombotickou (antiagregační či antikoagulační) terapii
U žen ve věku 45 a více let, u kterých není zvýšené riziko intracerebrální hemoragie a které mají dobrou gastrointestinální toleranci, je doporučena nízká dávka acetylsalicylové kyseliny (ASA); její účinnost je ale nízká.
Je doporučeno, aby podávání nízké dávky ASA bylo zváženo u mužů v primární prevenci IM; nesnižuje však riziko ischemického iktu.
U pacientů s ischemickou chorobou dolních končetin (periferní arteriální nemocí) může být v primární prevenci iktu opodstatněné podávání cilostazolu.
Jiné antiagregační látky než ASA a cilostazol nejsou v primární prevenci iktu doporučeny.
ASA může být doporučena pacientům s nevalvulární fibrilací síní (FS) mladším 65 let, u kterých nejsou přítomny vaskulární rizikové faktory.
Pokud nejsou kontraindikace, je u pacientů s nevalvulární FS ve věku 65–75 let, u kterých nejsou přítomny vaskulární rizikové faktory, doporučena buď ASA nebo perorální antikoagulace (international normalized ratio – INR 2,0–3,0).
Pokud nejsou kontraindikace, je u pacientů s nevalvulární FS ve věku > 75 let nebo u mladších pacientů, u kterých jsou ale přítomny rizikové faktory jako arteriální hypertenze, dysfunkce levé komory nebo DM, doporučena antikoagulace (INR 2,0–3,0).
Je doporučeno, aby pacientům s FS, kteří nemohou užívat antikoagulancia, byla podávána ASA.
Je doporučeno, aby pacienti s FS, kteří mají umělou srdeční chlopeň, užívali dlouhodobě antikoagulaci s cílovou hodnotou INR závisející na typu chlopně, nikoliv však nižší než INR 2,0–3,0.
U pacientů s asymptomatickou stenózou arteria carotis interna (ACI) > 50 % je doporučena nízká dávka ASA s cílem snížení rizika jejich cévních příhod.
c) Karotickou endarterektomii a angioplastiku
Karotická endarterektomie (CEA) není doporučena u asymptomatických osob s významnou karotickou stenózou (dle North American Symptomatic Carotid Endarterectomy Trial – NASCET 60–99 %) s výjimkou těch, u kterých je vysoké riziko iktu (tzn. pacientů, kteří mají zároveň kumulaci dalších rizikových faktorů pro vznik CMP) a nízké (< 3 %) riziko perioperačního iktu, IM nebo smrti.
Je doporučeno, aby pacienti před CEA a po ní užívali ASA.
Karotický stenting (CAS) může být zvážen u vysoce selektovaných pacientů s asymptomatickou karotickou stenózou (min. 60 % dle angiografie a min. 70 % dle ultrazvuku).
Další používané klasifikace onemocnění
Dle etiopatogeneze
- Onemocnění velkých tepen – většinou u pacientů se stenózou karotidy nad 50 % a nálezem infarktu ve stejnostranné kortikosubkortikální oblasti nebo subkortikální oblasti velikosti > 1,5 cm.
- Kardioembolizační – mezi nejvýznamnější příčiny patří FS, chlopenní náhrady, myxom síně, infekční endokarditida, stav po IM (do čtyř týdnů), trombus v levé komoře nebo levé síni, akinetický segment levé komory, dilatační kardiomyopatie a další.
- Onemocnění malých tepen (lakunární infarkty) – ischemie v subkortikální oblasti, typicky v bazálních gangliích, thalamu či mozkovém kmeni do velikosti 1,5 cm.
- Jiné příčina – kolagenózy, vaskulitidy, nezánětlivé vaskulopatie (fibromuskulární dysplazie, Moya moya, amyloidní angiopatie a další), intrakraniální žilní trombóza.
- Nezjištěná příčina.
Dle postižené tepny
Na povodí a. cerebri anterior, a. cerebri media, a. cerebri posterior, vertebrobazilární povodí, perforující arterioly a další.
Doporučení (tab. 6)

Proces péče
Anamnéza a klinický obraz při vzniku onemocnění
Anamnéza
Anamnéza a klinický obraz jsou u ischemických CMP většinou charakterizovány náhlým vznikem příznaků ložiskového postižení mozku jako:
- slabost až ochrnutí nebo porucha citlivosti poloviny těla (hemiparéza až hemiplegie, hemihypestezie i hemidysestezie);
- porucha symbolických funkcí (zejména fatická porucha);
- náhle vzniklá nevysvětlitelná závrať nebo náhlé pády, zejména ve spojení s předchozími příznaky;
- náhlá porucha ostrosti vidění, diplopie;
- amauróza, zpravidla jednostranná;
- další neurologické příznaky podle lokalizace léze.
Klinický obraz
Ischemická CMP (MI) se zpravidla projevuje náhlým rozvojem ložiskové neurologické symptomatologie centrálního (mozkového) původu podle teritoria postižené mozkové tepny – slabostí až ochrnutím a/ nebo poruchou citlivosti poloviny těla, poruchou symbolických funkcí, deviací hlavy a očních bulbů, pohledovou parézou, výpady zorného pole, diplopií, náhle vzniklou nevysvětlitelnou závratí nebo náhlým pádem ve spojení s předchozími centrálními neurologickými příznaky, amaurózou (zpravidla jednostrannou), event. dalšími symptomy dle lokalizace léze. Bolest hlavy bývá přítomna vzácněji než u mozkového krvácení. K dalším vzácnějším symptomům patří úvodní zvracení, porucha vědomí nebo epileptické paroxyzmy.
Diagnostika a diferenciální diagnostika
Zahrnuje provedení diagnostických testů – viz níže. U pacientů indikovaných k trombolýze by doba od příjezdu pacienta do nemocnice k zahájení léčby neměla přesáhnout 60 min.
Přednemocniční péče
Při podezření na akutní CMP má být vždy přivolána ZZS. Každý pacient s akutní CMP, byť se u něho projevují jen mírné příznaky, musí být považován za kriticky nemocného pacienta.
Všichni pacienti by měli být přivezeni do nemocnice s iktovým centrem nebo komplexním cerebrovaskulárním centrem. Pokud pacient splňuje časová kritéria pro zahájení trombolytické terapie, musí být směrován do itového centra, schopného poskytnout intravenózní trombolýzu (v prvních 4,5 hod) nebo event. intraarteriální trombolýzu či mechanickou rekanalizaci (v prvních 6 hod).
Nemocniční péče
Po příjezdu pacienta do nemocnice musí být provedeny následující diagnostické testy a vyšetření:
a) změření krevní tlaku;
b) změření saturace kyslíku u pacientů s podezřením na dechovou insuficienci nebo při známkách hypoxie;
c) neurologické vyšetření;
d) laboratorní vyšetření: krevní obraz, biochemický skríning a koagulace;
e) CT nebo MR mozku (ve většině případů půjde o vstupní vyšetření);
f) EKG vyšetření;
g) ultrazvukové vyšetření extrakraniálních a intrakraniálních tepen. Toto vyšetření lze v individuálních případech nahradit jiným cévním vyšetřením (CT angio, MR angio, DSA).
Urgentnost je dána latencí, s jakou se pacient dostaví do nemocnice. U pacientů s možnou indikací k trombolýze musí být vyšetření provedena do 60 min od jejich příjezdu (vyjma bodu f), není-li toto vyšetření akutně dostupné).
Další možná vyšetření prováděná v průběhu hospitalizace k upřesnění etiologie CMP:
a) interní a/ nebo kardiologické vyšetření;
b) speciální sonografické vyšetření (např. detekce mikroembolizací, stanovení cerebrovaskulární rezervní kapacity atd.);
c) vyšetření mozkových cév pomocí CT angiografie, MR angiografie či DSA;
d) vyšetření MR (jako alternativa je už v základních vyšetřeních);
e) transtorakální a transezofageální echokardiografie;
f) Holterovo monitorování EKG a TK;
g) speciální laboratorní a genetická vyšetření, vč. vyšetření trombofilních stavů;
h) SPECT mozku metodou HMPAO, vč. stanovení cerebrovaskulární rezervní kapacity;
i) elektroencefalografie, případně další elektrodiagnostika;
j) perfuzní vyšetření mozku pomocí CT nebo MR.
Následná péče
Základní ambulantní dispenzární péče dle Vyhlášky 60/1997 Sb. probíhá v neurologické ambulanci, optimálně ve specializované cerebrovaskulární poradně. Doplňková péče podle potřeby v ambulanci interní, kardiologické atd. Kontroly základních fyziologických parametrů, zejména krevního tlaku, zajišťuje registrující praktický lékař. Je indikováno provedení vyšetření uvedených v bodě 3 výše sloužící k precizní diagnostice etiologie MI a k uskutečnění potřebných preventivních opatření vč. nasazení adekvátní sekundárně preventivní terapie. U pacientů s prokázanou cévní patologií (uzávěr nebo stenóza) jsou indikována periodická neurosonologická vyšetření – viz standard č. 13.3, 13.4, 13.6 – Verlag–Dashöfer [40].
Základní léčba
U ischemické CMP je léčba závislá na časovém faktoru (princip farmakologického okna) a příčině.
Přednemocniční terapie
Přednemocniční péči zajišťuje většinou ZZS a spočívá v následujících postupech:
- zajištění vitálních funkcí, zajištění žilního přístupu;
- péče o dýchací cesty, podání kyslíku v případě hypoxie nebo podezření na dechovou insuficienci;
- podání antihypertenziv při TK nad 220/120 mm Hg nebo při známkách kardiálního či renálního selhání; TK je doporučeno snižovat pomalu a maximálně do hodnot systol./ diastol. TK 180/110 mm Hg;
- symptomatická terapie dle stavu pacienta (antiemetika, anxiolytika, antikonvulziva atd.).
Nemocniční terapie
Obecná
a) Monitorování vitálních a neurologických funkcí na iktové jednotce (jednotce péče o pacienty s CMP) nebo na běžném oddělení (po 72 hod od rozvoje iktu v případě přetrvávání významného neurologického deficitu).
b) Zajištění funkce plic a ochrany dýchacích cest s podáním kyslíku v případě poklesu saturace O2 pod 95 %.
c) Péče o kardiovaskulární systém, vč. léčby přidružených a nových srdečních onemocnění, zejména arytmií a srdečního selhání.
d) Regulace krevního tlaku – opatrné snižování arteriálního TK u pacientů s extrémně vysokým TK (> 220/120 mm Hg) zjištěným opakovaným měřením nebo u pacientů s těžkým srdečním selháním, disekcí aorty či hypertenzní encefalopatií; nízký TK sekundárně v důsledku hypovolemie nebo ve spojitosti s neurologickým zhoršením léčit objemovými expandéry.
e) Monitorování metabolizmu glukózy, při hladině cukru v krvi nad 10 mmol/l je doporučena léčba inzulinem, při hladině cukru v krvi pod 2,8 mmol/l je doporučena intravenózní dextróza nebo infuze 10–20% glukózy.
f) Monitorování tělesné teploty, při tělesné teplotě nad 37,5 °C se podávají antipyretika (paracetamol) nebo se aplikuje fyzikální chlazení. Nutné je okamžitě pátrat po zdroji infekce a tu léčit.
g) Zajištění nutrice s korekcí elektrolytů a tekutin, k náhradě tekutin v průběhu prvních 24 hod je doporučen fyziologický roztok.
Specifická, vč. popisu operačního výkonu
a) Do 4,5 hod od nástupu příznaků ischemické CMP v indikovaných případech intravenózní aplikace rtPA (0,9 mg/kg; max. 90 mg), kdy je 10 % dávky podáno jako bolus a následuje infuze po dobu 60 min. Výjimkou je uzávěr arteria basilaris, kdy je intravenózní aplikace rtPA akceptována i po 4,5 hod od nástupu příznaků ischemické CMP. Pokud doba nástupu příznaků ischemické CMP není známa nebo je nejasná, protože příznaky byly přítomny při probuzení nebo tento údaj nelze získat (např. při afázii nebo při poruše vědomí), může být rtPA podán na základě nálezu zobrazovacího vyšetření, který svědčí pro trvání ischemie méně než 4,5 hod. Intravenózní rtPA může být užit i u pacientů nad 80 let. Je doporučeno snížit TK před intravenózním podáním rtPA, pokud dosahuje hodnot 185/110 mm Hg nebo vyšších.
b) Do 6 hod od nástupu příznaků ischemické CMP provedení mechanické trombektomie stent-retrievery v případě symptomatického uzávěru intrakraniální části arteria carotis interna nebo proximální části arteria cerebri media (segment M1 a M2) nebo arteria basilaris. Výjimkou je uzávěr arteria basilaris, kdy je provedení mechanické trombektomie akceptováno i po 6 hod od nástupu příznaků ischemické CMP. Pokud doba nástupu příznaků není známa nebo je nejasná, protože příznaky byly přítomny při probuzení či tento údaj nelze získat (např. při afázii nebo při poruše vědomí), může být mechanická trombektomie provedena na základě nálezu zobrazovacího vyšetření, který svědčí pro trvání ischemie méně než 6 hod.
c) Do 48 hod od nástupu příznaků ischemické CMP provedení dekompresní kraniektomie u pacientů do 60 let věku s maligním infarktem v povodí arteria cerebri media.
d) Je doporučeno, aby při léčbě expanzivních infarktů mozečku, které utlačují mozkový kmen, byla provedena časná ventrikulostomie nebo chirurgická dekomprese do 72 hod.
e) U všech pacientů s MI je indikována časná antiagregační medikace (ASA v dávce 100 – 325 mg nebo klopidogrel v dávce 75 mg během 48 hod) v případě, že není indikována antikoagulační anebo trombolytická terapie.
f) Obecné podání plné dávky nefrakcionovaného heparinu, nízkomolekulárního heparinu či heparinoidů není v léčbě pacientů s akutním ischemickým iktem doporučeno.
g) V současné době není žádné doporučení léčby pacientů s MI neuroprotektivy.
h) Rheologika, kortikoidy, vazodilatancia a hemodiluce nejsou u pacientů s MI indikovány.
Prevence a léčba komplikací
a) U imobilních pacientů s vysokým rizikem hluboké žilní trombózy se doporučuje po prodělaném MI podat nízkou dávku heparinu subkutánně nebo nízkomolekulární heparin v dávce miniheparinizace v rámci prevence hluboké žilní trombózy a plicní embolie, přestože existuje mírně vyšší riziko dodatečného nitrolebního krvácení.
b) Infekce vzniklé po MI musí být léčeny vhodnými antibiotiky. Aspirační pneumonii lze předcházet vyšetřením pacientovy schopnosti polykat a v případě dysfagie vyživováním nazogastrickou sondou. Profylaktické podávání antibiotik není doporučeno, levofloxacin může být u pacientů s MI škodlivý.
c) Časná mobilizace pacienta po MI pomáhá předcházet četným komplikacím, vč. vzniku aspirační pneumonie, hluboké žilní trombózy a dekubitů.
d) K redukci incidence venózního tromboembolizmu je doporučena časná rehydratace.
e) Doporučuje se podávat antikonvulziva za účelem profylaxe recidiv epileptických záchvatů.
f) Preventivní podávání antikonvulziv pacientům po čerstvém MI, u kterých se dosud záchvaty nevyskytly, se nedoporučuje.
g) U každého pacienta s MI je doporučeno zhodnocení rizika pádů a u rizikových pacientů doplňkové podávání kalcia/ vitaminu D. Bisfosfonáty (alendronát, etidronát a risedronát) jsou doporučeny u žen s předchozími frakturami.
h) U pacientů s močovou inkontinencí jsou doporučeny vyšetření a léčba specialistou.
i) Je doporučeno posouzení polykacích problémů. U pacientů s MI s poruchou polykání je doporučeno časné (během 48 hod) zahájení výživy nazogastrickou sondou. U pacientů s MI v prvních dvou týdnech není doporučeno zvažovat výživu perkutánní enterální gastrostomií.
j) Perorální dietní doplňky jsou doporučeny jen pacientům s malnutricí bez dysfagie.
k) Zatímco posouzení kognitivního deficitu se jeví žádoucí, nejsou k dispozici dostatečné údaje k doporučení specifického léčebného postupu.
l) Je doporučeno sledovat u pacientů během hospitalizace i po propuštění výskyt deprese. U pacientů s depresí je doporučována nefarmakologická a farmakologická antidepresivní terapie.
m) K léčbě emoční lability po MI má být zvážena medikamentózní terapie.
n) U vybraných pacientů jsou k léčbě neuropatické bolesti po MI doporučena tricyklická antidepresiva nebo antiepileptika.
o) Je doporučeno zvážení léčby spasticity po MI botulotoxinem.
p) Je doporučeno, že osmotická terapie může být užita v léčbě zvýšeného nitrolebního tlaku před léčbou chirurgickou, pokud je tato zvažována.
q) Stran užití hypotermie u pacientů s maligním vývojem MI nejsou dána žádná doporučení.
Prevence recidivy stavu (sekundární prevence)
Sekundární prevence může významně snížit pravděpodobnost opakování ischemické CMP. Sekundární prevence zahrnuje:
a) Režimová a léčebná opatření k eliminaci vaskulárních rizikových faktorů
- Je doporučeno, aby byl pravidelně kontrolován TK. Snižování TK je doporučeno po akutní fázi iktu, a to i u pacientů s normálními hodnotami TK.
- Je doporučeno, aby byla pravidelně kontrolována glykemie. Je doporučeno ovlivnění DM úpravou životního stylu a individualizovanou farmakoterapií.
- U pacientů s DM 2. typu, kteří nevyžadují inzulin, je po iktu doporučena léčba pioglitazonem.
- U pacientů s nekardioemboligenním iktem je doporučena léčba statinem.
- Je doporučen zákaz kouření cigaret.
- Je doporučen zákaz nadměrné konzumace alkoholu.
- Je doporučena pravidelná fyzická aktivita.
- Je doporučena dieta s omezením soli a nasycených tuků, bohatá na ovoce, zeleninu a vlákninu.
- Jedincům s vyšší hodnotou BMI je doporučena redukční dieta.
- Nejsou doporučeny doplňky vitamínů – antioxidantů.
- Není doporučena hormonální substituční terapie.
- Je doporučeno, aby poruchy dýchání ve spánku jako obstrukční spánková apnoea (OSA) byly léčeny s využitím dýchání s kontinuálním pozitivním tlakem v dýchacích cestách (continuous positive airway pressure breathing).
- Je doporučeno, aby byl u pacientů s kryptogenním iktem a vysoce rizikovým patentním foramen ovale (PFO) zvážen jeho endovaskulární uzávěr.
b) Specifické medikamentózní postupy – antitrombotickou (antiagregační či antikoagulační) terapii
- Je doporučeno, aby byla pacientům po ischemické CMP podávána antitrombotická terapie.
- Je doporučeno, aby pacientům nevyžadujícím antikoagulaci byla podávána antiagregační terapie. Má být, pokud možno, podáván samotný klopidogrel (75 mg/d) nebo samotná ASA (50–325 mg/d). Alternativně je možno použít samostatně triflusal. Kombinace ASA (2 × 25 mg) a dipyridamolu (2 × 200 mg), dosud rovněž podávaná v této indikaci, není v ČR od 1. 1. 2016 dostupná – doporučujeme převést pacienty z této kombinace dle možnosti na klopidogrel.
- Kombinace ASA a klopidogrelu není u pacientů s nedávným ischemickým iktem doporučena, s výjimkou pacientů se specifickými indikacemi (např. nestabilní angina pectoris nebo non-Q IM, nebo nedávný stenting); léčba má být podávána po dobu až devíti měsíců po příhodě.
- Kombinace ASA a klopidogrelu může být opodstatněna u pacientů s nedávným (v posledních 30 dnech) iktem nebo TIA v důsledků významné (70–99%) stenózy velké intrakraniální tepny, a to po dobu do 90 dnů.
- Kombinace ASA a klopidogrelu může být zvážena u lehkého iktu (minor stroke) nebo TIA, a to se zahájením během 24 hod a podáváním po dobu do 90 dnů.
- U pacientů s rozvojem iktu na antiagregační terapii je doporučeno nové posouzení patofyziologie a rizikových faktorů.
- U pacientů s nevalvulární FS po prodělaném ischemickém iktu je v rámci sekundární prevence indikována trvalá perorální antikoagulační terapie. V případě použití warfarinu je nutné dosažení cílového INR 2,0–3,0. V současnosti jsou dostupná také tzv. nová antikoagulancia (NOAK) – dabigatran, apixaban, rivaroxaban, která nevyžadují pravidelné kontroly koagulace a navíc jsou v určitých případech významně bezpečnější a účinnější než warfarin. Jejich použití je však limitováno úhradovými omezeními.
- Zahájení a forma perorální antikoagulace by měla být pečlivě zvážena u rizikových pacientů. Samotný vyšší věk není kontraindikací perorální antikoagulace.
- U pacientů s kardioemboligenním iktem bez spojitosti s FS je doporučeno podávat perorální antikoagulancia (warfarin s cílovým INR 2,0–3,0), pokud je vysoké riziko jeho recidivy.
- Je doporučeno, aby antikoagulancia nebyla podávána po nekardioemboligenním ischemickém iktu s výjimkou specifických situací, jako jsou ateromy aorty, fuziformní aneuryzma bazilární tepny, cervikální arteriální disekce, PFO za přítomnosti potvrzené hluboké žilní trombózy nebo aneuryzmatu septa síní.
- Pokud je perorální antikoagulace kontraindikována, je doporučeno podání optimální antiagregace – kombinace nízké dávky ASA a dypiridamolu, dosud upřednostňovaná v této indikaci, není v ČR od 1. 1. 2016 dostupná – doporučujeme klopidogrel 75 mg.
c) Karotickou endarterektomii (CEA) nebo angioplastiku
- CEA je doporučena u pacientů se stenózou ACI 70–99 %. CEA má být prováděna pouze v centrech s frekvencí peroperačních komplikací (všechny ikty a úmrtí) méně než 6 %.
- Je doporučeno provedení CEA co nejdříve po poslední ischemické příhodě, po TIA a lehké CMP nejlépe během dvou týdnů.
- Je doporučeno, že CEA může být indikována u některých pacientů se stenózou 50–69 %; nejpřínosnější může být pro muže s nedávným výskytem hemisferálních symptomů. CEA u stenózy (50 – 69%) má být prováděna pouze v centrech s frekvencí peroperačních komplikací (všechny ikty a úmrtí) méně než 3 %.
- CEA není doporučena u pacientů se stenózou méně než 50 %.
- Je doporučeno ponechat pacienty na antiagregační terapii jak před CEA, tak i po ní.
- Karotická perkutánní transluminátní angioplastika a/ nebo stenting (CAS) jsou doporučeny u pacientů s významnou symptomatickou stenózou karotidy: pacienti s kontraindikací CEA, lokalizací stenózy v chirurgicky nepřístupné oblasti, restenózou po předchozí CEA a poradiační stenózou.
- CAS je indikován jako alternativa k CEA u pacientů se symptomatickou karotickou stenózou (> 70% podle neinvazivního zobrazení nebo > 50% podle katetrizační angiografie) se středním nebo nízkým rizikem komplikací spojených s endovaskulární intervencí.
- Při volbě mezi CEA a CAS je opodstatněné zvážení věku pacienta. U pacientů starších než cca 70 let může být užití CEA spojeno s lepším výsledným stavem než CAS, především pokud je anatomie tepen nepříznivá pro endovaskulární intervenci. U mladších pacientů je CAS rovnocenná CEA, týká-li se rizika periprocedurálních komplikací (iktus, IM nebo úmrtí) a dlouhodobého rizika ipsilaterálního iktu.
- Pacientům má být podávána kombinace klopidogrelu a ASA ihned před stentingem a nejméně měsíc po něm.
d) Angioplastiku nebo operaci vertebrální tepny
U pacientů se stenózou extrakraniálního úseku vertebrální tepny, u kterých přetrvávají symptomy navzdory optimální medikamentózní léčbě, mohou být zváženy stenting nebo operace (vertebrální endarterektomie nebo transpozice vertebrální tepny).
e) Eliminaci zjištěného centrálního embolického zdroje (postižené chlopně, myxom, aortální aneuryzma, nástěnná trombóza, léčba arytmií, srdečních a aortálních zánětů apod.).
Následná péče
Následná ústavní a rehabilitační péče
Cílem rehabilitační péče (institucionální nebo ambulantní) je:
- podpora návratu mozkových funkcí, nácvik denních činností a aktivního pohybu s využitím pomůcek k dosažení maximální míry soběstačnosti;
- motivace pacienta k aktivnímu přístupu;
- reedukace řeči (logopedická péče o fatické poruchy), snižování následků kognitivních poruch, ovlivňování poruch polykání, nácvik substitučních mechanizmů;
- předcházení a ovlivňování komplikací, jako jsou kloubní afekce, např. zmrzlé rameno, kontraktury, spastické postižení pohybového aparátu;
- psychoterapeutické působení ke zmírnění psychiatrických následků vč. deprese;
- pracovní rehabilitace s cílem resocializace a návratu pracovní schopnosti pacienta;
- instruktáž rodinných příslušníků s cílem jejich zapojení do rehabilitace pacienta v domácím prostředí.
Aktivní rehabilitace by měla optimálně být zahájena časně a probíhat tak dlouho, dokud lze objektivně pozorovat zlepšení neurologického deficitu.
Potřeba dlouhodobé ošetřovatelské péče a sociální pomoci je dána stupněm funkčního postižení, mírou způsobilosti pro denní úkony, mírou nezávislosti a také kvalitou rodinného zázemí. Domácí ošetřovatelská péče je výhodnější než institucionální a musí být vytvářeny podmínky pro její maximální využití. Je potřebná co nejširší edukace a zapojení rodinných příslušníků pacienta do rehabilitačních a resocializačních aktivit.
Lázeňská péče je součástí rehabilitační léčby nemocných s CMP a provádí se v zařízeních splňujících nezbytné podmínky (viz indikační seznam – Vyhláška MZ ČR č. 58/1997 Sb., kterou se stanoví indikační seznam pro lázeňskou péči o dospělé, děti a dorost a doporučené postupy).
Následná ambulantní péče
Ambulantní péče o pacienty s cerebrovaskulárními chorobami je specializovaným druhem neurologické péče, který je plně zaměřen na vyšetřování, léčení a dispenzární sledování nemocných po prodělané CMP. Frekvenci dispenzárních prohlídek v cerebrovaskulárních poradnách s přihlédnutím k typu CMP, klinickému stavu, nálezům stenóz, provedeným rekonstrukčním nebo rekanalizačním výkonům upravuje Vyhláška č. 60/1997 Sb. MZ ČR ve smyslu přílohy vyhlášky dle § 1.
Očekávaný výsledný stav a prognóza
Cíl léčby
Cílem léčby je plné uzdravení pacienta, event. minimalizace postižení do takového stupně, aby byla zachována soběstačnost pacienta a byla možná jeho resocializace. Přibližně 30 % pacientů ovšem zůstává trvale nesoběstačných, většina z nich vyžaduje institucionální péči.
Prognóza
Prognóza pacienta s MI závisí na:
a) lokalizaci a velikosti infarktu;
b) věku a přidružených onemocněních pacienta (především stavu kardiovaskulárního aparátu);
c) správném zajištění vitálních funkcí a poskytování intenzivní péče v akutním období;
d) včasnosti diagnózy a zahájení léčby.
V závislosti na závažnosti postižení a poskytnuté léčbě lze po třech měsících od MI očekávat asi 30% mortalitu, 30% invaliditu a 40% pravděpodobnost částečného nebo úplného vyléčení.
Riziko recidivy ischemické CMP je do 10 % v následujících 30 dnech, asi 5 % ročně a asi 25–30 % v následujících pěti letech. Zvláště vysoké riziko recidivy MI je u pacientů s chronickou FS a symptomatickou stenózou vnitřní karotidy nad 70 %.
Posudková hlediska
Rozhodující je stupeň trvalého neurologického postižení, zejména v oblasti motoriky končetin, poruchy řečových a kognitivních funkcí a z nich plynoucí míra soběstačnosti, event. i pracovní schopnosti pacienta. Na konečném stavu se podílejí i přítomná přidružená onemocnění a dostatečná intenzivní rehabilitace pacienta. Konečné posudkové rozhodnutí musí být provedeno až s patřičným odstupem po proběhlém MI, obvykle ne dříve než přibližně za šest měsíců od příhody. Velmi žádoucí je snaha o pracovní reedukaci, případně rekvalifikaci pacienta a maximální resocializaci, s instruktáží a zapojením rodinných příslušníků do těchto procesů.
Další doporučená léčba, ošetřovatelská péče nebo sociální pomoc
Mimo sekundární prevenci a léčbu přidružených nemocí závisí další schéma péče a pomoci (především ošetřovatelská péče a sociální pomoc) nemocným po MI na:
- výsledném zdravotním stavu nemocného vč. přítomnosti přidružených onemocnění, stupni trvalého neurologického deficitu a míře soběstačnosti;
- sociálním zázemí pacienta (možnost zajištění optimální péče v domácím prostředí či nutnost další institucionální péče s převahou zdravotnických nebo sociálních prvků).
Doporučení (tab. 7)

Výsledky
Doporučení pro sběr dat za účelem vyhodnocování struktury, procesu a výsledků péče
K hodnocení kvality a výkonnosti péče o pacienty s MI můžeme použít data zdravotních pojišťoven, data národního registru hospitalizovaných (ÚZIS) a data nově sbíraná, v rámci ukazatelů kvality a výkonnosti Center vysoce specializované cerebrovaskulární péče a Center vysoce specializované péče o pacienty s iktem – dle Věstníku MZ ČR č. 10/2012 [15].
Protože data zdravotních pojišťoven, data národního registru hospitalizovaných (ÚZIS) jsou klinicky málo specifická, byl zaveden speciální sběr dat dle tzv. Ukazatelů výkonnosti a kvality center pečujících o pacienty s akutní CMP. Požadovaná data všechna centra zasílají každoročně povinně na odbor zdravotní péče Ministerstva zdravotnictví ČR. Jedná se o počty pacientů s akutní CMP přijatých v rámci sledovaného období daným centrem z primárního, případně sekundárního spádu (komplexní centra), počty pacientů hospitalizovaných na JIP, počty pacientů, u kterých byla provedena intravenózní (systémová) trombolýza, vč. podílu pacientů, u nichž byla tato léčba provedena do 60 min od přijetí, dále počty pacientů s provedenou mechanickou rekanalizací a s provedenou neurochirurgickou intervencí, dále o 30denní mortalitu, vztaženou na příslušnou diagnózu, počty pacientů přeložených na akutní rehabilitační lůžka a délku hospitalizace pacientů s diagnózou akutní CMP v daném centru. Analýza těchto dat umožňuje sledovat vývoj kvality péče o pacienty s MI v ČR a také vytipovat případné problémy v jednotlivých centrech, u kterých je nutno zjednat nápravu (tab. 8).

Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Ondřej Škoda, Ph.D.
Neurologické oddělení
Nemocnice Jihlava
Vrchlického 59
586 33 Jihlava
e-mail: skodao@nemji.cz
Zdroje
1. Zákon č. 372/2011 Sb., o zdravotních službách a podmínkách jejich poskytování (zákon o zdravotních službách).
2. Zákon č. 48/1997 Sb., o veřejném zdravotním pojištění, v platném znění.
3. Zákon č. 95/2004, Zákon o podmínkách získávání a uznávání odborné způsobilosti a specializované způsobilosti k výkonu zdravotnického povolání lékaře, zubního lékaře a farmaceuta, v platném znění.
4. Zákon č. 96/2004 Sb., o podmínkách získávání a uznávání způsobilosti k výkonu nelékařských zdravotnických povolání a k výkonu činností souvisejících s poskytováním zdravotní péče a o změně některých souvisejících zákonů, v platném znění.
5. Vyhláška č. 134/1998 Sb., Seznam zdravotních výkonů s bodovými hodnotami, v platném znění.
6. Vyhláška č. 385/2006 Sb., o zdravotnické dokumentaci.
7. Vyhláška č. 386/2007 Sb., kterou se stanoví nemoci, u nichž se poskytuje dispenzární péče, časové rozmezí dispenzárních prohlídek a označení specializace dispenzarizujícího lékaře.
8. Vyhláška č. 434/1992 Sb., o zdravotnické záchranné službě, ve znění pozdějších předpisů.
9. Vyhláška č. 49/1993 Sb., o technických a věcných požadavcích na vybavení zdravotnických zařízení.
10. Vyhláška č. 58/1997 Sb., indikační seznam lázeňské péče, v platném znění.
11. Metodické opatření č. 12/ 1998 Věstníku MZ ČR (Koncepce následné lůžkové péče).
12. Věstník MZ ČR č. 2/2010 Péče o pacienty s cerebrovaskulárním onemocněním v ČR.
13. Věstník MZ ČR č. 8/2010 Metodický pokyn – cerebrovaskulární péče v ČR.
14. Věstník MZ ČR č. 3/2012 Cerebrovaskulární péče v ČR – změna seznamu center se statutem iktové centrum.
15. Věstník MZ ČR č. 10/2012 Metodický pokyn – péče o pacienty s akutní cévní mozkovou příhodou.
16. Věstník MZ ČR č. 4/2015 Metodický pokyn – cerebrovaskulární péče v ČR.
17. Věstník MZ ČR č. 11/2015 Seznam center vysoce specializované cerebrovaskulární péče a péče o pacienty s iktem.
18. Aboderin I, Venables G, for the PAN European Consensus Meeting on Stroke Management. Stroke management in Europe. J Intern Med 1996;240 : 173–80.
19. Adams H, Brott T, Crowell R, et al. Guidelines for the Management of Patients with Acute Ischemic Stroke. A Statement for Healthcare Professionals from a Special Writing Group of the Stroke Council, American Heart Association. Stroke 1994;25(9):1901–14.
20. Adams HP jr, Woolson RF, Helgason C, et al. Low molecular weight heparinoid, ORG 10172 (Danaparoid), and outcome after acute ischemic stroke: a randomized controlled trial. JAMA 1998;279 : 1265–72.
21. Asplund K, Marké LÅ, Terént A, et al. Costs and gains in stroke prevention: european perspective. Cerebrovasc Dis 1993;3(Suppl 1):34–42.
22. Berkhemer OA, Fransen PS, Beumer D, et al. A randomized trial for itraarterial treatment of acute ischemic stroke. N Engl J Med 2015;372(2):11–20. doi: 10.1056/NEJMoa1411587.
23. Biller J, Feinberg WM, Castaldo JE, et al. Guidelines for carotid endarterectomy: a statement for healthcare professionals from a special writing group of the Stroke Council, American Heart Association. Stroke 1998;29(2):554–62.
24. Brainin M, Barnes M, Baron JC, et al. Guidance for the preparation of neurological management guidelines by EFNS scientific task forces – revised recommendations 2004. Eur J Neurol 2004;11(9):577–81.
25. Brainin M, European Federation of Neurological Societies Task Force. Neurological acute stroke care: the role of European neurology. Eur J Neurol 1997;13(4):435–41.
26. Brott T, Fieschi C, Hacke W. General therapy of acute ischemic stroke. In: Hacke W, Hanley DF, Einhäup K, Bleck TP, eds. NeuroCritical Care. Berlin, Springer 1994;553–77.
27. Brott T, Reed RL. Intensive care for acute stroke in the community hospital setting. Stroke 1989;20(5):694–7.
28. Campbell BC, Mitchell PJ, Kleinig TJ, et al. Endovascular therapy for ischemic stroke with perfusion-imaging selection. N Engl J Med 2015;372(11):1009–18.
29. Caplan, Biller J, Feinberg WM L et al. Guidelines for carotid endarterectomy: a statement for healthcare professionals from a special writing group of the Stroke Council, American Heart Association. Stroke 1998;97(5):501–9.
30. European Ad Hoc Consensus Group: European strategies for early intervention in stroke. Cerebrovasc Dis 1996;6 : 315–24.
31. Goyal M, Demchuk AM, Menon BK, et al. Randomized Assessment of Rapid Endovascular Treatment of Ischemic Stroke. N Engl J Med 2015;372(11):1019–30. doi: 10.1056/NEJMoa1414905.
32. Hacke W, Stingele R, Steiner T, et al. Critical care of acute ischemic stroke. Intensive Care Med 1995;21(10):856–62.
33. Indredavik B, Slørdahl S, Bakke F, et al. Stroke unit treatment: long - term effects. Stroke 1997;28(10):1861–6.
34. Langhorne P, Williams B, Gilcrist B. Do stroke units safe lifes? Lancet 1993;342(8868):395–8.
35. National Institute of Neurolocial Disorders and Stroke: rt - PA Stroke Study Group (NINDS). Tissue plasminogen activator for acute ischemic stroke. N Engl J Med 1995;333(24):1581–7.
36. Pan European Consensus Meeting on Stroke management, 1995, Nov 8 – 10, Helsingborg, Sweden (abstracts). Neurol Neurochir Pol 1997;31(Suppl 1):1–40.
37. Saver JL, Goyal M, Bonafe A, et al. Stent-retriever thrombectomy after intravenous t-PA vs. t-PA alone in stroke. N Engl J Med 2015;372(24):2285–95. doi: 10.1056/NEJMoa1415061.
38. Stroke Units Trialists` Collaboration. A systematic review of the randomized trials of organised impatient (stroke unit) care after stroke. Br Med J 1997;314(7088):1151–9.
39. The European Stroke Organisation (ESO) Executive Committee and the ESO Writing Committee. Guidelines for management of ischaemic stroke and transient ischaemic attack 2008. Cerebrovasc Dis 2008;25(5):457–507. doi: 10.1159/000131083.
40. Update Guidelines January 2009 New Elements. [online]. Available from URL: http://www.eso–stroke.org/pdf/ESO_Extended_Thrombolysis_KSU.pdf.
41. Meschia JF, Bushnell C, Boden-Albala B, et al. Guidelines for the primary prevention of stroke: a statement for healthcare professionals from the American Heart Association/ American Stroke Association. Stroke 2014;45(12):3754–832. doi: 10.1161/STR.000000 0000000046.
42. Kernan WN, Ovbiagele B, Black HR, et al. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2014;45(7):2160–236. doi: 10.1161/STR.0000000000000024.
43. Aulický P, Rabinstein A, Seet RC, et al. Dosing of tissue plasminogen activator often differs from 0.9 mg/ kg, but does not affect the outcome. J Stroke Cerebrovasc Dis 2013;22(8):1293–7. doi: 10.1016/j.jstrokecerebrovasdis.2012.10.010.
44. Bar M, Školoudík D, Roubec M, et al. Transcranial duplex sonography and CT angiography in acute stroke patients. J Neuroimaging 2010;20(3):240–5. doi: 10.1111/j.1552-6569.2008.00358.x.
45. Bartkova A, Sanak D, Dostal J, et al. Acute ischaemic stroke in pregnancy: a severe complication of ovarian hyperstimulation syndrome. J Neurol Sci 2008;29(6):463–6.
46. Beneš V, Mohapl M, Kramář F, et al. Reconstructive surgery in cerebral ischemia: extracranial – intracranial arterial bypass – is revival possible? Adv Clin Exp Med 2000;9(Suppl 1):33–40.
47. Herzig R, Buřval S, Křupka B, et al. Comparison of ultrasonography, CT angiography, and digital subtraction angiography in severe carotid stenoses. Eur J Neurol 2004;11(11):774–81.
48. Herzig R, Hluštík P, Školoudík D, et al. Assessment of the cerebral vasomotor reactivity in internal carotid artery occlusion using a transcranial Doppler sonography and functional MRI. J Neuroimaging 2008;18(1):38–45. doi: 10.1111/j.1552-6569.2007.00168.x.
49. Herzig R, Urbánek K, Vlachová I, et al. Facilities for acute stroke patients care in the Czech Republic: nationwide epidemiological study. Eur J Epidemiol 2003;18(1):19–26.
50. Herzig R, Vlachová I, Křupka B, et al. Přínos existence iktové jednotky ke zlepšení diagnostiky u pacientů s cévními mozkovými příhodami. Cesk Slov Neurol N 2007;70/103(3):272–6.
51. Kalita Z, Keller O, Bar M, et al. Sekundární prevence recidivy po akutní cévní mozkové příhodě [(iCMP) – mozkovém infarktu/ tranzitorní ischemické atace (TIA) a hemoragické CMP]. In: Standardy léčebných postupů a indikátory kvality ve zdravotní péči. Praha: Verlag Dashöfer 2008 : 1–18.
52. Kalita Z. Doporučená léčba po prodělané cévní mozkové příhodě. Neurol Praxi 2002;3 : 308–15.
53. Kalvach P, Gregová D, Škoda O, et al. Cerebral blood supply with aging: normal, stenotic and recanalized. J Neurol Sci 2007;257(1–2):143–8.
54. Krahulík D, Vaverka M, Herzig R, et al. Extra intrakraniální mikroanastomosa: Metodika vyšetření a výsledky souboru pacientů. Cesk Slov Neurol N 2009;72/105(2):142–6.
55. Mikulík R, Neumann J, Václavík D, et al. Standard pro diagnostiku a léčbu pacientů s mozkovým infarktem. Cesk Slov Neurol N 2006;69/102(3):320–5.
56. Neumann J, Mikulík R, Václavík D, et al. Standard pro diagnostiku a léčbu pacientů po tranzitorní ischemické atace. Cesk Slov Neurol N 2006;69/102(3):326–30.
57. Neumann J, Škoda O. Sekundární prevence ischemických cévních mozkových příhod – přehled současných možností. Med Praxi 2007;5 : 233–6.
58. Neumann J. Diabetes mellitus ve vztahu k ischemické cévní mozkové příhodě. Cesk Slov Neurol N 2006;69/102(Suppl 2):14–5.
59. Neumann J. Role hyperlipidémie u iktů. Postgr Med 1999;4 : 68–70.
60. Neumann J. Současné možnosti péče o pacienta s akutní ischemickou cévní mozkovou příhodou. Med Praxi 2007;1 : 30–1.
61. Neumann J, Tomek A, Školoudík D, et al. Doporučený postup pro intravenózní trombolýzu v léčbě akutního mozkového infarktu – verze 2014. Cesk Slov Neurol N 2014;77(3):381–5.
62. Skoloudik D, Bar M, Skoda O, et al. Safety and efficacy of the sonographic acceleration of the middle cerebral artery recanalization results of the pilot thrombotripsy study. Ultrasound Med Biol 2008;34(11):1775–82. doi: 10.1016/j.ultrasmedbio.2008.04.002.
63. Šaňák D, Bártková A, Horák D, et al. Význam MR v indikaci systémové trombolýzy – analýza prvních 30 pacientů. Cesk Slov Neurol N 2007;70/103(2):143–51.
64. Šaňák D, Herzig R, Školoudík D, et al. The safety and efficacy of continuous transcranial duplex Doppler monitoring of middle cerebral artery occlusion in acute stroke patients: comparison of TCDD and thrombolysis in MCA recanalization. J Neuroimaging 2010;20(1):58–63. doi: 10.1111/j.1552-6569.2008.00354.x.
65. Šaňák D, Nosáľ V, Horák D, et al. Impact of diffusion-weighted MRI-measured initial cerebral infarction volume on clinical outcome in acute stroke patients with middle cerebral artery occlusion treated by thrombolysis. Neuroradiology 2006;48(9):632–9.
66. Šenkárová Z, Hluštík P, Otruba P, et al. Modulation of cortical activity in patients suffering from upper arm spasticity following stroke and treated with botulinum toxin A: an fMRI study. J Neuroimaging 2010;20(1):9–15. doi: 10.1111/j.1552-6569.2009.00375.x.
67. Škoda O. Antiagregace v sekundární prevenci cévní mozkové příhody. Interní Med 2006;12 : 534–8.
68. Škoda O, Herzig R, Mikulík R, et al. Klinický standard pro diagnostiku a léčbu pacientů s ischemickou cévní mozkovou příhodou a s tranzitorní ischemickou atakou. In: Národní sada klinických standardů. Praha: Národní referenční centrum 2011 : 1–39.
69. Škoda O, Kalvach P, Procházka B, et al. Non-invasive evaluation of proximal vertebral artery stenosis using color Doppler sonography and CT angiography. J Neuroradiol 2014;41(5):336–41. doi: 10.1016/j.neurad.2013.11.003.
70. Školoudík D, Bar M, Šaňák D, et al. D-dimers increase in acute ischemic stroke patients with the large artery occlusion, but do not depend on the time of artery recanalization. J Thromb Thrombolysis 2010;29(4):477–82. doi: 10.1007/s11239-009-0372-9.
71. Školoudík D, Bar M, Václavík D, et al. Riziko vzniku vaskulární příhody při léčbě fluvastatinem a fenofibrátem. Cesk Slov Neurol N 2007;70/103(2):163–7.
72. Školoudík D, Bar M, Zapletalová O, et al. Hladina D-dimerů u pacientů s akutní ischemickou cévní mozkovu příhodou. Cesk Slov Neurol N 2007;70/103(4):375–9.
73. Školoudík D, Fadrná T, Bar M, et al. Changes in haemocoagulation in healthy volunteers after a 1-hour thrombotripsy using a diagnostic 2 – 4 MHz transcranial probe. J Thromb Thrombolysis 2008;26(2):119–24.
74. Školoudík D, Fadrná T, Sedláková M, et al. Změny kognitivních funkcí u pacientů s akutní cévní mozkovou příhodou testovaných pomocí Mini-Mental State Examination a Clock-Drawing Test. Cesk Slov Neurol N 2007;70/103(4):282–7.
75. Školoudík D, Václavík D, Chudoba V, et al. Riziko vaskulární příhody u pacientů se stenózou intrakraniální tepny. Cesk Slov Neurol N 2006;69/102(5):355–9.
76. Školoudík D, Bar M, Mikulík R, et al. Standard pro podání systémové trombolýzy pacientům s akutním mozkovým infarktem. Cesk Slov Neurol N 2006;69/102(2):151–6.
77. Školoudík D, Bar M, Škoda O, et al. Účinnost sonotrombotripse a sonotrombolýzy v rekanalizaci střední mozkové tepny. Ces Slov Neurol N 2007;70/103(3):248–52.
78. Václavík D, Školoudík D, Škoda O, et al. Asociace vybraných rizikových faktorů s tíží aterosklerotického postižení v karotické bifurkaci. Cesk Slov Neurol N 2008;71/104(3):285–92.
79. Vlachová I, Herzig R, Vaverková H, et al. Prediktivní hodnota ultrasenzitivního C-reaktivního proteinu u cévní mozkové příhody a jeho vztah k ateroskleróze karotid. Cesk Slov Neurol N 2007;70/ 103(1):49–55.
80. Vlachová I, Krčová V, Herzig R, et al. Tkáňový aktivátor plazminogenu, inhibitor plazmatického aktivátoru-1 a von Willebrandův faktor v akutní a konvalescentní fázi ischemické cévní mozkové příhody. Cesk Slov Neurol N 2006;69/ 102(4):438 – 43.
81. Sedova P, Brown RD jr, Zvolsky M, et al. Validation of Stroke Diagnosis in the National Registry of Hospitalized Patients in the Czech Republic. J Stroke Cerebrovasc Dis 2015;24(9):2032–8. doi: 10.1016/j.jstrokecerebrovasdis.2015.04.019.
82. Haršány M, Kadlecová P, Svigelj V, et al.; for the SITS-EAST Investigators. Factors Influencing Door-to-Imaging Time: Analysis of the Safe Implementation of Treatments in Stroke-EAST Registry. J Stroke Cerebrovasc Dis 2014;23(8):2122–9. doi: 10.1016/j.jstrokecerebrovasdis.2014.03.019.
83. Mikulik R, Kadlecova P, Czlonkowska A, et al. Factors influencing in-hospital delay in treatment with intravenous thrombolysis. Stroke 2012;43(6):1578–83. doi: 10.1161/STROKEAHA.111.644120.
84. Mikulik R, Vaclavik D, Sanak D, et al. A nationwide study on topography and efficacy of the stroke treatment network in the Czech Republic. J Neurol 2010;257(1):31–7. doi: 10.1007/s00415-009-5259-3.
85. Connolly SJ, Ezekowitz MD, Yusuf S,et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009;361(12):1139 – 51. doi: 10.1056/NEJMoa0905561.
86. Patel MR, Mahaffey KW, Garg J, et al. Rivaroxaban versus warfarin in with nonvalvular atrial fibrillation. N Engl J Med 2011;365(10):883 – 91. doi: 10.1056/NEJMoa1009638.
87. Granger CB, Alexander JH, McMurray JJ, et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011;365(11):981 – 92. doi: 10.1056/NEJMoa1107039.
88. Diener HC, Connolly SJ, Ezekowitz MD, et al. Dabigatran compared with warfarin in patients with atrial fibrillation and previous transient ischaemic attack or stroke: a subgroup analysis of the RE-LY trial. Lancet Neurol 2010;9(12):1157–63. doi: 10.1016/S1474-4422(10)70274-X.
89. Alberts MJ, Eikelboom JW, Hankey GJ. Antithrombotic therapy for stroke prevention in non-valvular atrial fibrillation. Lancet Neurol 2012;11(12):1066–81. doi: 10.1016/S1474-4422(12)70258-2.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2016 Číslo 3
-
Všechny články tohoto čísla
- Pre-motorické a non-motorické príznaky Parkinsonovej choroby – taxonómia, klinická manifestácia a neuropatologické koreláty
- Majú bunkové terapie budúcnosť v liečbe extrapyramidových ochorení? ÁNO
- Mají buněčné terapie budoucnost v léčbě extrapyramidových onemocnění? NE
- Mají buněčné terapie budoucnost v léčbě extrapyramidových onemocnění?
- Atypický parkinsonizmus a frontotemporální demence – klinické, patologické a genetické aspekty
- MikroRNA u cerebrovaskulárních onemocnění – od patofyziologie k potenciálním biomarkerům
- Současné možnosti in vivo protonové (1H) MR spektroskopie v diagnostice mozkového abscesu
- Korelace intenzity fluorescence s proporcionálním zastoupením maligních buněk ve tkáni při resekci glioblastomu s použitím 5-ALA
- Validační studie české verze Bostonského testu pojmenování
- Periprocedurální komplikace a dlouhodobý efekt karotických angioplastik – výsledky z praxe
- Periprocedurální komplikace a dlouhodobý efekt karotických angioplastik – výsledky z praxe
- Baha jako možné řešení jednostranné hluchoty
- Léčba gama nožem u algických syndromů v inervační oblasti nervus glossopharyngeus
- Pacient s homozygozitou mutácie E200K v rodine slovenského klastru genetickej formy Creutzfeldtovej-Jakobovej choroby
- Schwannom nejspíše z krčního sympatiku – kazuistika
- Projekt ncRNAPain
- Využití zolpidemu v neurorehabilitaci pacienta ve stavu minimálního vědomí – kazuistika
- Klinický standard pro diagnostiku a léčbu pacientů s ischemickou cévní mozkovou příhodou a s tranzitorní ischemickou atakou – verze 2016
- Webové okénko
-
Analýza dat v neurologii
LVII. Koncept atributivního rizika v analýze populačních studií – IV. Hodnocení populačního efektu preventivních programů
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Schwannom nejspíše z krčního sympatiku – kazuistika
- Validační studie české verze Bostonského testu pojmenování
- Klinický standard pro diagnostiku a léčbu pacientů s ischemickou cévní mozkovou příhodou a s tranzitorní ischemickou atakou – verze 2016
- Pre-motorické a non-motorické príznaky Parkinsonovej choroby – taxonómia, klinická manifestácia a neuropatologické koreláty

