Kožní léze komplikující Parkinsonovu nemoc
The Skin Lesions as a Complications of Parkinson’s Disease
Aim:
We aimed to describe the incidence of pressure lesions (L89) and granulomatous lesion of the skin and subcutaneous tissues (L92) in the selected group of patients with Parkinson‘s disease (PD) (G20).
Material and methods:
We performed a retrospective analysis of data of Parkinson‘s disease patients from hospital information system from the year 2016. Parkinson‘s disease patients were followed in an outpatient Movement Disorder Centre of St. Anne’s University University Hospital in Brno.
Results:
We found 24 patients (3.1%) with pressure lesions and 16 patients (2.1%) with hypergranulations in postoperative scar in place of PEG insertion out of 776 patients (with 3,158 examinations during a selected period) data points. All patients included in the study had a main diagnosis of PD ranging from early form of the disease to a late stage with motor fluctuations and symptoms present (70%). In 94% of patients who suffered from pressure lesions we found partial or complete immobility.
Conclusion:
The incidence of pressure lesions was quite low, which can be cause either by low incidence or by methodological issues on a local level, or by a loss of data from institutional follow up care or home care. We have also found certain level of complications in patients treated by intradudodenal application of L DOPA, i.e. granulations in the skin opening at the point of PEG tube insertion.
Key words:
Parkinson‘s disease – skin lesions – pressure lesions – granulomatosis lesions – complications
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Autoři:
J. Búřil 1; P. Búřilová 2
Působiště autorů:
I. neurologická klinika
LF MU a FN u sv. Anny v Brně
1; Ústav zdravotnických informací
a statistiky ČR, Praha
2
Vyšlo v časopise:
Cesk Slov Neurol N 2017; 80(Supplementum 1): 50-53
Kategorie:
Původní práce
doi:
https://doi.org/10.14735/amcsnn2017S50
Souhrn
Cíl:
Zjistit výskyt dekubitálních lézí (L89) a granulomatózních onemocnění kůže a podkožního vaziva (L92) u vybraného souboru pacientů s Parkinsonovou nemocí (G20).
Soubor a metodika:
U souboru pacientů s Parkinsonovou nemocí dispenzarizovaných na specializované ambulanci Centra pro abnormní pohyby a parkinsonizmus I. neurologické kliniky LF MU a FN u sv. Anny v Brně byla provedena retrospektivní analýza dat nemocničního informačního systému (NIS) za rok 2016.
Výsledky:
Z 3 158 záznamů u 776 pacientů bylo identifikováno 24 (3,1 %) pacientů s dekubitální lézí a 16 (2,1 %) s hypergranulací v pooperační jizvě v místě zavedení perkutánní endoskopické gastrostomie (PEG) jejunální. Všichni hodnocení pacienti měli hlavní diagnózou Parkinsonova nemoc v rozsahu od incipientní diagnostikované nemoci až po fázi onemocnění s pozdními hybnými komplikacemi a rozvinutými symptomy (70 %). U 94 % pacientů s dekubitálními lézemi byla klinickým vyšetřením zjištěna částečná nebo úplná imobilita.
Závěr:
Výskyt dekubitálních lézí byl relativně nízký, což může být dáno reálně nízkou incidencí anebo nedostatečně propracovanou metodikou sběru dat na lokální úrovni a také ztrátou významných dat z pracovišť následné a domácí zdravotní péče. Prokázán byl výskyt komplikací u pacientů léčených intraduodenální aplikací L-DOPA formou PEG jejunální sondy v podobě granulací v oblasti zavedení PEG jejunální sondy.
Klíčová slova:
Parkinsonova nemoc – kožní léze – dekubitální léze – granulomatózní léze – komplikace
Úvod
Parkinsonova nemoc (G20) je chronické progresivní neurodegenerativní onemocnění centrálního nervového systému. V klinickém obrazu jsou nejnápadnější motorické symptomy, ale součástí jsou také desítky symptomů nemotorických [1,2]. Pacienti s Parkinsonovou nemocí mají rozmanitou motorickou symptomatologii, která zahrnuje jak hypokineticko-rigidní syndrom (v pokročilém stadiu též s poruchami stability a chůze, freeezingem), tak i hyperkinetické syndromy (např. tremor, dystonii, choreatické dyskineze v rámci tzv. pozdních hybných komplikací a tremor) [3].
Uvedená klinická symptomatologie je spojována s dalšími komplikacemi nejen v průběhu hospitalizační péče, ale i v následné rehabilitační a domácí zdravotní a laické péči. Konkrétní komplikace lze rozdělit na ty, které se dají do jisté míry lékařským a nelékařským zdravotnickým personálem a zdravotními službami ovlivnit, a ty, které lze ovlivnit zlepšením odborné péče pouze omezeně anebo vůbec.
Pacienti jsou během hospitalizace při dominanci posturální nestability ohroženi především pády s možností traumatického postižení pacienta s rizikem rozvoje dekubitů a event. i poškozením mechanizmu (hardwaru) zavedených systémů terapie pozdních hybných komplikací (hluboká mozková stimulace, apomorfinová pumpa, terapie L-DOPA formu perkutánní endoskopické gastrostomie (PEG) jejunální sondy) [4]. Komplikace jsou do značné míry ovlivnitelné intervencí lékaře s pečlivou kompenzací terapie Parkinsonovy nemoci (úprava dávky antiparkinsonské medikace nebo změna nastavení terapie intraduodenální L-DOPA, parametrů hluboké mozkové stimulace, dávky apomorfinu). Četnou skupinu komplikací představuje v případě dekompenzace parkinsonské symptomatologie a rozvoje výrazné rigidity s omezením hybnosti pacienta nebo imobilizace z jiné příčiny rozvoj dekubitálních lézí u pacientů se zvýšeným rizikem dle škály Nortonové, což následně vyžaduje intenzivní ošetřovatelskou a event. i chirurgickou péči [5,6]. Pacienti s uvedenými komplikacemi obvykle potřebují i další péči v rámci domácí zdravotní péče a rehabilitačního zařízení.
Zvláštní skupinou komplikací, které jsou do značné míry zdravotnickým personálem neovlivnitelné, je rozvoj granulací v oblasti zavedení PEG jejunální sondy. Povytažení PEG jejunální sondy zapříčiňuje vznik vnitřního dekubitu v oblasti žaludeční stěny při tlaku terče vnitřní části PEG jejunální sondy. V případě zavedení hardwaru v rámci operace hluboké mozkové stimulace (Deep Brain Stimulation; DBS) mohou vznikat kožní změny v oblasti implantátu s hrozbou rozvoje septické komplikace v místě implantace stimulátoru DBS, event. elektrod DBS a s možnou rejekcí implantovaného stimulátoru DBS [7,8].
Cíle
Cílem průzkumu bylo zjistit výskyt dekubitálních lézí (L89) a granulomatózních onemocnění kůže a podkožního vaziva (L92) u vybraného souboru pacientů s Parkinsonovou nemocí (G20).
Metodika
Analyzována byla data z nemocničního informačního systému (NIS) FN u sv. Anny v Brně za období leden – prosinec 2016. Zařazeny byly záznamy u pacientů s hlavní diagnózou Parkinsonova nemoc, kteří jsou dispenzarizováni na specializované ambulanci I. neurologické kliniky (I. NK) FN u sv. Anny v Brně. U pacientů s diagnózou G20 byl zjišťován záznam diagnózy dekubitální léze (L89) a granulomatózních onemocnění kůže a podkožního vaziva (L92) dle MKN-10.
Soubor
Celkem bylo analyzováno 3 158 záznamů u 776 pacientů s Parkinsonovou nemocí (MNK-10, G20) jako hlavní diagnózou u 100 % pacientů v daném souboru. V souboru bylo 58,4 % (n = 453) žen a 41,6 % (n = 323) mužů. Průměrný věk pacientů činil 64,8 let (min. věk 30, max. věk 82). Dekubitální léze a granulomatózní onemocnění kůže a podkožního vaziva byly identifikovány u celkem 40 (5,2 %) pacientů z celkového počtu 776 dispenzarizovaných pacientů na specializované ambulanci (I. NK) za stanovené období (stanoven leden – prosinec 2016 s ohledem na celkové množství záznamů a v souvislosti s v té době realizovanými změnami v hlášení nežádoucích událostí ve sledovaném zdravotnickém zařízení). Ve sledovaném souboru pacientů bylo 30 % v incipientní fázi onemocnění s plně rozvinutými symptomy Parkinsonovy choroby a u 70 % byly již rozvinuty pozdní hybné komplikace s fluktuacemi stavu ON/ OFF. Hybné komplikace byly ověřovány klinickým neurologickým vyšetřením pomocí škály Unified Parkinson‘s Disease Rating Scale (UPDRS) a Hoehn and Yahr škály (H-Y scale) [9,10], zobrazovacími metodami (počítačová tomografie mozku) a elektroencefalografií. Celý soubor pacientů byl diagnostikován dle standardních kritérií pro diagnostiku Parkinsonovy nemoci [11].
Graf 1 prezentuje počet pacientů ošetřených od ledna 2011 do prosince 2016 a nárůst kontrolních klinických vyšetření na specializované ambulanci. Přehled počtu klinických vyšetření uvádíme s cílem zjistit, zda ve sledovaném roce nedošlo k významné odchylce od let předchozích, kterou by nebylo možno vysvětlit s ohledem na dosavadní praxi na pracovišti.

Kontinuální zvyšování počtu kontrolních klinických vyšetření patrné v grafu souvisí zřejmě jednak se zvyšujícím se věkem dispenzarizovaných pacientů, jednak s faktem využívaných terapeutických intervencí, které vyžadují častější sledování pacientů (např. DBS). Frekvence kontrol ale také může souviset s výskytem komplikací, které je nezbytné odpovídajícím způsobem dokumentovat, což byl také jeden z hlavních motivů naší práce.
Výsledky a diskuze
Výskyt Parkinsonovy nemoci se má do roku 2030 zdvojnásobit [12]. Nejčastější výskyt onemocnění je prokázán ve věku 65 let, avšak jsou diagnostikováni i pacienti v mladším věku, asi 5 – 10 % je diagnostikovaných ve věku pod 50 let. U mužů je pozorováno o něco vyšší riziko rozvoje onemocnění než u žen [13]. V rámci realizovaného průzkumu byl potvrzen vyšší počet dispenzarizovaných mužů (58,4 %), průměrný věk v celém souboru byl 65 let a pouze 7 % pacientů ve sledovaném souboru bylo ve věku pod 50 let.
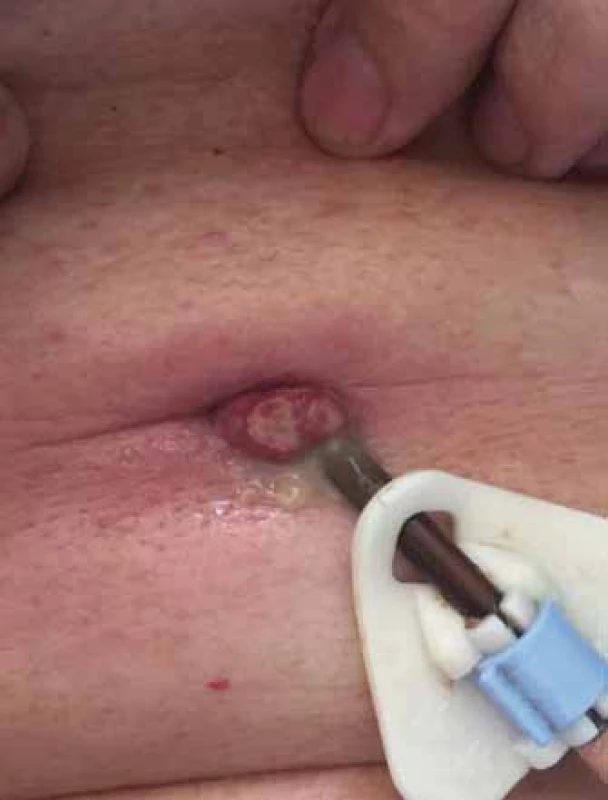
V České republice nejsou aktuálně k dispozici přesná data o počtu nemocných s Parkinsonovou nemocí. Poslední dostupné statistické údaje se vzájemně liší, přičemž Ústav zdravotnických informací a statistiky (ÚZIS ČR) uváděl v roce 2012 celkem 26 680 nemocných, podle Evropské asociace Parkinsonovy nemoci (EPDA) to bylo 18 000 a podle publikace Parkinsonova nemoc z různých pohledů to bylo 15 000 [14]. Jak bylo uvedeno výše, zejména pacienti s pokročilým onemocněním trpí omezenou mobilitou a ta je rizikovým faktorem vzniku dekubitálních lézí. Dle další podrobné analýzy, v níž byl využit Národní registr hospitalizovaných (NRHOSP), ve sledovaném období let 2007 – 2014 bylo zjištěno celkem 1 707 (34,7 %) vykázaných diagnóz L89 u skupin pacientů s neurodegenerativním a onkologickým onemocněním z celkového počtu 4 924 hodnocených záznamů. Jednalo se především o dekubitální léze vyššího stupně, avšak ve skupině neurodegenerativních onemocnění nebyla Parkinsonova nemoc přímo specifikována [15]. V rámci specializované ambulance na I. NK bylo hodnoceno celkem 776 pacientů. Záchyt dekubitálních lézí byl 3,1 % a granulomatózních onemocnění kůže a podkožního vaziva 2,7 %. Dekubitální léze se vyskytovaly v lokalizaci: sakrum v 62,5 %, paty ve 25 % a kombinace obou v 12,5 %. Granulomatózní onemocnění bylo přítomno pouze u pacientů léčených intraduodenální aplikací L-DOPA formou PEG jejunální sondy (obr. 1), kteří podstupovali pravidelná kontrolní vyšetření na sledovaném pracovišti. Celkový počet léčených pacientů intraduodenální aplikaci L-DOPA činil 45 za vybrané období, u 16 (35,5 %) z nich se vyskytly kožní komplikace. U pacientů s granulomatózní komplikací byla jediná možnost léčby chirurgické snesení granulátu, jak doporučuje odborná literatura [16].
Bylo prokázáno, že mezi časté nemotorické příznaky u pacientů s Parkinsonovou nemocí patří poruchy autonomních nervových funkcí. Vyskytují se až u 80 % nemocných a pro svůj výrazný negativní dopad na každodenní život představují závažný zdravotní problém [17]. Souvisí také s rizikem vzniku poruchy tkáňové a kožní integrity. Dochází též k dalším změnám kůže, které se objevují v důsledku Parkinsonovy nemoci, a to hypersalivace, hyperhidróza, seborea či maligní kožní léze [18]. Podráždění a léze kožního krytu mohou vyvolat také aplikace transdermálních náplastí využívaných v symptomatické terapii příznaků Parkinsonovy nemoci nebo kognitivní dysfunkce, což je zatím ověřeno na pracovišti autorů empiricky. Mezi další faktory zvyšující riziko vzniku dekubitálních lézí řadíme imobilitu, s níž souvisí jiné rizikové faktory, jako zvýšené pocení a inkontinence. U 94 % pacientů s nálezem dekubitů zařazených v průzkumu byla klinickým vyšetřením potvrzena částečná nebo úplná imobilita (UPDRS, H-Y). Ta je jedním z rizikových faktorů vzniku dekubitálních lézí, avšak dokumentovaný výskyt dekubitálních lézí byl nízký (n = 24; 3,1 %). Lze předpokládat, že za hospitalizace byl výskyt dekubitálních lézí nízký vzhledem k poskytování kvalitní ošetřovatelské péče nelékařského zdravotnického personálu za spoluúčasti rehabilitační péče. Možným důvodem nízkého záchytu v rámci ambulantní dispenzární péče je nedostatečně propracovaná metodika sběru dat na lokální úrovni [19]. Dalším možným vysvětlením, které by vyžadovalo doplňující analýzu, je nedostatečná kontinuita péče a transfer informací při zajištění péče v rámci pracovišť následné a domácí zdravotní péče.
Závěr
V České republice aktuálně chybí národní strategie pro Parkinsonovu nemoc. Neexistuje doposud propracovaný mezioborový systém péče a zajištění kontinuity péče a návaznost na domácí zdravotní péči s cílem zvýšit kvalitu života a prodloužit tím soběstačnost pacientů, což by vedlo k předcházení a zmírnění úpadku psychických i fyzických sil u nemocných. Retrospektivní analýzou dat z nemocničního informačního systému byl prokázán výskyt komplikací u pacientů léčených intraduodenální aplikací L-DOPA formou PEG jejunální sondy ve formě granulomatózního onemocnění v ústí sondy. Výskyt dekubitálních lézí byl zjištěn nízký (3,1 %), což může být dáno reálně nízkou incidencí. Druhým možným zdůvodněním je nedostatečně propracovaná metodika sběru dat na lokální úrovni sledovaného pracoviště a potenciálně riziko ztráty významných dat z pracovišť následné a domácí zdravotní péče. Vhodným řešením by byl terénní pracovník v rámci specializované ambulance I. NK, který by docházel za dispenzarizovanými pacienty do domácího prostředí a edukoval je a příbuzné o preventivních a režimových opatřeních v rámci léčby. Dalším východiskem je úprava metodického materiálu pro lokální sběr dat zaměřených na výskyt kožních komplikací (dekubitální léze a nehojící se rány), která je aktuálně naplánována a měla by umožnit další sledování komplikací u dispenzarizovaných pacientů.
Děkujeme členům týmu Centra pro abnormní pohyby a parkinsonizmus při I. neurologické klinice LF MU a FN u sv. Anny v Brně za poskytnutí dat k provedení průzkumu.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Přijato k recenzi: 15. 6. 2017
Přijato do tisku: 3. 7. 2017
MUDr. Jiří Búřil
I. neurologická klinika
LF MU a FN u sv. Anny v Brně
Pekařská 53
656 91 Brno
e-mail: jiri.buril@fnusa.cz
Zdroje
1. Pfeiffer RF, Wszolek ZK, Ebadi M. Parkinson‘s Disease. 2nd ed. CRC Press 2012 : 14 – 6.
2. Tarakad A, Jankovic J. Diagnosis and Management of Parkinson‘s Disease. Semin Neurol 2017;37(2):118 – 26. doi: 10.1055/ s-0037-1601888.
3. National Institue of Neurological Disorders and Stroke. Parkinson‘s Disease Information Page 2017. [online]. Available from URL: https:/ / www.ninds.nih.gov/ Disorders/ All-Disorders/ Parkinsons-Disease-Information-Page.
4. Menšíková K, Bareš M, Kaňovský P, et al. Atypické parkinsonské syndromy. Praha: Galén 2015 : 13 – 21.
5. Majkusová K, Jarošová D. Falls risk factors in an acute – care setting: a retrospective study. Cent Eur J Nurs Midwifery 2014;5(2):47 – 53.
6. Jurásková D. Pády a zranění pacientů v souvislosti s poskytováním zdravotní a sociální péče. Ošetřovatelství teorie a praxe moderního ošetřovatelství 2008;10(34):58 – 75.
7. Bareš M, Kianička B. Léčba Parkinsonovy nemoci. Neurol Praxi 2014;15(2):105 – 8.
8. Leibson CL, Maraganore DM, Bower JH, et al. Comorbid conditions associated with Parkinson’s disease: a population-based study. Mov Disord 2006;21(4):446 – 55.
9. Goetz CG, Tilley BC, Shaftman SR, et al. Movement Disorder Society-sponsored revision of the unified Parkinson’s Disease Rating Scale (MDS-UPDRS): scale presentation and clinimetric testing results. Mov Disord 2008;23(15):2129 – 70. doi: 10.1002/ mds.22340.
10. Goetz CG, Poewe W, Racol O, et al. Movement Disorder Society Task Force report on the Hoehn and Yahr staging scale: status and recommendations. Mov Disord 2004;9(9):1020 – 8. doi: 10.1002/ mds.20213.
11. Sorbi S, Hort J, Erkinjuntti T, et al. EFNS-ENS Guidelines on the diagnosis and management of disorders associated with dementia. Eur J Neurol 2012;19(9):1159 – 79. doi: 10.1111/ j.1468-1331.2012.03784.x.
12. National Parkinson Foundation. Parkinson’s DiseaseOverview 2016. [online]. Available from URL: www.parkinson.org/ parkinson-s-disease.aspx.
13. Henchcliffe C, Severt WL. Disease modification in Parkinson’s disease. Drugs Aging 2011;28(8):605 – 15. doi: 10.2165/ 11591320-000000000-00000.
14. Kolektiv autorů. Parkinsonova nemoc z různých pohledů. Společnost Parkinson, Praha 2013. [online]. Dostupné z URL: http:/ / parkinson-help.cz/ tiskova-zprava-2/ .
15. Pokorná A, Benešová K, Mužík J, et al. Sledování dekubitálních lézí u pacientů s neurologickým onemocněním – analýza Národního registru hospitalizovaných. Cesk Slov Neurol N 2016;79(Suppl 1):S8 – 14. doi: 10.14735/ amcsnn2016S8.
16. Fischer M, Gemende I, Marsch W, et al. Skin function and skin disorders in Parkinson’s Disease. J Neur Trans 2001;108(2):205 – 13.
17. Beitz JM. Skin and wound issues in patients with Parkinson’s disease: an overview of common disorders. Ostomy Wound Manage 2013;59(6):26 – 36.
18. Průzkum agentury STEM/ MARK pro Parkinson – Help, o.s., březen 2015. [online]. Dostupné z URL: http:/ / parkinson-help.cz/ tiskova-zprava-2/ .
19. Pokorná A, Benešová K, Jarkovský J, et al. PressureInjuries in Inpatient Care Facilities in the Czech Republic: Analysis of a National Electronic Database. J WoundOstomy Continence Nurs 2017;44(4):1 – 5. doi: 10.1097/ WON.0000000000000344.
Štítky
Dětská neurologie Neurochirurgie NeurologieČlánek vyšel v časopise
Česká a slovenská neurologie a neurochirurgie

2017 Číslo Supplementum 1
-
Všechny články tohoto čísla
- Léčba ran – farmakoekonomická data z pohledu poskytovatele a plátce péče
- Deformace je „zabiják“ buněk – implikace pro ochranu osob s poraněním míchy před vznikem dekubitů
- Vztah mezi rizikovými faktory, hodnocením rizika a patologií vzniku dekubitální léze
- Diferenciální diagnostika dekubitů a dekubity vznikající v souvislosti s přístrojovou technikou
- Možnosti hodnocení psychometrických vlastností škál pro hodnocení rizika vzniku tlakových lézí na vybraných pracovištích v intenzivní péči – pilotní studie
- Využití lalokových plastik v operační léčbě dekubitů
- Výskyt dekubitů u pacientů s lézí míšní na spinální jednotce Kliniky úrazové chirurgie LF MU a FN Brno 2013– 2016
- Kožní léze komplikující Parkinsonovu nemoc
- Validizace ošetřovatelské diagnózy akutní a chronická bolest dle NANDA International u pacientů s ránou
- Dekubity jsou pro mne stále noční můrou
- Editorial
- Datové zdroje pro sledování nehojících se ran v Národním zdravotnickém informačním systému – epidemiologie nehojících se ran v České republice – analýza Národního registru hospitalizovaných v letech 2007– 2015
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Validizace ošetřovatelské diagnózy akutní a chronická bolest dle NANDA International u pacientů s ránou
- Využití lalokových plastik v operační léčbě dekubitů
- Diferenciální diagnostika dekubitů a dekubity vznikající v souvislosti s přístrojovou technikou
- Dekubity jsou pro mne stále noční můrou
